回答下列问题:
(1)麻醉剂的发现和使用是人类医学史上一项了不起的成就。一种常用麻醉剂氯仿常因保存不慎而被氧化,产生剧毒光气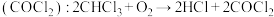 ,光气
,光气 分子的立体构型是
分子的立体构型是________ 形。
(2)某有机物的结构简式为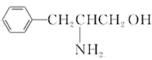 。该有机物分子是
。该有机物分子是____________ (填“极性”或“非极性”)分子,该有机物分子中采取 杂化的原子对应元素的电负性由大到小的顺序为
杂化的原子对应元素的电负性由大到小的顺序为____________ 。
(3)乙二胺 分子中氮原子杂化类型为
分子中氮原子杂化类型为_________________ 。
(4)叠氮化合物是一类重要的化合物,其中氢叠氮酸( )是一种弱酸,其分子结构可表示为
)是一种弱酸,其分子结构可表示为 ,肼
,肼 被亚硝酸氧化时便可得到氢叠氮酸
被亚硝酸氧化时便可得到氢叠氮酸 ,发生的反应为
,发生的反应为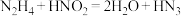 。
。 的酸性和醋酸相近,可微弱电离出
的酸性和醋酸相近,可微弱电离出 和
和 。
。
①叠氮酸根能与许多金属离子等形成配合物,如 ,根据价层电子对互斥理论判断
,根据价层电子对互斥理论判断 的空间构型为
的空间构型为________________ 。
②下列有关说法正确的是_____________ (填序号)。
A. 中含有5个
中含有5个 键
键
B. 中的三个氮原子均采用
中的三个氮原子均采用 杂化
杂化
C. 、
、 、
、 、
、 都是极性分子
都是极性分子
D.肼 的沸点高达
的沸点高达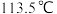 ,说明肼分子间可形成氢键
,说明肼分子间可形成氢键
(1)麻醉剂的发现和使用是人类医学史上一项了不起的成就。一种常用麻醉剂氯仿常因保存不慎而被氧化,产生剧毒光气
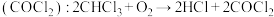 ,光气
,光气 分子的立体构型是
分子的立体构型是(2)某有机物的结构简式为
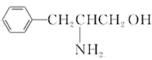 。该有机物分子是
。该有机物分子是 杂化的原子对应元素的电负性由大到小的顺序为
杂化的原子对应元素的电负性由大到小的顺序为(3)乙二胺
 分子中氮原子杂化类型为
分子中氮原子杂化类型为(4)叠氮化合物是一类重要的化合物,其中氢叠氮酸(
 )是一种弱酸,其分子结构可表示为
)是一种弱酸,其分子结构可表示为 ,肼
,肼 被亚硝酸氧化时便可得到氢叠氮酸
被亚硝酸氧化时便可得到氢叠氮酸 ,发生的反应为
,发生的反应为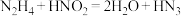 。
。 的酸性和醋酸相近,可微弱电离出
的酸性和醋酸相近,可微弱电离出 和
和 。
。①叠氮酸根能与许多金属离子等形成配合物,如
 ,根据价层电子对互斥理论判断
,根据价层电子对互斥理论判断 的空间构型为
的空间构型为②下列有关说法正确的是
A.
 中含有5个
中含有5个 键
键B.
 中的三个氮原子均采用
中的三个氮原子均采用 杂化
杂化C.
 、
、 、
、 、
、 都是极性分子
都是极性分子D.肼
 的沸点高达
的沸点高达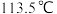 ,说明肼分子间可形成氢键
,说明肼分子间可形成氢键
更新时间:2024-03-27 22:20:26
|
相似题推荐
【推荐1】元素周期表中锑元素的数据如图。

(1)根据锑的价层电子排布式5s25p3可知,锑在元素周期表中位于第___________ 周期,第___________ 族。
(2)基态锑原子中有___________ 个未成对电子,这些未成对电子具有___________ (填“相同”或“不同”)的自旋状态。
(3)基态锑原子的5s轨道形状为___________ 形,该原子最外层电子占有___________ 个轨道。
(4)Bi在元素周期表中与Sb相邻,位于Sb的正下方。则两种元素的电负性Sb___________ Bi;原子半径Sb___________ Bi (填“>”或“<”)。

(1)根据锑的价层电子排布式5s25p3可知,锑在元素周期表中位于第
(2)基态锑原子中有
(3)基态锑原子的5s轨道形状为
(4)Bi在元素周期表中与Sb相邻,位于Sb的正下方。则两种元素的电负性Sb
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】氢能的存储是其应用的主要瓶颈,配位氢化物、富氢载体化合物是目前所采用的主要储氢材料。
(1)Ti(BH4)2是一种过渡元素硼氢化物储氢材料。在基态Ti2+中,电子占据的最高能层符号为________ ,该能层具有的原子轨道数为________ 。
(2)液氨是富氢物质,是氢能的理想载体,利用N2+3H2 2NH3实现储氢和输氢。下列说法正确的是
2NH3实现储氢和输氢。下列说法正确的是( )
(3)已知NF3与NH3的空间构型相同,但NF3不易与Cu2+形成配离子,其原因是___________ 。
(1)Ti(BH4)2是一种过渡元素硼氢化物储氢材料。在基态Ti2+中,电子占据的最高能层符号为
(2)液氨是富氢物质,是氢能的理想载体,利用N2+3H2
 2NH3实现储氢和输氢。下列说法正确的是
2NH3实现储氢和输氢。下列说法正确的是| A.NH3分子中氮原子的轨道杂化方式为sp2杂化 |
| B.NH4+与PH4+、CH4、BH4-、ClO4-互为等电子体 |
| C.相同压强下,NH3沸点比PH3的沸点高 |
| D.[Cu(NH3)4]2+中,N原子是配位原子 |
(3)已知NF3与NH3的空间构型相同,但NF3不易与Cu2+形成配离子,其原因是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】完成下列表格
| 粒子 | 空间结构 | 杂化类型 |
 | ||
 |
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】 与
与 的中心原子均为
的中心原子均为 杂化,二者键角:
杂化,二者键角:
___________  (填“>”“=”或“<”),从结构角度说明原因:
(填“>”“=”或“<”),从结构角度说明原因:___________ 。
 与
与 的中心原子均为
的中心原子均为 杂化,二者键角:
杂化,二者键角:
 (填“>”“=”或“<”),从结构角度说明原因:
(填“>”“=”或“<”),从结构角度说明原因:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】回答下列问题
(1)用VSEPR 理论判断:
(2)基态Fe原子有___________ 个未成对电子,Fe3+的价电子排布式为___________ 。Fe在周期表中位于___________ 列。
(3)Cl的核外电子排布式为___________ 。
(4)22Ti的原子结构示意图___________ 。
(5)Sn为ⅣA族元素,单质Sn与干燥 反应生成
反应生成 。常温常压下
。常温常压下 为无色液体,
为无色液体, 空间构型为
空间构型为___________ 。
(1)用VSEPR 理论判断:
| 物质 | 孤对电子对数 | 轨道杂化方式 | 分子或离子的空间结构 |
PO | |||
| COCl2 |
(3)Cl的核外电子排布式为
(4)22Ti的原子结构示意图
(5)Sn为ⅣA族元素,单质Sn与干燥
 反应生成
反应生成 。常温常压下
。常温常压下 为无色液体,
为无色液体, 空间构型为
空间构型为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】已知: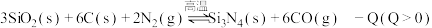 ,在反应条件下,向
,在反应条件下,向 密闭容器中加入反应物,
密闭容器中加入反应物, 后达到平衡。完成下列填空:
后达到平衡。完成下列填空:
(1)氮原子的核外电子排布式:_______ ;硅原子核外电子的运动状态有_______ 种。
(2)上述反应混合物中的极性分子是_______ ,写出非极性分子的电子式_______ 。
(3)将 三种离子的半径按由大到小的顺序排列
三种离子的半径按由大到小的顺序排列_______ 。
(4)氧原子核外电子有_______ 种能量不同的轨道。 属于
属于_______ 晶体。
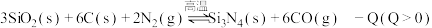 ,在反应条件下,向
,在反应条件下,向 密闭容器中加入反应物,
密闭容器中加入反应物, 后达到平衡。完成下列填空:
后达到平衡。完成下列填空:(1)氮原子的核外电子排布式:
(2)上述反应混合物中的极性分子是
(3)将
 三种离子的半径按由大到小的顺序排列
三种离子的半径按由大到小的顺序排列(4)氧原子核外电子有
 属于
属于
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】乙炔( )、丙烯腈(
)、丙烯腈( )、乙烯酮(
)、乙烯酮(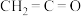 )是有机合成工业的重要原料。工业上曾用
)是有机合成工业的重要原料。工业上曾用 和
和 反应制取乙炔,用乙炔和氢氰酸(HCN)在氯化亚铜等催化作用下生产丙烯腈,乙炔与
反应制取乙炔,用乙炔和氢氰酸(HCN)在氯化亚铜等催化作用下生产丙烯腈,乙炔与 在一定条件下反应生成乙烯酮。回答下列问题:
在一定条件下反应生成乙烯酮。回答下列问题:
(1)写出基态钙原子的核外电子排布式:___________ ;Cu元素在元素周期表中的位置为___________ 。
(2)乙炔分子的空间结构为___________ ,乙炔分子属于___________ (填“极性”或“非极性”)分子。
(3)丙烯腈分子中碳原子的杂化轨道类型是___________ 。
(4)乙烯酮在室温下可聚合成二聚乙烯酮(结构简式为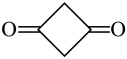 ),二聚乙烯酮分子中含有的
),二聚乙烯酮分子中含有的 键与
键与 键的数目之比为
键的数目之比为___________ 。
 )、丙烯腈(
)、丙烯腈( )、乙烯酮(
)、乙烯酮(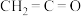 )是有机合成工业的重要原料。工业上曾用
)是有机合成工业的重要原料。工业上曾用 和
和 反应制取乙炔,用乙炔和氢氰酸(HCN)在氯化亚铜等催化作用下生产丙烯腈,乙炔与
反应制取乙炔,用乙炔和氢氰酸(HCN)在氯化亚铜等催化作用下生产丙烯腈,乙炔与 在一定条件下反应生成乙烯酮。回答下列问题:
在一定条件下反应生成乙烯酮。回答下列问题:(1)写出基态钙原子的核外电子排布式:
(2)乙炔分子的空间结构为
(3)丙烯腈分子中碳原子的杂化轨道类型是
(4)乙烯酮在室温下可聚合成二聚乙烯酮(结构简式为
 ),二聚乙烯酮分子中含有的
),二聚乙烯酮分子中含有的 键与
键与 键的数目之比为
键的数目之比为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】叠氮化钠(NaN3)是一种无色结晶,广泛用于汽车安全气囊及化工合成等.常见的两种制备方法为:2NaNH2+N2O=NaN3+NaOH+NH3、3NaNH2+NaNO3=NaN3+3NaOH+NH3↑
(1)下列说法正确的是________ .
A. N3-与N2O互为等电子体
B. NaN3、NaNH2、NaOH、NaNO3均为离子化合物
C. NaNH2熔点(210℃)比NaOH 熔点(318.4℃)低,是因为前者相对分子质量小
(2)NH3沸点(﹣33.34℃)比N2O沸点(﹣88.49℃)高,其主要原因:________
(3)依据价层电子对互斥理论,NO3-空间构型呈________ 形。
(1)下列说法正确的是
A. N3-与N2O互为等电子体
B. NaN3、NaNH2、NaOH、NaNO3均为离子化合物
C. NaNH2熔点(210℃)比NaOH 熔点(318.4℃)低,是因为前者相对分子质量小
(2)NH3沸点(﹣33.34℃)比N2O沸点(﹣88.49℃)高,其主要原因:
(3)依据价层电子对互斥理论,NO3-空间构型呈
您最近一年使用:0次
【推荐2】(1)已知常压下,乙醇沸点为78.5℃,而与其分子量接近的丙烷的沸点是-42.1℃,两者沸点相差如此之大的主要原因是___________ 。
(2)AlCl3可作净水剂,其理由是___________ (用必要的方程式和相关文字说明)。
(3)丙氨酸的结构简式___________ 。
(2)AlCl3可作净水剂,其理由是
(3)丙氨酸的结构简式
您最近一年使用:0次

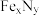 )在磁记录材料领域有着广泛的应用前景。某
)在磁记录材料领域有着广泛的应用前景。某 基态核外电子排布式为
基态核外电子排布式为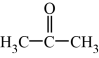 )分子中碳原子轨道的杂化类型是
)分子中碳原子轨道的杂化类型是 (直线形分子)、
(直线形分子)、 (平面三角形分子)、
(平面三角形分子)、 (正四面体型分子)都是非极性分子,
(正四面体型分子)都是非极性分子, (V形分子)都是极性分子。请分析什么样的
(V形分子)都是极性分子。请分析什么样的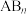 型分子为非极性分子
型分子为非极性分子

