氢能的存储是其应用的主要瓶颈,配位氢化物、富氢载体化合物是目前所采用的主要储氢材料。
(1)Ti(BH4)2是一种过渡元素硼氢化物储氢材料。在基态Ti2+中,电子占据的最高能层符号为________ ,该能层具有的原子轨道数为________ 。
(2)液氨是富氢物质,是氢能的理想载体,利用N2+3H2 2NH3实现储氢和输氢。下列说法正确的是
2NH3实现储氢和输氢。下列说法正确的是( )
(3)已知NF3与NH3的空间构型相同,但NF3不易与Cu2+形成配离子,其原因是___________ 。
(1)Ti(BH4)2是一种过渡元素硼氢化物储氢材料。在基态Ti2+中,电子占据的最高能层符号为
(2)液氨是富氢物质,是氢能的理想载体,利用N2+3H2
 2NH3实现储氢和输氢。下列说法正确的是
2NH3实现储氢和输氢。下列说法正确的是| A.NH3分子中氮原子的轨道杂化方式为sp2杂化 |
| B.NH4+与PH4+、CH4、BH4-、ClO4-互为等电子体 |
| C.相同压强下,NH3沸点比PH3的沸点高 |
| D.[Cu(NH3)4]2+中,N原子是配位原子 |
(3)已知NF3与NH3的空间构型相同,但NF3不易与Cu2+形成配离子,其原因是
2016·海南·一模 查看更多[1]
更新时间:2016-12-09 07:53:25
|
相似题推荐
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】含Cu、Zn、Sn及S的四元半导体化合物(简写为CZTS),是一种低价、无污染的绿色环保型光伏材料,可应用于薄膜太阳能电池领域。回答下列问题:
(1)基态S原子的价电子中,两种自旋状态的电子数之比为___________ 。
(2)Cu与Zn相比,第二电离能与第一电离能差值更大的是___________ ,原因是___________ 。
(3)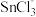 的几何构型为
的几何构型为___________ 。
(4)将含有未成对电子的物质置于外磁场中,会使磁场强度增大,称其为顺磁性物质,下列物质中,属于顺磁性物质的是___________填标号)。
(1)基态S原子的价电子中,两种自旋状态的电子数之比为
(2)Cu与Zn相比,第二电离能与第一电离能差值更大的是
(3)
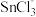 的几何构型为
的几何构型为(4)将含有未成对电子的物质置于外磁场中,会使磁场强度增大,称其为顺磁性物质,下列物质中,属于顺磁性物质的是___________填标号)。
| A.[Cu(NH3)2]Cl | B.[Cu(NH3)4]SO4 | C.[Zn(NH3)4]SO4 | D.Na2[Zn(OH)4] |
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】有A、B、C、D、E、F六种元素,它们的相关信息如下表:
请填写下列空格:
(1)A原子的电子式:_____ 。
(2)B离子的结构示意图:_______ 。
(3)C元素的名称:___ ,C原子中能量最高的电子位于第______ 层,与C离子质子数与电子数均相同的微粒可能是______ (用微粒符号表示)。
(4)D的二价阴离子的电子式:___ ,D元素的某种同位素原子质量数为34,该原子核内的中子数为_____ 。
(5)A、B、E三种元素形成的化合物常用于吸收F单质,反应的化学方程式:_____________ 。
| 元素代号 | 相关信息 |
| A | 最外层的电子数是次外层电子数的3倍 |
| B | 海水中含量第一位的金属元素 |
| C | L层得1个电子后成为稳定结构 |
| D | 二价阴离子核外有18个电子 |
| E | 失去一个电子后就成为一个质子 |
| F | 单质为黄绿色气体,具有刺激性气味 |
请填写下列空格:
(1)A原子的电子式:
(2)B离子的结构示意图:
(3)C元素的名称:
(4)D的二价阴离子的电子式:
(5)A、B、E三种元素形成的化合物常用于吸收F单质,反应的化学方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】由氧化物经氯化作用生成氯化物是工业生产氯化物的常用方法,Cl2、CCl4是常用的氯化剂。如:
Na2O+Cl2=2NaCl+O2
CaO+Cl2=CaCl2+O2
SiO2+2CCl4=SiCl4+2COCl2
Cr2O3+3CCl4=2CrCl3+3COCl2
请回答下列问题:
(1)Cr2O3、CrCl3中Cr均为+3价,写出Cr3+的基态电子排布式______________ ;
(2)CCl4分子中C原子采取__________ 杂化成键。
(3)COCl2俗称光气,分子中C原子采取sp2杂化成键。光气分子的结构式是_________ ,其中碳氧原子之间共价键是________ (填序号):
a.2个σ键b.2个π键c.1个σ键、1个π键
(4)CaO晶胞如右上图所示,CaO晶体中Ca2+的配位数为____ 。CaO晶体和NaCl晶体中离子排列方式相同,其晶格能分别为:CaO-3 401kJ•mol-1、NaCl-786kJ•mol-1。导致两者晶格能差异的主要原因是_________________________________ 。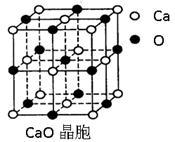
Na2O+Cl2=2NaCl+O2
CaO+Cl2=CaCl2+O2
SiO2+2CCl4=SiCl4+2COCl2
Cr2O3+3CCl4=2CrCl3+3COCl2
请回答下列问题:
(1)Cr2O3、CrCl3中Cr均为+3价,写出Cr3+的基态电子排布式
(2)CCl4分子中C原子采取
(3)COCl2俗称光气,分子中C原子采取sp2杂化成键。光气分子的结构式是
a.2个σ键b.2个π键c.1个σ键、1个π键
(4)CaO晶胞如右上图所示,CaO晶体中Ca2+的配位数为

您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】很多含巯基(-SH)的有机化合物是重金属元素汞的解毒剂。例如,解毒剂化合物Ⅰ可与氧化汞生成化合物Ⅱ。
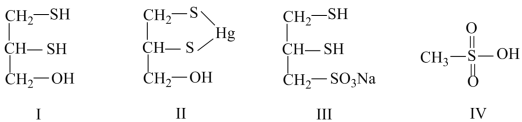
(1)1mol化合物Ⅰ含有_______ mol σ键。
(2)基态硫原子价层电子排布式为_______ 。
(3)H2S、CH4、H2O的沸点由高到低顺序为_______ 。
(4)汞的原子序数为80,位于元素周期表第_______ 周期第ⅡB族。
(5)化合物Ⅲ也是一种汞解毒剂。化合物Ⅳ是一种强酸。下列说法正确的有_______ 。
A.在Ⅰ中S原子采取sp3杂化
B.在Ⅱ中S元素的电负性最大
C.在Ⅲ中C-C-C键角是180°
D.在Ⅲ中存在离子键与共价键
E.在Ⅳ中硫氧键的键能均相等

(1)1mol化合物Ⅰ含有
(2)基态硫原子价层电子排布式为
(3)H2S、CH4、H2O的沸点由高到低顺序为
(4)汞的原子序数为80,位于元素周期表第
(5)化合物Ⅲ也是一种汞解毒剂。化合物Ⅳ是一种强酸。下列说法正确的有
A.在Ⅰ中S原子采取sp3杂化
B.在Ⅱ中S元素的电负性最大
C.在Ⅲ中C-C-C键角是180°
D.在Ⅲ中存在离子键与共价键
E.在Ⅳ中硫氧键的键能均相等
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】非线性光学晶体在信息、激光技术、医疗、国防等领域有重要应用价值。我国科学家利用Cs2CO3、XO2(X=Si、Ge)和H3BO3首次合成了组成为CsXB3O7的非线性光学晶体。回答下列问题:
(1)C、O、Si三种元素电负性由大到小的顺序为___________ ;第一电离能 I1(Si)___________ I1(Ge)(填>或<)。
(2)基态Ge原子核外电子排布式为___________ ;SiO2、GeO2具有类似的晶体结构,其中熔点较高的是___________ ,原因是___________ 。
(3)图中为硼酸晶体的片层结构,其中硼的杂化方式为___________ 。H3BO3在热水中比冷水中溶解度显著增大的主要原因是___________
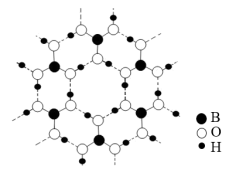
(1)C、O、Si三种元素电负性由大到小的顺序为
(2)基态Ge原子核外电子排布式为
(3)图中为硼酸晶体的片层结构,其中硼的杂化方式为

您最近一年使用:0次
【推荐3】 有电极化特性、非磁绝缘性、光致发光性等多种优异性能。回答下列问题:
有电极化特性、非磁绝缘性、光致发光性等多种优异性能。回答下列问题:
(1)基态Co原子的价层电子排布图为_______ 。
(2) 、
、 、
、 的键角由大到小的顺序为
的键角由大到小的顺序为_______ ;C、N、O、F的第一电离能由大到小的顺序为_______ 。
(3)碱金属离子镶入适合的冠醚空腔可形成特殊材料,两种冠醚结构如图1所示。
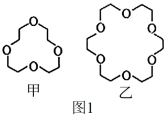
冠醚中O原子的杂化形式为_______ ;H、C、O的电负性由小到大的顺序为_______ 。
(4) 的晶胞如图2所示。处于面心的F形成正八面体空隙,Co处于体心,K处于顶点。
的晶胞如图2所示。处于面心的F形成正八面体空隙,Co处于体心,K处于顶点。

①每个晶胞中由K和F共同形成的正四面体空隙有_______ 个。
②晶胞的另一种表示中,Co处于各顶角位置,则K处于_______ 位置。
 有电极化特性、非磁绝缘性、光致发光性等多种优异性能。回答下列问题:
有电极化特性、非磁绝缘性、光致发光性等多种优异性能。回答下列问题:(1)基态Co原子的价层电子排布图为
(2)
 、
、 、
、 的键角由大到小的顺序为
的键角由大到小的顺序为(3)碱金属离子镶入适合的冠醚空腔可形成特殊材料,两种冠醚结构如图1所示。

冠醚中O原子的杂化形式为
(4)
 的晶胞如图2所示。处于面心的F形成正八面体空隙,Co处于体心,K处于顶点。
的晶胞如图2所示。处于面心的F形成正八面体空隙,Co处于体心,K处于顶点。
①每个晶胞中由K和F共同形成的正四面体空隙有
②晶胞的另一种表示中,Co处于各顶角位置,则K处于
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】CH3COOH中C原子轨道杂化类型为________________ 。
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】钛及其化合物作用重要,尤其氧化钛、四氧化钛、钛酸钡等应用更广。回答下列问题:
(1)基态钛原子的价层电子排布式为_______ 。
(2) 二氧化钛是世界上最白的物质,1g二氧化钛可以把450多平方厘米的面积涂得雪白,是调制白油漆的最好颜料。基态Ti4+中核外电子占据的原子轨道数为_____ 个。
(3)四氯化钛是种有趣的液体,在潮湿空气中水解生成白色的二氧化钛水凝胶,军事上利用四氯化钛的这种“怪脾气”制造烟雾剂。写出四氯化钛水解的化学方程式_______ 。
(4)Ti(BH4)3是一种储氢材料,可由TiCl4和LiBH4反应制得。LiBH4由Li+和BH 构成,其中BH
构成,其中BH 的空间构型为
的空间构型为_______ ;B原子的杂化轨道类型为_______ 。
(5)Mn、Fe均为第四周期过渡金属元素,两元素的部分电离能数据如下:
锰元素位于第_______ 周期_______ 族_______ 区;比较两元素的I2、I3可知,气态Mn2+再失去1个电子比气态Fe2+再失去1个电子难,对此你的解释是_______ 。
(1)基态钛原子的价层电子排布式为
(2) 二氧化钛是世界上最白的物质,1g二氧化钛可以把450多平方厘米的面积涂得雪白,是调制白油漆的最好颜料。基态Ti4+中核外电子占据的原子轨道数为
(3)四氯化钛是种有趣的液体,在潮湿空气中水解生成白色的二氧化钛水凝胶,军事上利用四氯化钛的这种“怪脾气”制造烟雾剂。写出四氯化钛水解的化学方程式
(4)Ti(BH4)3是一种储氢材料,可由TiCl4和LiBH4反应制得。LiBH4由Li+和BH
 构成,其中BH
构成,其中BH 的空间构型为
的空间构型为(5)Mn、Fe均为第四周期过渡金属元素,两元素的部分电离能数据如下:
元素 | Mn | Fe | |
电离能/kJ∙mol−1 | I1 | 717 | 759 |
I2 | 1509 | 1561 | |
I3 | 3248 | 2957 | |
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】已知C、N、O、H是元素周期表中前10号元素,它们的原子半径依次减小,H能分别与C、N、O形成电子总数相等的分子 、
、 、
、 。
。
(1)在 、
、 、
、 分子中,C、N、O三原子都采取
分子中,C、N、O三原子都采取___________ 杂化。
(2) 是
是___________ 分子(填“极性”或“非极性”)。
(3) 是一种易液化的气体,请简述其易液化的原因:
是一种易液化的气体,请简述其易液化的原因:___________ 。
(4) 分子的VSEPR模型的空间构型为
分子的VSEPR模型的空间构型为___________ ; 分子的空间构型为
分子的空间构型为___________ 。
 、
、 、
、 。
。(1)在
 、
、 、
、 分子中,C、N、O三原子都采取
分子中,C、N、O三原子都采取(2)
 是
是(3)
 是一种易液化的气体,请简述其易液化的原因:
是一种易液化的气体,请简述其易液化的原因:(4)
 分子的VSEPR模型的空间构型为
分子的VSEPR模型的空间构型为 分子的空间构型为
分子的空间构型为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】Cu2+在水中呈现蓝色是因为形成了水合铜离子,其化学式为__ ;提供空轨道接受孤电子对的粒子是__ ;水分子与铜离子间结合的化学键名称为__ 。
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】O元素可与 素形成低价态氧化物
素形成低价态氧化物 。
。
(1) 立方晶胞结构如图所示,则
立方晶胞结构如图所示,则 的配位数为___________。
的配位数为___________。
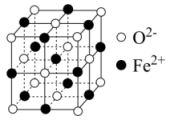
(2)与 紧邻的所有
紧邻的所有 构成的几何构型为___________。
构成的几何构型为___________。
(3) 晶胞边长为
晶胞边长为 ,则该晶体的密度为
,则该晶体的密度为___________  。(用含a、
。(用含a、 的代数式表示,
的代数式表示, 代表阿伏伽德罗常数的值)
代表阿伏伽德罗常数的值)
 素形成低价态氧化物
素形成低价态氧化物 。
。(1)
 立方晶胞结构如图所示,则
立方晶胞结构如图所示,则 的配位数为___________。
的配位数为___________。
| A.3 | B.4 | C.5 | D.6 |
 紧邻的所有
紧邻的所有 构成的几何构型为___________。
构成的几何构型为___________。| A.平面三角形 | B.正四面体 | C.立方体 | D.正八面体 |
 晶胞边长为
晶胞边长为 ,则该晶体的密度为
,则该晶体的密度为 。(用含a、
。(用含a、 的代数式表示,
的代数式表示, 代表阿伏伽德罗常数的值)
代表阿伏伽德罗常数的值)
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】铬与氮能形成多种化合物,其中氮化铬(CrN)具有高的硬度和良好的耐磨性,是一种很受重视的耐磨涂层。将低碳铬铁在真空加热炉于1150℃氮化得到粗氮化铬铁,再经硫酸处理,除去铁杂质。经过滤、水洗、干燥,即得氮化铬。也可由氨和卤化铬反应制得。
(1)基态Cr核外电子排布式为_______ 。
(2) 中心原子轨道的杂化类型为
中心原子轨道的杂化类型为_______ 。
(3)元素As与N同族。预测As的氢化物分子的立体结构为_______ ,其沸点比 的
的_______ (填“高”或“低”),其判断理由_______ 。
(4)三价铬离子能形成多种配位化合物。 中提供电子对形成配位键的原子是
中提供电子对形成配位键的原子是_______ ,中心离子的配位数为_______ 。
(1)基态Cr核外电子排布式为
(2)
 中心原子轨道的杂化类型为
中心原子轨道的杂化类型为(3)元素As与N同族。预测As的氢化物分子的立体结构为
 的
的(4)三价铬离子能形成多种配位化合物。
 中提供电子对形成配位键的原子是
中提供电子对形成配位键的原子是
您最近一年使用:0次



