回答下列问题:
(1)某温度下,向含有AgCl固体的AgCl饱和溶液中加入少量稀盐酸,则AgCl的溶解度______ (填增大,减小或不变,下同),Ksp______ ,c(Ag+)______ 。
(2)现有25℃0.1mol/L的氨水。请回答以下问题:
①若向氨水中加入氯化铵固体,此时溶液中NH3•H2O电离程度_______ (填“增大”、“减小”或“不变”);此时溶液中水的离子积约等于_______ 。
②若向氨水中加入稀硫酸,使其恰好中和,写出离子方程式:______ 所得溶液的pH______ 7(填“>”“=”或“<”),用离子方程式表示其原因:______ 。
(1)某温度下,向含有AgCl固体的AgCl饱和溶液中加入少量稀盐酸,则AgCl的溶解度
(2)现有25℃0.1mol/L的氨水。请回答以下问题:
①若向氨水中加入氯化铵固体,此时溶液中NH3•H2O电离程度
②若向氨水中加入稀硫酸,使其恰好中和,写出离子方程式:
更新时间:2024-04-10 15:31:25
|
相似题推荐
填空题
|
较易
(0.85)
名校
【推荐1】(1)内因:___________________ 。
(2)外因:①浓度:_________________________
②温度:________________________________________
③酸碱度
(3)酸式盐溶液的酸碱性:强酸酸式盐显__________ ,原因是_____________________________ 。多元弱酸酸式盐溶液的酸碱性取决于_____________________________________ ,例如NaHCO3溶液显碱性,原因是_________________ ,_______________________________ (离子方程式和文字说明);
NaHSO3溶液显酸性的原因是________________ ,_____________________ (离子方程式和文字说明)。
(4)用↑、↓、→、←表示,填表:CH3COONa溶液改变下列条件,填写变化情况:CH3COO-+H2O CH3COOH+OH-
CH3COOH+OH-_______________
(2)外因:①浓度:
②温度:
③酸碱度
(3)酸式盐溶液的酸碱性:强酸酸式盐显
NaHSO3溶液显酸性的原因是
(4)用↑、↓、→、←表示,填表:CH3COONa溶液改变下列条件,填写变化情况:CH3COO-+H2O
 CH3COOH+OH-
CH3COOH+OH-| 改变条件 | 平衡移动 | c(CH3COO-) | c(OH-) | 水解 |
| 加入CH3COONa | ||||
| 通入HCl | ||||
| 升温 | ||||
| 加水 | ||||
| 加NaOH | ||||
| 加HAc | ||||
| 加NH4Cl |
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】一定温度下,将一定质量的冰醋酸加水稀释过程中,溶液的导电能力变化如图所示。

(1)a、b、c主点溶液的pH大小关系:_______ 。
(2)a、b、c三点CH3COOH的电离程度大小关系:_______ 。

(1)a、b、c主点溶液的pH大小关系:
(2)a、b、c三点CH3COOH的电离程度大小关系:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】(1)写出醋酸的电离方程式:_____________________________________ ;
(2)写出醋酸电离平衡常数表达式:_______________ ;
(3)向0.1mol/L 醋酸溶液中加入水,电离平衡向_______ 移动 (填“左”或“右”) ;n(CH3COOH)_______ ; c(CH3COOH)/c(H+)_______ (填“增大”、“减小”或“不变”);
(4)500mL 0.1mol/L 醋酸溶液a和500mL 0.1mol/L 盐酸溶液b与足量Zn粉反应,初始速率a___ b;生成H2的量a____ b;完全中和这两种酸,消耗NaOH的量a___ b(填“<”、“>”或“=”)。
(2)写出醋酸电离平衡常数表达式:
(3)向0.1mol/L 醋酸溶液中加入水,电离平衡向
(4)500mL 0.1mol/L 醋酸溶液a和500mL 0.1mol/L 盐酸溶液b与足量Zn粉反应,初始速率a
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】用沉淀法除杂能否将杂质离子全部通过沉淀除去________ ?
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
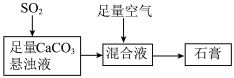
【推荐2】下图表示的是生产石膏的简单流程,请用平衡移动原理解释向CaCO3悬浊液中通入SO2发生反应的原因______ 。

您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】回答下列问题
(1)写出过量Mg(OH)2固体放入水中溶解形成饱和溶液时的溶解平衡表达式________________________________ ,向有Mg(OH)2沉淀的溶液中加入过量浓NH4Cl,溶液变澄清,相关反应的化学方程式为____________________________ ,已知室温时饱和的Mg(OH)2溶液的pH=10,则Mg(OH)2的溶度积为___________ 。
(2)明矾是KAl(SO4)2·12H2O,其溶液中离子浓度由大到小的顺序______________________ ;向明矾溶液中逐渐滴入Ba(OH)2 溶液至SO 离子恰好沉淀完全时,溶液的显
离子恰好沉淀完全时,溶液的显_______ 性(填酸、碱、中),离子反应的总方程式:_________________________________________________ 。
(3)为配制SbCl3溶液,取少量SbCl3固体,加2mL~3mL水溶解,此时却会产生白色沉淀Sb2O3,写出此时反应的化学方程式为:___________________________ ,故在配制SbCl3溶液时应加少量____________ 。
(1)写出过量Mg(OH)2固体放入水中溶解形成饱和溶液时的溶解平衡表达式
(2)明矾是KAl(SO4)2·12H2O,其溶液中离子浓度由大到小的顺序
 离子恰好沉淀完全时,溶液的显
离子恰好沉淀完全时,溶液的显(3)为配制SbCl3溶液,取少量SbCl3固体,加2mL~3mL水溶解,此时却会产生白色沉淀Sb2O3,写出此时反应的化学方程式为:
您最近一年使用:0次



