人类的农业生产离不开氮肥,几乎所有的氮肥都以氨为原料,某化学兴趣小组利用图1装置制备氨气,图2装置探究其相关性质。
(1)图1装置中生成 的化学方程式为
的化学方程式为_____ 。
(2)检验圆底烧瓶中已收集满氨气的方法是_____ 。
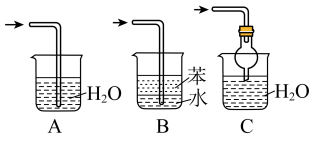
Ⅱ.探究氨气与氧化铜的反应(如图2)验证氨气的性质及部分反应产物:
(3)无水硫酸铜的作用是_____ ;有同学认为需要在无水硫酸铜的后面再接一个装有 固体的球形干燥管,这样做的目的是
固体的球形干燥管,这样做的目的是_____ 。
(4)该实验缺少尾气吸收装置。如图中能用来吸收尾气的装置是_____ (填字母)。 粉末变红,b中无水硫酸铜变蓝,并收集到一种单质气体。则该反应的化学方程式为
粉末变红,b中无水硫酸铜变蓝,并收集到一种单质气体。则该反应的化学方程式为_____ ,证明氨气具有_____ (填“氧化”或“还原”)性。
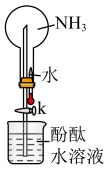
(6)①如图是进行氨气喷泉实验的装置,氨气使烧杯中溶液由无色变为红色,其原因是(用方程式表示)_____ 。
②在上图的烧瓶中充满干燥气体,胶头滴管及烧杯中分别盛有液体。下列组合中不可能形成喷泉的是_____ 。 和
和 B.
B. 和氢氧化钠溶液 C.
和氢氧化钠溶液 C. 和饱和食盐水 D.
和饱和食盐水 D. 和烧碱溶液
和烧碱溶液
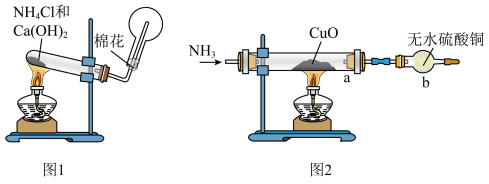
(1)图1装置中生成
 的化学方程式为
的化学方程式为(2)检验圆底烧瓶中已收集满氨气的方法是
Ⅱ.探究氨气与氧化铜的反应(如图2)验证氨气的性质及部分反应产物:
(3)无水硫酸铜的作用是
 固体的球形干燥管,这样做的目的是
固体的球形干燥管,这样做的目的是(4)该实验缺少尾气吸收装置。如图中能用来吸收尾气的装置是
 粉末变红,b中无水硫酸铜变蓝,并收集到一种单质气体。则该反应的化学方程式为
粉末变红,b中无水硫酸铜变蓝,并收集到一种单质气体。则该反应的化学方程式为(6)①如图是进行氨气喷泉实验的装置,氨气使烧杯中溶液由无色变为红色,其原因是(用方程式表示)
②在上图的烧瓶中充满干燥气体,胶头滴管及烧杯中分别盛有液体。下列组合中不可能形成喷泉的是
 和
和 B.
B. 和氢氧化钠溶液 C.
和氢氧化钠溶液 C. 和饱和食盐水 D.
和饱和食盐水 D. 和烧碱溶液
和烧碱溶液
更新时间:2024-04-12 14:12:11
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
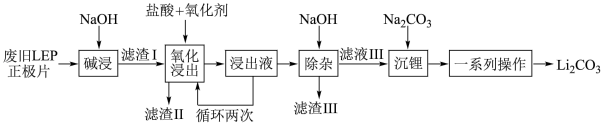
【推荐1】随着新能源汽车销量的猛增,动力电池退役高峰将至,磷酸铁锂(LEP)是目前使用最多的动力电池材料,因此回收磷酸铁锂具有重要意义。一种从废旧磷酸铁锂正极片( LiFePO4、导电石墨、铝箔)中回收锂的工艺流程如下:
ii.Li2CO3在水中的溶解度随温度升高而降低,但煮沸时与水发生反应。
回答下列问题:
(1)LiFePO4中用途最广用量最大的金属元素在周期表中的位置是___________ 。
(2)“氧化浸出”时,保持其他条件不变,不同氧化剂对锂的浸出实验结果如下表,实际生产中氧化剂选用H2O2,不选用NaClO3的原因是___________ 。在“氧化浸出”时,适当的升温可加快反应速率,但般不采取高温法, 其原因是___________ 。“氧化浸出”时生成了难溶的FePO4,该反应的离子方程式为。___________ 。
(3)“浸出液”循环两次的目的是___________ 。
(4)“滤渣II”经纯化可得FePO4,流程中生成的Li2CO3、FePO4在高温条件下与H2C2O4煅烧可得LiFePO4,实现再生利用,其化学方程式为___________ 。
(5)“一系列操作”具体包括___________ 、洗涤、干燥。
ii.Li2CO3在水中的溶解度随温度升高而降低,但煮沸时与水发生反应。
回答下列问题:
(1)LiFePO4中用途最广用量最大的金属元素在周期表中的位置是
(2)“氧化浸出”时,保持其他条件不变,不同氧化剂对锂的浸出实验结果如下表,实际生产中氧化剂选用H2O2,不选用NaClO3的原因是
| 序号 | 锂含量/% | 氧化剂 | pH | 浸出液Li 浓度/(g·L-1) | 浸出渣中Li 含量/% |
| 1 | 3.7 | H2O2 | 3.5 | 9.02 | 0.10 |
| 2 | 3.7 | NaClO3 | 3.5 | 9.05 | 0.08 |
| 3 | 3.7 | O2 | 3.5 | 7.05 | 0.93 |
| 4 | 3.7 | NaClO | 3.5 | 8.24 | 0.43 |
(4)“滤渣II”经纯化可得FePO4,流程中生成的Li2CO3、FePO4在高温条件下与H2C2O4煅烧可得LiFePO4,实现再生利用,其化学方程式为
(5)“一系列操作”具体包括
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】蚀刻铜制线路板的蚀刻液种类很多:酸性蚀刻液,如 蚀刻溶液、H2O2-盐酸及CuCl2-盐酸
蚀刻溶液、H2O2-盐酸及CuCl2-盐酸 碱性蚀刻液,如
碱性蚀刻液,如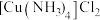 溶液等。回答下列问题:
溶液等。回答下列问题:
(1)写出下列蚀刻液蚀刻铜的离子方程式。
①FeCl3溶液:_______ 。
②H2O2-盐酸:_______ 。
③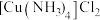 溶液:
溶液:_______  生成
生成 。
。
(2)利用废 蚀刻液
蚀刻液 含
含 、
、 及
及 制备碱性蚀刻液
制备碱性蚀刻液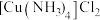 溶液和
溶液和 的主要步骤包括:用
的主要步骤包括:用 氧化废蚀刻液,通入氨气
氧化废蚀刻液,通入氨气 ,固液分离,用盐酸溶解沉淀和
,固液分离,用盐酸溶解沉淀和 的制备。下列实验装置不能达到实验目的的是
的制备。下列实验装置不能达到实验目的的是_______  填字母
填字母 。
。
A.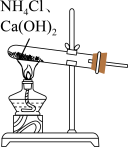 制备
制备
B. 制备
制备 并沉铁
并沉铁
C. 分离
分离 溶液和
溶液和 沉淀
沉淀
D. 将
将 溶液蒸干制备
溶液蒸干制备
(3)常用水合肼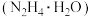 还原法回收CuCl2-盐酸蚀刻液得到单质铜,先用氢氧化钠溶液中和其中酸并将溶液调至强碱性,然后加入水合肼得纳米铜,该氧化还原反应中氧化剂与还原剂的物质的量之比为
还原法回收CuCl2-盐酸蚀刻液得到单质铜,先用氢氧化钠溶液中和其中酸并将溶液调至强碱性,然后加入水合肼得纳米铜,该氧化还原反应中氧化剂与还原剂的物质的量之比为_______ 。
(4)文献报道一种回收蚀刻废液中铜并制取胆矾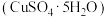 的主要工艺流程如下:
的主要工艺流程如下:

已知: 易与酸反应。
易与酸反应。
 在混合器中,
在混合器中, 的离子方程式为
的离子方程式为_______ 。
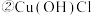 溶于硫酸的离子方程式为
溶于硫酸的离子方程式为_______ 。
 蚀刻溶液、H2O2-盐酸及CuCl2-盐酸
蚀刻溶液、H2O2-盐酸及CuCl2-盐酸 碱性蚀刻液,如
碱性蚀刻液,如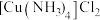 溶液等。回答下列问题:
溶液等。回答下列问题:(1)写出下列蚀刻液蚀刻铜的离子方程式。
①FeCl3溶液:
②H2O2-盐酸:
③
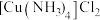 溶液:
溶液: 生成
生成 。
。(2)利用废
 蚀刻液
蚀刻液 含
含 、
、 及
及 制备碱性蚀刻液
制备碱性蚀刻液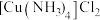 溶液和
溶液和 的主要步骤包括:用
的主要步骤包括:用 氧化废蚀刻液,通入氨气
氧化废蚀刻液,通入氨气 ,固液分离,用盐酸溶解沉淀和
,固液分离,用盐酸溶解沉淀和 的制备。下列实验装置不能达到实验目的的是
的制备。下列实验装置不能达到实验目的的是 填字母
填字母 。
。A.
 制备
制备
B.
 制备
制备 并沉铁
并沉铁C.
 分离
分离 溶液和
溶液和 沉淀
沉淀D.
 将
将 溶液蒸干制备
溶液蒸干制备
(3)常用水合肼
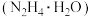 还原法回收CuCl2-盐酸蚀刻液得到单质铜,先用氢氧化钠溶液中和其中酸并将溶液调至强碱性,然后加入水合肼得纳米铜,该氧化还原反应中氧化剂与还原剂的物质的量之比为
还原法回收CuCl2-盐酸蚀刻液得到单质铜,先用氢氧化钠溶液中和其中酸并将溶液调至强碱性,然后加入水合肼得纳米铜,该氧化还原反应中氧化剂与还原剂的物质的量之比为(4)文献报道一种回收蚀刻废液中铜并制取胆矾
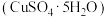 的主要工艺流程如下:
的主要工艺流程如下:
已知:
 易与酸反应。
易与酸反应。 在混合器中,
在混合器中, 的离子方程式为
的离子方程式为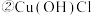 溶于硫酸的离子方程式为
溶于硫酸的离子方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】碘酸钾 是重要的分析试剂。某研究小组设计实验制备
是重要的分析试剂。某研究小组设计实验制备 ,并进行相关探究。
,并进行相关探究。
Ⅰ.制备
制备 实验装置如下:
实验装置如下:

查阅资料: 为白色固体,能溶于水,难溶于四氯化碳:
为白色固体,能溶于水,难溶于四氯化碳: 溶于水,难溶于乙醇。
溶于水,难溶于乙醇。
(1)橡胶管a的作用是_______ 。
(2)装置B中 的作用是
的作用是_______ 。
(3)装置B中制取 的化学反应方程式为
的化学反应方程式为_______ 。
Ⅱ.制备
(4)从B中分离出 溶液,加入KOH溶液中和制得
溶液,加入KOH溶液中和制得 溶液,再加入适量
溶液,再加入适量_______ ,经搅拌、静置、过滤等操作,得到白色固体粗产品,提纯得 晶体。
晶体。
Ⅲ.实验探究
为探究 溶液和
溶液和 溶液的反应,该小组设计了实验A:向足量的酸性
溶液的反应,该小组设计了实验A:向足量的酸性 溶液滴入数滴淀粉溶液,再加入
溶液滴入数滴淀粉溶液,再加入 溶液,开始时无明显现象,一段时间(T秒)后,溶液变蓝。
溶液,开始时无明显现象,一段时间(T秒)后,溶液变蓝。
(5)溶液变蓝,表明 体现了
体现了_______ 性。
(6)针对T秒前溶液未变蓝,小组做出如下猜想:
①猜想a:T秒前未生成 ,是由于反应的活化能
,是由于反应的活化能_______ (填“大”或“小”),反应速率_______ (填“快”或“慢”)导致的。
②猜想b:T秒前生成了 ,但由于存在
,但由于存在 ,
, 迅速被消耗,反应为
迅速被消耗,反应为_______ (用离子方程式表示)。
(7)请设计实验B,证明猜想b成立:向实验A的蓝色溶液中加入_______ ,蓝色迅速消失,后再次变蓝。
 是重要的分析试剂。某研究小组设计实验制备
是重要的分析试剂。某研究小组设计实验制备 ,并进行相关探究。
,并进行相关探究。Ⅰ.制备

制备
 实验装置如下:
实验装置如下:
查阅资料:
 为白色固体,能溶于水,难溶于四氯化碳:
为白色固体,能溶于水,难溶于四氯化碳: 溶于水,难溶于乙醇。
溶于水,难溶于乙醇。(1)橡胶管a的作用是
(2)装置B中
 的作用是
的作用是(3)装置B中制取
 的化学反应方程式为
的化学反应方程式为Ⅱ.制备

(4)从B中分离出
 溶液,加入KOH溶液中和制得
溶液,加入KOH溶液中和制得 溶液,再加入适量
溶液,再加入适量 晶体。
晶体。Ⅲ.实验探究
为探究
 溶液和
溶液和 溶液的反应,该小组设计了实验A:向足量的酸性
溶液的反应,该小组设计了实验A:向足量的酸性 溶液滴入数滴淀粉溶液,再加入
溶液滴入数滴淀粉溶液,再加入 溶液,开始时无明显现象,一段时间(T秒)后,溶液变蓝。
溶液,开始时无明显现象,一段时间(T秒)后,溶液变蓝。(5)溶液变蓝,表明
 体现了
体现了(6)针对T秒前溶液未变蓝,小组做出如下猜想:
①猜想a:T秒前未生成
 ,是由于反应的活化能
,是由于反应的活化能②猜想b:T秒前生成了
 ,但由于存在
,但由于存在 ,
, 迅速被消耗,反应为
迅速被消耗,反应为(7)请设计实验B,证明猜想b成立:向实验A的蓝色溶液中加入
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】化学实验小组同学利用以下实验装置制备氨气,并探究氨气的性质(部分仪器已略去)。请回答:___________ 。
(2)用装置B收集氨气时,应选择氨气的进气口是___________ (选填“a”或“b”);然后打开装置B中的止水夹c,观察到烧瓶内产生了___________ (现象)。
(3)干燥氨气常用___________ ,检验氨气的常用方法是___________ 。
(4)为防止环境污染,以下装置(盛放的液体均为水)可用于吸收多余氨气的是___________ (填序号)。 的原理是(写离子方程式)
的原理是(写离子方程式)___________ 。

(2)用装置B收集氨气时,应选择氨气的进气口是
(3)干燥氨气常用
(4)为防止环境污染,以下装置(盛放的液体均为水)可用于吸收多余氨气的是

 的原理是(写离子方程式)
的原理是(写离子方程式)
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】氨气在工农业生产中有重要应用。某化学小组同学利用以下装置制备氨气,并探究氨气的性质(夹持仪器略)。
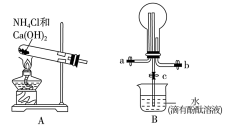

(1)实验室用装置A制备氨气的化学方程式为___________ 。
(2)用装置B收集氨气时,进气口是___________ (填“a”或“b”)。打开装置B中的活塞c,烧瓶内产生了红色喷泉,则说明氨具有的性质是___________ 。
(3)向C中 固体上滴几滴浓氨水。迅速盖上玻璃片,浓盐酸液滴附近会出现白烟,发生反应的化学方程式为
固体上滴几滴浓氨水。迅速盖上玻璃片,浓盐酸液滴附近会出现白烟,发生反应的化学方程式为___________ ,检验氨气的方法是___________ 。 液滴中先出现灰绿色沉淀,过一段时间后变成红褐色,发生的反应有
液滴中先出现灰绿色沉淀,过一段时间后变成红褐色,发生的反应有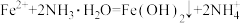 和
和___________ 。


(1)实验室用装置A制备氨气的化学方程式为
(2)用装置B收集氨气时,进气口是
(3)向C中
 固体上滴几滴浓氨水。迅速盖上玻璃片,浓盐酸液滴附近会出现白烟,发生反应的化学方程式为
固体上滴几滴浓氨水。迅速盖上玻璃片,浓盐酸液滴附近会出现白烟,发生反应的化学方程式为 液滴中先出现灰绿色沉淀,过一段时间后变成红褐色,发生的反应有
液滴中先出现灰绿色沉淀,过一段时间后变成红褐色,发生的反应有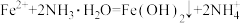 和
和
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
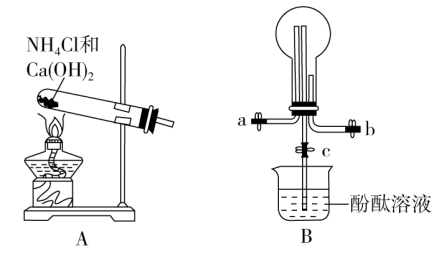
【推荐3】某化学实验小组同学利用以下实验装置制备氨气,并探究氨气的性质(部分仪器已略去)。请回答:
(1)实验室制备氨气的化学方程式为_______ 。
(2)实验中要干燥氨气,应选用的干燥剂是_______。
(3)用装置B收集氨气时,应选择氨气的进气口是_______ (选填“a”或“b”),并说明选择的理由是_______ 。
(4)打开装置B中的止水夹c,若观察到烧瓶内产生了红色喷泉,则说明氨气具有的性质是_______ ,_______ 。
(5)为防止环境污染,以下装置(盛放的液体均为水)可用于吸收多余氨气的是_______ (填序号)。
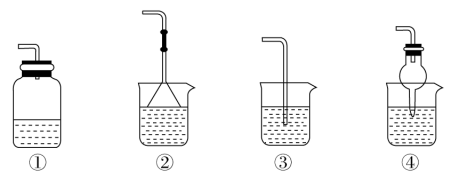

(1)实验室制备氨气的化学方程式为
(2)实验中要干燥氨气,应选用的干燥剂是_______。
| A.浓硫酸 | B.无水氯化钙 | C.五氧化二磷 | D.碱石灰 |
(4)打开装置B中的止水夹c,若观察到烧瓶内产生了红色喷泉,则说明氨气具有的性质是
(5)为防止环境污染,以下装置(盛放的液体均为水)可用于吸收多余氨气的是

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
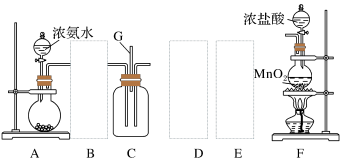
【推荐1】某课外活动小组用如图所示的实验装置探究氯气与氨气之间的反应。其中A、F为氨气和氯气的发生装置,C为纯净、干燥的氯气与氨气反应的装置。
请回答下列问题:
(1)装置F中发生反应的离子方程式是______________ 。
(2)装置A中的烧瓶内固体可选用_______________ (选填以下选项的代号)。
A.碱石灰 B.浓硫酸 C.生石灰 D.五氧化二磷 E.烧碱
(3)虚线框内应添加必要的除杂装置,请从图的备选装置中选择,并将编号填入下列空格:B___ D____ E_____
Ⅰ.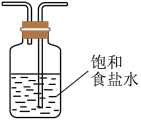 Ⅱ.
Ⅱ.  Ⅲ.
Ⅲ. 
(4)氯气和氨气在常温下混合就能发生反应生成氯化铵和氮气,该反应的化学方程式为:_______ ;装置C内出现浓厚的白烟(该物质化学式为_______ ),并在容器内壁凝结,请设计一个实验方案鉴定该固体就是:______ 。
(5)若从装置C和G处逸出的尾气中含有N2和少量C12,应如何处理____________ 。

请回答下列问题:
(1)装置F中发生反应的离子方程式是
(2)装置A中的烧瓶内固体可选用
A.碱石灰 B.浓硫酸 C.生石灰 D.五氧化二磷 E.烧碱
(3)虚线框内应添加必要的除杂装置,请从图的备选装置中选择,并将编号填入下列空格:B
Ⅰ.
 Ⅱ.
Ⅱ.  Ⅲ.
Ⅲ. 
(4)氯气和氨气在常温下混合就能发生反应生成氯化铵和氮气,该反应的化学方程式为:
(5)若从装置C和G处逸出的尾气中含有N2和少量C12,应如何处理
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】实验室常用氯化铵与氢氧化钙的固体混合加热制取氨气,实验室提供的有关装置见下表:
完成下列填空:
(1)从上图中选择实验室制取氨气的发生装置_____ (选填编号)、收集装置____ (选填编号)。
(2)用注射器收集50 mL纯净的氨气,然后再抽取10 mL滴有酚酞试液的蒸馏水,并用橡皮塞封闭针头。充分振荡后注射器内_______ (选填“有”“无”)气体剩余,液体呈___ 色,用化学方程式解释液体颜色变化的原因_____________________ 。
(3)工业合成氨的简易流程如下:
通过循环Ⅰ可利用的气态物质是_______
a.催化剂 b.只有N2 c.只有H2 d.N2和H2
(4)将 CO2通入到氨化的饱和食盐水中制备NaHCO3固体,反应的化学方程式__________ 。
(5)NH3、PH3、AsH3三种氢化物热稳定性由强到弱的顺序是_______ ,理由是___________ 。
(6)工业上用氨水吸收SO2尾气,最终得到化肥 (NH4)2SO4。(NH4)2SO4溶液呈_______ 性,用离子方程式解释原因__________________ ;该溶液中存在多种守恒,用离子浓度表示其中一种守恒关系________________________ 。
气体发生装置 |
a |
b |
c |
气体收集装置 |
|
|
|
完成下列填空:
(1)从上图中选择实验室制取氨气的发生装置
(2)用注射器收集50 mL纯净的氨气,然后再抽取10 mL滴有酚酞试液的蒸馏水,并用橡皮塞封闭针头。充分振荡后注射器内
(3)工业合成氨的简易流程如下:
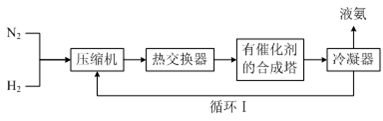
通过循环Ⅰ可利用的气态物质是
a.催化剂 b.只有N2 c.只有H2 d.N2和H2
(4)将 CO2通入到氨化的饱和食盐水中制备NaHCO3固体,反应的化学方程式
(5)NH3、PH3、AsH3三种氢化物热稳定性由强到弱的顺序是
(6)工业上用氨水吸收SO2尾气,最终得到化肥 (NH4)2SO4。(NH4)2SO4溶液呈
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】(1)如图,若烧瓶是干燥的。当烧瓶口向上时,由A口导入气体,可收集下列中的____________ (填序号,下同)气体。若烧瓶充满水,可收集下列中的________ 气体。

① NO ②NH3 ③SO2 ④ NO2
(2)若烧瓶中事先已集满一瓶氨气,并将烧瓶口向下放置,由______ 口导入气体可收集NO气体,其原因是 ____________________________________________ 。
(3)实验室通常制备氨气的化学方程式______________________________ 。

① NO ②NH3 ③SO2 ④ NO2
(2)若烧瓶中事先已集满一瓶氨气,并将烧瓶口向下放置,由
(3)实验室通常制备氨气的化学方程式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】实验小组对氯气的制备和性质进行探究。
Ⅰ.实验室制备和收集氯气的常用装置如下图。

(1)盛放 的仪器名称是
的仪器名称是___________ 。
(2)利用该装置制备氯气的化学方程式为___________ 。
(3)在实验过程中饱和食盐水的作用是___________ 。
(4)实验装置接口的连接顺序为e→___________ →___________ →___________ →___________ →i→h→g→f。
Ⅱ.为探究NaCl对 溶解性的影响,进行如下实验。
溶解性的影响,进行如下实验。
已知 在常温下溶解度为
在常温下溶解度为 。测定不同浓度NaCl溶液中的
。测定不同浓度NaCl溶液中的 溶解度,结果如下:
溶解度,结果如下:
(5)根据实验数据,NaCl溶液浓度大于___________  时,增加NaCl溶液浓度对
时,增加NaCl溶液浓度对 溶解度变化无明显影响。
溶解度变化无明显影响。
(6)为进一步探究食盐水中哪些微粒能降低 溶解度,取三支试管,分别加入一定浓度NaCl溶液、HCl溶液和
溶解度,取三支试管,分别加入一定浓度NaCl溶液、HCl溶液和 溶液,通入足量
溶液,通入足量 后,测定
后,测定 溶解度。
溶解度。
①
___________ ,
___________ ,
___________ 。
②对比实验1和实验2可以得到的结论是___________ 。
③设置实验3的目的是___________ 。
④实验结论:食盐水中能够降低 溶解度的微粒有
溶解度的微粒有___________ 。
(7)有同学认为 会减弱NaCl溶液降低
会减弱NaCl溶液降低 溶解度的效果。为验证该同学的猜想是否正确,可设计实验方案为
溶解度的效果。为验证该同学的猜想是否正确,可设计实验方案为___________ 。
Ⅰ.实验室制备和收集氯气的常用装置如下图。

(1)盛放
 的仪器名称是
的仪器名称是(2)利用该装置制备氯气的化学方程式为
(3)在实验过程中饱和食盐水的作用是
(4)实验装置接口的连接顺序为e→
Ⅱ.为探究NaCl对
 溶解性的影响,进行如下实验。
溶解性的影响,进行如下实验。已知
 在常温下溶解度为
在常温下溶解度为 。测定不同浓度NaCl溶液中的
。测定不同浓度NaCl溶液中的 溶解度,结果如下:
溶解度,结果如下: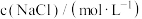 | 0.50 | 1.00 | 3.00 | 4.00 | 5.00 |
 溶解度 溶解度 | 0.0658 | 0.0580 | 0.0416 | 0.0360 | 0.0360 |
 时,增加NaCl溶液浓度对
时,增加NaCl溶液浓度对 溶解度变化无明显影响。
溶解度变化无明显影响。(6)为进一步探究食盐水中哪些微粒能降低
 溶解度,取三支试管,分别加入一定浓度NaCl溶液、HCl溶液和
溶解度,取三支试管,分别加入一定浓度NaCl溶液、HCl溶液和 溶液,通入足量
溶液,通入足量 后,测定
后,测定 溶解度。
溶解度。| 实验编号 | 1 | 2 | 3 |
| 实验装置 |  | 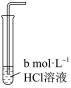 |  |
 溶解度 溶解度 | 0.0580 | 0.0665 | 0.0800 |


②对比实验1和实验2可以得到的结论是
③设置实验3的目的是
④实验结论:食盐水中能够降低
 溶解度的微粒有
溶解度的微粒有(7)有同学认为
 会减弱NaCl溶液降低
会减弱NaCl溶液降低 溶解度的效果。为验证该同学的猜想是否正确,可设计实验方案为
溶解度的效果。为验证该同学的猜想是否正确,可设计实验方案为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】如图是某化学兴趣小组设计的乙醇催化氧化的实验装置(图中加热仪器、铁架台、试管夹均未画出)。图中A处为无水乙醇(沸点78℃),B处为绕成螺旋状的细铜丝或银丝,C处为无水CuSO4粉末,D处为碱石灰,F处为新制的碱性Cu(OH)2悬浊液。

(1)为使A中乙醇平稳地汽化成乙醇蒸气,常采用的方法是_____________ 。
(2)若E中的固体为纯净物,则E的化学式是_____________ 。
(3)写出B处发生反应的化学方程式_____________
(4)加热F处的混合液的实验现象是_____________ 。

(1)为使A中乙醇平稳地汽化成乙醇蒸气,常采用的方法是
(2)若E中的固体为纯净物,则E的化学式是
(3)写出B处发生反应的化学方程式
(4)加热F处的混合液的实验现象是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】把小块木炭在酒精灯上烧至红热,迅速投入热的浓硝酸中,发生剧烈反应,同时有大量红棕色气体产生,液面上木炭迅速燃烧发出光亮。
(1)写出红热木炭被热的浓硝酸氧化为CO2的化学方程式____________________ 。
(2)木炭与浓硝酸反应过程中还伴随着浓硝酸的分解,除了产生氧气外,也产生红棕色气体。相同条件下该分解反应产生的氧气与红棕色气体的体积之比为____________________ 。
(3)某研究性学习小组的同学对“木炭在液面上迅速燃烧发出光亮”的原因做出3个猜想:
A.甲同学认为空气中O2支持木炭燃烧
B.乙同学认为浓硝酸分解产生的O2支持木炭燃烧
C.丙同学认为反应产生的NO2支持木炭燃烧
①根据木炭在空气中燃烧的现象,甲同学的猜想明显不合理,理由是____________________ 。
②理论分析乙同学的猜想也不正确,原因是________________________________________ 。
③要证实丙同学的猜想,还需补充的实验方案是____________________________________ 。(请写出实验操作、现象和结论)。
(1)写出红热木炭被热的浓硝酸氧化为CO2的化学方程式
(2)木炭与浓硝酸反应过程中还伴随着浓硝酸的分解,除了产生氧气外,也产生红棕色气体。相同条件下该分解反应产生的氧气与红棕色气体的体积之比为
(3)某研究性学习小组的同学对“木炭在液面上迅速燃烧发出光亮”的原因做出3个猜想:
A.甲同学认为空气中O2支持木炭燃烧
B.乙同学认为浓硝酸分解产生的O2支持木炭燃烧
C.丙同学认为反应产生的NO2支持木炭燃烧
①根据木炭在空气中燃烧的现象,甲同学的猜想明显不合理,理由是
②理论分析乙同学的猜想也不正确,原因是
③要证实丙同学的猜想,还需补充的实验方案是
您最近一年使用:0次





 水
水

