已知SO2是硫元素重要的化合物,是大气主要污染物之一,是形成酸雨的主要原因,是以还原性为主的酸性氧化物,具有漂白性。某研究性学习小组设计实验,制取SO2并探究SO2的某些性质。制取SO2反应的化学方程式为Na2SO3+H2SO4=Na2SO4+SO2↑+H2O,产生的气体通入下图所示装置。
(2)B、D装置的作用是 。
(3)S可以形成多种化合物,下列说法正确的是 。
(4)关于酸雨和大气污染的说法正确的是 。
(5)下列说法中正确的是 。
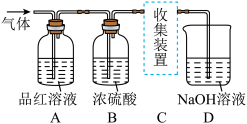
| A.品红溶液褪色,说明SO2气体具有氧化性 | B.品红溶液褪色,说明SO2气体具有漂白性 |
| C.品红溶液褪色,说明SO2气体具有还原性 | D.SO2气体有毒,不可以做食品添加剂 |
(2)B、D装置的作用是 。
| A.B装置中浓硫酸做干燥剂,干燥SO2气体 |
| B.D装置吸收尾气,防止污染空气 |
C.D装置中的离子方程式是SO2+2OH-=SO +H2O +H2O |
| D.B装置中的浓硫酸可以用碱石灰替代 |
(3)S可以形成多种化合物,下列说法正确的是 。
| A.H2S是弱酸 | B.浓硫酸有强氧化性 |
| C.硫化钠具有还原性 | D.硫酸中的硫元素是+4价 |
(4)关于酸雨和大气污染的说法正确的是 。
| A.空气中SO2的含量达到一定量会产生酸雨,此酸雨的成分是H2SO4 |
| B.空气中NO2的含量达到一定量会产生酸雨,此酸雨的成分是HNO3 |
| C.酸雨会使水体酸化,水体中的动植物死亡,对森林无影响 |
| D.雨水的pH=5.6就会形成酸雨 |
(5)下列说法中正确的是 。
| A.烧结黏土制陶瓷不涉及化学反应 |
| B.玻璃、水泥的生产都要用石灰石做原料 |
| C.晶体硅熔点高、硬度大,因此可用于制作半导体材料 |
| D.玻璃、餐桌上的瓷盘和水晶项链的主要成分都是硅酸盐 |
更新时间:2024-04-15 09:26:06
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
【推荐1】SO2常用作漂白剂和防腐剂,但它也是造成大气污染的主要有害气体之一、火力发电厂使用的煤炭是常用的含硫燃料,燃煤烟气需净化后再排放。回答下列问题:
(1)某实验小组探究SO2的化学性质,装置如图所示(abc均为浸有相应试液的棉花,夹持与加热装置略)。

制备SO2的反应化学方程式为___________ 。
(2)a处的实验现象为___________ ;b处观察到颜色褪去,SO2体现的化学性质为___________ 。
(3)在工业生产上规定空气中二氧化硫允许排放量不超过0.02mgL1,该小组为测定火力发电厂附近空气中的二氧化硫的含量,进行如下实验:
取标准状况下的空气1L(含氮气、氧气、二氧化碳、二氧化硫等),缓慢通入适量I2的淀粉溶液中,则溶液由蓝色变为无色,向所得溶液中加入过量的氯化钡溶液,产生白色沉淀,一系列操作后,称得其质量为0.233g。其中,“一系列操作”为___________ ;空气中SO2是否超过允许排放量:___________ (填“是”或“否”)。
(4)该小组查阅资料知:钙基固硫是燃煤烟气脱硫的常用方法,内容是先用CaCO3浆状物吸收SO2,再鼓入空气,得到硫酸钙用于制备石膏,变废为宝。此过程发生反应的化学方程式依次为___________ ,___________ 。
(1)某实验小组探究SO2的化学性质,装置如图所示(abc均为浸有相应试液的棉花,夹持与加热装置略)。

制备SO2的反应化学方程式为
(2)a处的实验现象为
(3)在工业生产上规定空气中二氧化硫允许排放量不超过0.02mgL1,该小组为测定火力发电厂附近空气中的二氧化硫的含量,进行如下实验:
取标准状况下的空气1L(含氮气、氧气、二氧化碳、二氧化硫等),缓慢通入适量I2的淀粉溶液中,则溶液由蓝色变为无色,向所得溶液中加入过量的氯化钡溶液,产生白色沉淀,一系列操作后,称得其质量为0.233g。其中,“一系列操作”为
(4)该小组查阅资料知:钙基固硫是燃煤烟气脱硫的常用方法,内容是先用CaCO3浆状物吸收SO2,再鼓入空气,得到硫酸钙用于制备石膏,变废为宝。此过程发生反应的化学方程式依次为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】某同学用如图所示装置探究SO2的性质及其有关实验。

(1)实验室用亚硫酸钠固体和一定浓度的硫酸反应制备SO2 气体,写出该反应的化学方程式________
(2)分别将SO2 气体通入下列C 溶液中,请回答下列问题:
①少量SO2通入紫色石蕊试液,现象是_______ ,继续通入过量SO2 气体,现象是____________
②SO2 通入紫色KMnO4溶液,现象是_______ ,其反应的离子方程式为__________
③过量SO2慢慢地通入澄清石灰水中,现象是_________
④若C为双氧水,则通入SO2 后,请大胆判断所得溶液是_______ (填溶质的化学式),若该同学制备的SO2 气体中混有CO2 气体,产生杂质的原因可能是亚硫酸钠固体中混有______________

(1)实验室用亚硫酸钠固体和一定浓度的硫酸反应制备SO2 气体,写出该反应的化学方程式
(2)分别将SO2 气体通入下列C 溶液中,请回答下列问题:
①少量SO2通入紫色石蕊试液,现象是
②SO2 通入紫色KMnO4溶液,现象是
③过量SO2慢慢地通入澄清石灰水中,现象是
④若C为双氧水,则通入SO2 后,请大胆判断所得溶液是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】请回答下列问题:
(1)某化学兴趣小组用除去表面氧化物的铁钉(碳素钢)与一定量浓硫酸共热,对产生的气体的成分进行探究。为检验气体成分,设计了下图所示装置:

①A装置产生的气体的成分除SO2、CO2之外,可能还有
②为检验并吸收SO2,装置B中加入的试剂为
③装置C中品红溶液的作用是
④证明气体中含有CO2的实验现象
⑤装置H的作用为
(2)兴趣小组同学设计下图装置验证二氧化硫的化学性质。
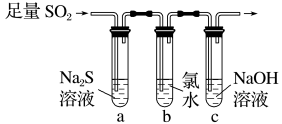
a装置可验证SO2具有
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】(1)断裂 化学键所需要的能量如表所示,腓(
化学键所需要的能量如表所示,腓( )的有关化学反应的能量变化如图所示。
)的有关化学反应的能量变化如图所示。
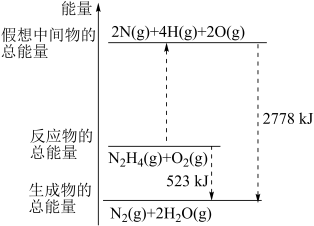
回答下列问题:
①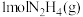 与
与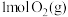 反应生成
反应生成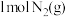 和
和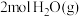 放出的能量为
放出的能量为____ kJ。
②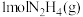 与
与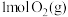 断键吸收的能量为
断键吸收的能量为____ kJ。
③a=____ 。
④当有 生成时,放出的能量
生成时,放出的能量_____ (填“>”“<”或“=”)523kJ。
(2)某镇有座硫酸厂,设备简陋,技术陈旧,该厂每天排放大量含 的废气和含
的废气和含 的酸性废水。当地的其他工厂和居民均用煤炭作燃料。只要下雨就下酸雨,对该镇环境造成极大破坏。
的酸性废水。当地的其他工厂和居民均用煤炭作燃料。只要下雨就下酸雨,对该镇环境造成极大破坏。
①分析该镇下酸雨的原因:_______ ;
②举一例说明酸雨对环境造成的危害:_______ ;
③该镇某中学环保小组提出了治理酸雨的下列措施,你认为其中不妥的是_______ ;
④可用熟石灰来处理硫酸厂排出的酸性废水,处理原理的化学方程式是_______ ;
⑤浓硫酸弄到手上后直接用大量水洗,然后涂上碳酸氢钠。这样的处理方法正确吗?_______ (填“正确”或“不正确”),理由是_______ 。
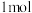 化学键所需要的能量如表所示,腓(
化学键所需要的能量如表所示,腓( )的有关化学反应的能量变化如图所示。
)的有关化学反应的能量变化如图所示。
| 化学键 |  | 氧氧键 |  |  |
能量/( ) ) |  | 498 | 946 | 391 |
①
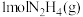 与
与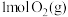 反应生成
反应生成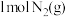 和
和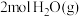 放出的能量为
放出的能量为②
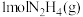 与
与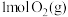 断键吸收的能量为
断键吸收的能量为③a=
④当有
 生成时,放出的能量
生成时,放出的能量(2)某镇有座硫酸厂,设备简陋,技术陈旧,该厂每天排放大量含
 的废气和含
的废气和含 的酸性废水。当地的其他工厂和居民均用煤炭作燃料。只要下雨就下酸雨,对该镇环境造成极大破坏。
的酸性废水。当地的其他工厂和居民均用煤炭作燃料。只要下雨就下酸雨,对该镇环境造成极大破坏。①分析该镇下酸雨的原因:
②举一例说明酸雨对环境造成的危害:
③该镇某中学环保小组提出了治理酸雨的下列措施,你认为其中不妥的是
| A.将硫酸厂搬离该镇 |
| B.建议环保部门限令整改 |
C.将硫酸厂排出的废气中的 处理后排放 处理后排放 |
| D.工厂和居民改用较清洁的燃料 |
⑤浓硫酸弄到手上后直接用大量水洗,然后涂上碳酸氢钠。这样的处理方法正确吗?
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】X、Y、Z、W是中学化学中常见的四种气体。已知:X、Y、Z三种气体都能对大气造成污染,在工业上都可以用碱液吸收;X是化石燃料燃烧的产物之一,是形成酸雨的物质;Y是一种单质,它的水溶液具有漂白作用;Z是硝酸工业的汽车尾气中的有害物质之一,能与水反应;W气体的水溶液滴入酚酞变红色。
请回答下列问题:
(1)X、Y两种气体按物质的量之比1:1在水溶液中能发生反应,化学方程式为_________________________________________________________ ;
(2)科学家发现,Z在催化剂条件下能与W反应,反应产物中的单质应是(填化学式)_____________________ ;该反应是氧化还原反应,则其中的氧化剂是(填化学式)__________________________________________________ 。
(3)在Z与水的反应中,氧化剂与还原剂的物质的量之比为__________________________________
请回答下列问题:
(1)X、Y两种气体按物质的量之比1:1在水溶液中能发生反应,化学方程式为
(2)科学家发现,Z在催化剂条件下能与W反应,反应产物中的单质应是(填化学式)
(3)在Z与水的反应中,氧化剂与还原剂的物质的量之比为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】中科院官微曾给出灰霾中细颗粒物的成因,部分分析如下图所示。

(1)根据如图1所示信息可以看出,所列的气体污染物并非由机动车行驶造成的是______ 。 汽车发动机废气稀燃控制系统的主要工作原理如图2所示,写出稀燃过程中NO发生的主要反应的方程式:________ 。
(2)农业活动排出的氨可能是来自施用的化肥分解,也可能是化肥施用不当导致的。比如某些氮肥与碱性肥料混合施用会释放出氨,请用离子方程式解释该现象:_________ 。
(3)经过研究发现我国的霾呈中性,其主要原因如下方程式,A的化学式是_______ 。2NH3(气)+SO2(气) +2NO2(气)→2NH (溶液)+ A(溶液) +2HONO(气)
(溶液)+ A(溶液) +2HONO(气)
(4)煤燃烧时排放的烟气含有SO2和NOx,采用NaClO2溶液作为吸收剂可同时对烟气进行脱硫、脱硝。将含有SO2和NO,的烟气通入盛有NaClO2溶液的反应器中,反应一.段时间后,测得溶液中离子浓度的有关数据如下表所示(其他极微量离子忽略不计):
①NO和NaClO2溶液反应的离子方程式是________________ 。
②表中y=___________________ 。
(5)工业生产硝酸也有可能产生NOx污染。请写出硝酸生产中的第一步:氨的催化氧化的化学方程式为_______ 。 若用氮气制氨的产率为90%,用氨生产硝酸时氨的催化氧化和氮氧化物转化为硝酸的损耗依次为5%、3%,则1000 mol氮气可制得________ (计算结果保留整数)mol硝酸。

(1)根据如图1所示信息可以看出,所列的气体污染物并非由机动车行驶造成的是
(2)农业活动排出的氨可能是来自施用的化肥分解,也可能是化肥施用不当导致的。比如某些氮肥与碱性肥料混合施用会释放出氨,请用离子方程式解释该现象:
(3)经过研究发现我国的霾呈中性,其主要原因如下方程式,A的化学式是
 (溶液)+ A(溶液) +2HONO(气)
(溶液)+ A(溶液) +2HONO(气)(4)煤燃烧时排放的烟气含有SO2和NOx,采用NaClO2溶液作为吸收剂可同时对烟气进行脱硫、脱硝。将含有SO2和NO,的烟气通入盛有NaClO2溶液的反应器中,反应一.段时间后,测得溶液中离子浓度的有关数据如下表所示(其他极微量离子忽略不计):
| 离子 | Na+ | SO | NO | H+ | C1- |
| 浓度/(mol/L) | 5.5×10-3 | 8.5×10-4 | y | 2.8×10-4 | 3.5×10-3 |
①NO和NaClO2溶液反应的离子方程式是
②表中y=
(5)工业生产硝酸也有可能产生NOx污染。请写出硝酸生产中的第一步:氨的催化氧化的化学方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】化学与经济和社会的发展关系密切,在人类文明的可持续发展中发挥着日益重要的作用。
(1)物质的结构决定性质,物质的制取和用途等是性质的体现。
①下列试剂需保存在棕色试剂瓶中的是_______ (填字母)。
a.新制氯水 b.浓硫酸 c.NaOH溶液
②工业冶铁和生产普通玻璃都要用到的原料是_______ (填名称)。
③已知:5KI+KIO3+6HCl=6KCI+3Cl2↑+3H2O,向加碘食盐(含KIO3)中加入盐酸酸化的KI和淀粉溶液,出现的现象是_______
④生产中可用浓氨水检验氯气管道是否漏气。若管道漏气,用浓氨水检查时会产生白烟。已知该反应有氮气生成,且为置换反应,反应的化学方程式为_______ 。
(2)化学是环境科学的基础,能够保护生态环境实现人与自然和谐相处。
①下列环境问题与所对应的物质不相关的是_______ (填字母)。
a.酸雨—二氧化碳 b.臭氧层破坏—氟氯烃 c.光化学污染—氮氧化物
②漂白粉可用于生活用水的杀菌消毒,漂白粉的有效成分是_______ (填化学式)。
③工业上采用向燃煤中加入石灰石,以减少燃煤过程中SO2的排放,发生的化学反应为:CaCO3+O2+SO2—CaSO4+CO2请配平化学方程式,并标出电子转移的方向和数目___ 。
(3)工业上可通过高温分解FeSO4的方法制备Fe2O3,同时生成SO2和SO3两种气体。为检验这两种硫的氧化物,可将产生的气体通入如图所示的装置中进行实验。

①写出FeSO4,高温分解的化学反应方程式:_________
②实验中可以观察到现象为_______
③实验中NaOH溶液的作用_______
(1)物质的结构决定性质,物质的制取和用途等是性质的体现。
①下列试剂需保存在棕色试剂瓶中的是
a.新制氯水 b.浓硫酸 c.NaOH溶液
②工业冶铁和生产普通玻璃都要用到的原料是
③已知:5KI+KIO3+6HCl=6KCI+3Cl2↑+3H2O,向加碘食盐(含KIO3)中加入盐酸酸化的KI和淀粉溶液,出现的现象是
④生产中可用浓氨水检验氯气管道是否漏气。若管道漏气,用浓氨水检查时会产生白烟。已知该反应有氮气生成,且为置换反应,反应的化学方程式为
(2)化学是环境科学的基础,能够保护生态环境实现人与自然和谐相处。
①下列环境问题与所对应的物质不相关的是
a.酸雨—二氧化碳 b.臭氧层破坏—氟氯烃 c.光化学污染—氮氧化物
②漂白粉可用于生活用水的杀菌消毒,漂白粉的有效成分是
③工业上采用向燃煤中加入石灰石,以减少燃煤过程中SO2的排放,发生的化学反应为:CaCO3+O2+SO2—CaSO4+CO2请配平化学方程式,并标出电子转移的方向和数目
(3)工业上可通过高温分解FeSO4的方法制备Fe2O3,同时生成SO2和SO3两种气体。为检验这两种硫的氧化物,可将产生的气体通入如图所示的装置中进行实验。

①写出FeSO4,高温分解的化学反应方程式:
②实验中可以观察到现象为
③实验中NaOH溶液的作用
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】某化学兴趣小组利用铜跟浓硫酸反应,探究SO2的部分性质,实验装置如图所示。

(1)装置A中发生反应的化学方程式为________ 。
(2)装置B的作用是贮存多余的气体,B中广口瓶内应盛放的液体是________ (填序号);
①水 ②饱和的NaHSO3溶液 ③NaOH溶液 ④酸性KMnO4
(3)装置D中试管口塞一团棉花,棉花中应浸有一种液体,其作用是________ 。
(4)装置C和D中产生的现象相同,但原因却不同。D中是由于SO2具有________ 性,而C中则是由于________ 。
(5)SO2气体为无色气体,有强烈刺激性气味,是大气主要污染物之一,具有一定的还原性,探究SO2气体还原Fe3+、I2可以使用的药品和装置如图所示:

在上述装置中通入过量的SO2,为了验证A中SO2与Fe3+发生了氧化还原反应,取A中的溶液,分成两份,并设计了如下实验:
方案①:向第一份试液中加入少量酸性KMnO4溶液,紫红色褪去。
方案②:向第二份试液中加入KSCN溶液,不变红,再加入新制的氯水,溶液变红。
上述方案不合理的是_______ (填①或②),不合理的原因是________ 。在上述装置中能表明SO2的还原性强于I2的现象是________ 。

(1)装置A中发生反应的化学方程式为
(2)装置B的作用是贮存多余的气体,B中广口瓶内应盛放的液体是
①水 ②饱和的NaHSO3溶液 ③NaOH溶液 ④酸性KMnO4
(3)装置D中试管口塞一团棉花,棉花中应浸有一种液体,其作用是
(4)装置C和D中产生的现象相同,但原因却不同。D中是由于SO2具有
(5)SO2气体为无色气体,有强烈刺激性气味,是大气主要污染物之一,具有一定的还原性,探究SO2气体还原Fe3+、I2可以使用的药品和装置如图所示:

在上述装置中通入过量的SO2,为了验证A中SO2与Fe3+发生了氧化还原反应,取A中的溶液,分成两份,并设计了如下实验:
方案①:向第一份试液中加入少量酸性KMnO4溶液,紫红色褪去。
方案②:向第二份试液中加入KSCN溶液,不变红,再加入新制的氯水,溶液变红。
上述方案不合理的是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】硫酸是重要的化工原料,可用于生产化肥、农药、炸药、染料和盐类等。工业生产硫酸的流程图如图:

(1)工业上常以黄铁矿(FeS2)为原料,通过高温煅烧的方式来制备SO2,将KSCN滴入其另一种产物(红棕色氧化物)与盐酸充分反应后的溶液中,变成血红色,写出该反应的化学方程式______ 。
(2)为提高吸收塔中的工作效率,可采用的方式是______ 。
(3)硫酸工业的尾气中含有少量SO2,若直接排放会污染空气,并导致硫酸型酸雨。尾气处理可用NaOH溶液吸收,写出相关反应的离子方程式_____ 。
(4)为验证SO2的某些性质,设计了下列装置图。试回答:

①E中的实验现象为______ ,证明SO2具有______ 性。
②通入SO2后,F中的酸性KMnO4溶液褪色,证明SO2具有______ 性,写出相关的离子方程式_____ 。
③H中使用倒置漏斗的目的是______ 。

(1)工业上常以黄铁矿(FeS2)为原料,通过高温煅烧的方式来制备SO2,将KSCN滴入其另一种产物(红棕色氧化物)与盐酸充分反应后的溶液中,变成血红色,写出该反应的化学方程式
(2)为提高吸收塔中的工作效率,可采用的方式是
(3)硫酸工业的尾气中含有少量SO2,若直接排放会污染空气,并导致硫酸型酸雨。尾气处理可用NaOH溶液吸收,写出相关反应的离子方程式
(4)为验证SO2的某些性质,设计了下列装置图。试回答:

①E中的实验现象为
②通入SO2后,F中的酸性KMnO4溶液褪色,证明SO2具有
③H中使用倒置漏斗的目的是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】非金属材料及其化合物是无机非金属材料的主要成分,硅是无机非金属材料的主角,硅的氧化物和硅酸盐约占地壳质量的90%以上。
I.
(1)计算机芯片和太阳能电池的主要成分是_______ (填化学式,下同);光导纤维的主要成分是_______ ;工艺师常用氢氟酸来雕刻玻璃,其原理为_______ (填化学方程式)。
II.高纯度单晶硅的制备方法:
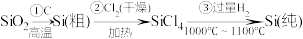
某同学从资料中查知:SiCl4的熔点为-70℃,沸点为57.6℃,在潮湿的空气中与水发生反应而变质。该同学设计了如图装置制取纯硅(装置中的热源及夹持装置均已略去)。
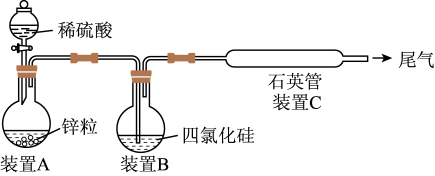
(2)已知:步骤①生成的另一产物为CO,写出步骤①中反应的化学方程式:_______ 。
(3)装置A中发生反应的离子方程式为_______ 。
(4)已知:SiCl4在潮湿的空气中能与水发生反应生成氯化氢。为防止空气污染,含有SiCl4的尾气可通入盛有_______ (填试剂名称)的烧杯中。
(5)同学甲认为用该装置进行实验,可能会导致实验失败,为保证制备纯硅实验的成功,你认为该装置应进行的改进措施是_______ 。
I.
(1)计算机芯片和太阳能电池的主要成分是
II.高纯度单晶硅的制备方法:
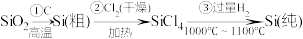
某同学从资料中查知:SiCl4的熔点为-70℃,沸点为57.6℃,在潮湿的空气中与水发生反应而变质。该同学设计了如图装置制取纯硅(装置中的热源及夹持装置均已略去)。

(2)已知:步骤①生成的另一产物为CO,写出步骤①中反应的化学方程式:
(3)装置A中发生反应的离子方程式为
(4)已知:SiCl4在潮湿的空气中能与水发生反应生成氯化氢。为防止空气污染,含有SiCl4的尾气可通入盛有
(5)同学甲认为用该装置进行实验,可能会导致实验失败,为保证制备纯硅实验的成功,你认为该装置应进行的改进措施是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】非金属材料及其化合物是无机非金属材料的主要成分,硅是无机非金属材料的主角,硅的氧化物和硅酸盐约占地壳质量的90%以上。
I.
(1)计算机芯片和太阳能电池的主要成分是___________ (填化学式,下同);光导纤维的主要成分是___________ ;工艺师常用氢氟酸来雕刻玻璃,其原理为___________ (填化学方程式)。
Ⅱ.高纯度单晶硅的制备方法:

某同学从资料中查知:SiCl4的熔点为-70℃,沸点为57.6℃,在潮湿的空气中与水发生反应而变质。该同学设计了如图装置制取纯硅(装置中的热源及夹持装置均已略去)。
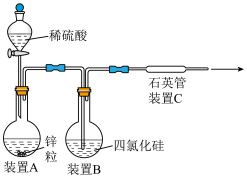
(2)已知:步骤①生成的另一产物为CO,写出步骤①中反应的化学方程式:___________ 。
(3)装置A中发生反应的离子方程式为___________ 。
(4)已知:SiCl4在潮湿的空气中能与水发生反应生成氯化氢。为防止空气污染,含有SiCl4的尾气可通入盛有___________ (填试剂名称)的烧杯中。
(5)同学甲认为用该装置进行实验,可能会导致实验失败,为保证制备纯硅实验的成功,你认为该装置应进行的改进措施是___________ 。
I.
(1)计算机芯片和太阳能电池的主要成分是
Ⅱ.高纯度单晶硅的制备方法:

某同学从资料中查知:SiCl4的熔点为-70℃,沸点为57.6℃,在潮湿的空气中与水发生反应而变质。该同学设计了如图装置制取纯硅(装置中的热源及夹持装置均已略去)。

(2)已知:步骤①生成的另一产物为CO,写出步骤①中反应的化学方程式:
(3)装置A中发生反应的离子方程式为
(4)已知:SiCl4在潮湿的空气中能与水发生反应生成氯化氢。为防止空气污染,含有SiCl4的尾气可通入盛有
(5)同学甲认为用该装置进行实验,可能会导致实验失败,为保证制备纯硅实验的成功,你认为该装置应进行的改进措施是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】生产芯片的半导体材料有硅、锗、砷化镓等,应用比较广泛的是硅。硅可由石英砂(主要成分是二氧化硅)制得,制备高纯硅的主要工艺流程如图所示:

资料:①SiHCl3能与H2O剧烈反应,在空气中易自燃;②粗SiHCl3 (沸点33.0℃)中含有少量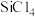 (沸点57.6℃)和HCl(沸点-84.7℃)
(沸点57.6℃)和HCl(沸点-84.7℃)
(1)流程①焦炭体现了___________ (填“氧化性”或“还原性”)。
(2)流程③提纯SiHCl3的操作是___________ 。
(3)流程④的化学反应为置换反应,写出其化学方程式:___________ 。
流程④制备高纯硅的装置如图(热源及夹持装置略去):

(4)若要从下列玻璃仪器中选择部分来组装A处的气体发生装置,需要的是___________ (填选项编号):
a. 分液漏斗 b.烧瓶 c.酒精灯 d.大试管 e.漏斗 f.烧杯 g.导管
装置B中的试剂是___________ (填试剂名称);装置C中的烧瓶需要加热,其目的是___________ 。
(5)反应一段时间后,装置D中观察到的现象是___________ 。
(6)为保证制备高纯硅实验的成功,操作的关键是检查实验装置的气密性,控制好反应温度以及___________ ,该流程中能够循环利用的物质是___________ 。

资料:①SiHCl3能与H2O剧烈反应,在空气中易自燃;②粗SiHCl3 (沸点33.0℃)中含有少量
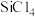 (沸点57.6℃)和HCl(沸点-84.7℃)
(沸点57.6℃)和HCl(沸点-84.7℃)(1)流程①焦炭体现了
(2)流程③提纯SiHCl3的操作是
(3)流程④的化学反应为置换反应,写出其化学方程式:
流程④制备高纯硅的装置如图(热源及夹持装置略去):

(4)若要从下列玻璃仪器中选择部分来组装A处的气体发生装置,需要的是
a. 分液漏斗 b.烧瓶 c.酒精灯 d.大试管 e.漏斗 f.烧杯 g.导管
装置B中的试剂是
(5)反应一段时间后,装置D中观察到的现象是
(6)为保证制备高纯硅实验的成功,操作的关键是检查实验装置的气密性,控制好反应温度以及
您最近一年使用:0次



