在化工生产中,硫资源应用广泛,利用含硫物质之间的转化有利于实现硫资源的综合利用。下图为硫及其化合物的“价—类”二维图。
(1)从硫元素化合价变化的角度分析,图中既有氧化性又有还原性的物质有______ ,______ (填化学式,任写两种)。
(2)写出Cu和Z的浓溶液发生反应的化学方程式__________________ 。
(3)将Y通入品红溶液中,可观察到的现象是______________________________ 。
(4)工业上处理废气时,通过步骤IⅡ和步骤w将Y转化为CaSO4再利用。
①实现步骤I的转化所加试剂是______ (写出一种即可)。
②实现步骤Ⅱ的转化可选择______ 试剂(填序号)。
A.O2 B.KI C.H2O2 D.Na2S
(5)欲制备Na2S2O3,从氧化还原角度分析,合理的是______(填序号)。
(6)将H2S与SO2混合,可生成淡黄色固体。该反应的氧化剂与还原剂的物质的量之比为______ 。
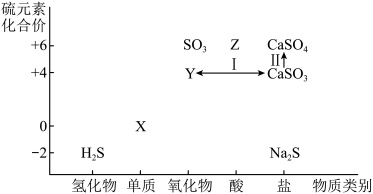
(1)从硫元素化合价变化的角度分析,图中既有氧化性又有还原性的物质有
(2)写出Cu和Z的浓溶液发生反应的化学方程式
(3)将Y通入品红溶液中,可观察到的现象是
(4)工业上处理废气时,通过步骤IⅡ和步骤w将Y转化为CaSO4再利用。
①实现步骤I的转化所加试剂是
②实现步骤Ⅱ的转化可选择
A.O2 B.KI C.H2O2 D.Na2S
(5)欲制备Na2S2O3,从氧化还原角度分析,合理的是______(填序号)。
| A.Na2S+S | B.Na2SO3+S | C.Na2SO3+Na2SO4 | D.SO2+Na2SO4 |
(6)将H2S与SO2混合,可生成淡黄色固体。该反应的氧化剂与还原剂的物质的量之比为
更新时间:2024/04/16 15:24:41
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】铅蓄电池在生活中应用广泛,其电极上发生的总反应为:Pb + PbO2 + 2H2SO4 ====2PbSO4+ 2H2O。该反应中,被还原的物质是______ (填化学式),作为还原剂的物质是______ (填化学式);若反应中消耗了2 mol Pb,则生成______ mol PbSO4。
您最近半年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】向Cu和CuO组成的混合物中,加入90mL5.0mol·L1稀硝酸溶液,恰好使混合物完全溶解,同时收集到标准状况下NO 2.24L。请回答以下问题:
(1)写出Cu与稀硝酸反应的离子方程式_____________________________________ ;
(2)原混合物中铜的物质的量为________ mol,氧化铜的物质的量为______ mol;
(3)若要将生成的NO气体完全转化为硝酸,需通氧气______ L(标准状况下)。
(1)写出Cu与稀硝酸反应的离子方程式
(2)原混合物中铜的物质的量为
(3)若要将生成的NO气体完全转化为硝酸,需通氧气
您最近半年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】完成下列反应对应的离子方程式
(1)用NaOH溶液除去Mg粉中的Al杂质_________ 。
(2)用醋酸浸泡除水垢(CaCO3)_________ 。
(3)洁厕灵和漂白液不宜混用_________ 。
(4)泡沫灭火器反应原理_________ 。
(5)SO2使酸性KMnO4溶液褪色________ 。
(6)实验室使用稀硫酸和H2O2溶解铜片_________ 。
(7)碱性条件下,Al粉将NO3-还原成为无污染的气体__________ 。
(1)用NaOH溶液除去Mg粉中的Al杂质
(2)用醋酸浸泡除水垢(CaCO3)
(3)洁厕灵和漂白液不宜混用
(4)泡沫灭火器反应原理
(5)SO2使酸性KMnO4溶液褪色
(6)实验室使用稀硫酸和H2O2溶解铜片
(7)碱性条件下,Al粉将NO3-还原成为无污染的气体
您最近半年使用:0次
填空题
|
较易
(0.85)
【推荐2】(1)配平下列反应的化学方程式(假定NO与NO2的物质的量之比为1:3)
 Fe +
Fe +  HNO3 =
HNO3 = Fe(NO3)3 +
Fe(NO3)3 + NO↑+
NO↑+ NO2↑+
NO2↑+ H2O
H2O
_______
(2)此反应配平时可以有多组系数,其原因是_______
(3)请简述检验溶液中的金属阳离子的实验操作及现象_______
 Fe +
Fe +  HNO3 =
HNO3 = Fe(NO3)3 +
Fe(NO3)3 + NO↑+
NO↑+ NO2↑+
NO2↑+ H2O
H2O(2)此反应配平时可以有多组系数,其原因是
(3)请简述检验溶液中的金属阳离子的实验操作及现象
您最近半年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】氧化还原反应是中学化学的重要内容。回答下列问题:
(1)野外,一般用铝热反应来焊接铁轨,其化学方程式为Fe2O3+2Al Al2O3+2Fe。该反应中氧化剂为
Al2O3+2Fe。该反应中氧化剂为___________ ,还原产物为___________ 。
(2)用单线桥法表示电子转移的方向和数目:___________  ,被氧化和被还原的氯原子的个数之比为
,被氧化和被还原的氯原子的个数之比为_______ 。
(3)高铁酸钠是一种新型的绿色消毒剂,主要用于饮用水处理,其中一种制备方法如下,配平该离子方程式:___________  。
。
(1)野外,一般用铝热反应来焊接铁轨,其化学方程式为Fe2O3+2Al
 Al2O3+2Fe。该反应中氧化剂为
Al2O3+2Fe。该反应中氧化剂为(2)用单线桥法表示电子转移的方向和数目:
 ,被氧化和被还原的氯原子的个数之比为
,被氧化和被还原的氯原子的个数之比为(3)高铁酸钠是一种新型的绿色消毒剂,主要用于饮用水处理,其中一种制备方法如下,配平该离子方程式:
 。
。
您最近半年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】有A、B、C三种常见的金属单质,A在空气中燃烧生成淡黄色固体;B也能在空气中剧烈燃烧,发出耀眼的白光;C在一定条件下与水蒸气反应生成H2和一种黑色固体。根据以上信息回答下列问题:
(1)写出化学式A______ B_____ C_____
(2)写化学方程式
①A在空气中燃烧_______________________________
②C与水蒸气反应____________________________________
③A与水反应________________________________________
(1)写出化学式A
(2)写化学方程式
①A在空气中燃烧
②C与水蒸气反应
③A与水反应
您最近半年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】有三种金属单质A、B、C,其中A的焰色反应为黄色,B、C是常见金属。三种金属单质A、B、C能与气体甲、乙、丙及物质D、E、F、G、H之间发生如下转化关系(图中有些反应的产物和反应的条件没有标出)。请根据以上信息回答下列问题:
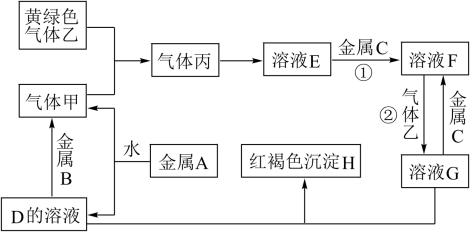
(1)写出下列物质的化学式:乙_________ 、H__________ ;
(2)写出反应②的离子方程式______________________ ;
(3)写出金属A与水反应的离子方程式___________________________ ;
(4)写出金属B与D的溶液反应的离子方程式____________________ ;
(5)F与D溶液反应后的产物在空气中转化为H的化学方程式___________ ;现象为_________________ 。

(1)写出下列物质的化学式:乙
(2)写出反应②的离子方程式
(3)写出金属A与水反应的离子方程式
(4)写出金属B与D的溶液反应的离子方程式
(5)F与D溶液反应后的产物在空气中转化为H的化学方程式
您最近半年使用:0次
填空题
|
较易
(0.85)
【推荐1】人们认识和应用物质常从两方面入手,一是从物质的类别认识该物质可能跟哪些物质发生反应;二是从物质所含元素的化合价分析该物质是否具有氧化性或还原性。如图所示是硫元素的各个价态与物质类别的对应关系:

(1)写出指定物质的化学式:
A____________ ,B____________ 。
(2)D转化为硫酸是酸雨形成的重要过程之一,写出其反应的化学方程式________________________ 。
(3)若C是铜盐,试写出由H2SO4→C的化学方程式__________________________ 。
(4)为进一步减少SO2的污染并变废为宝,我国正在探索在一定条件下用CO还原SO2得到单质硫的方法来除去SO2。写出该反应的化学方程式___________________________________ 。

(1)写出指定物质的化学式:
A
(2)D转化为硫酸是酸雨形成的重要过程之一,写出其反应的化学方程式
(3)若C是铜盐,试写出由H2SO4→C的化学方程式
(4)为进一步减少SO2的污染并变废为宝,我国正在探索在一定条件下用CO还原SO2得到单质硫的方法来除去SO2。写出该反应的化学方程式
您最近半年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】物质的类别和核心元素的化合价是研究物质性质的两个重要角度。下图所示是硫及其部分化合物的“价类二维图”,根据图示回答下列问题:

(1)足量B通入品红溶液的现象是___________ ;体现了B的___________ 性。足量B通入溴水中的现象是___________ ;体现了B的___________ 性。
(2)从物质的性质分析,B不可用___________ 进行干燥(填标号)。
A.浓硫酸 B.碱石灰 C.P2O5固体
(3)硫代硫酸钠(Na2S2O3)俗称海波。从类别的角度分析,其属于___________(填标号)。
(4)欲制备Na2S2O3,从氧化还原角度分析,下列选项中合理的是___________(填序号)。
(5)D的浓溶液与铜单质在加热条件下可以发生化学反应,反应的化学方程式为___________ 。

(1)足量B通入品红溶液的现象是
(2)从物质的性质分析,B不可用
A.浓硫酸 B.碱石灰 C.P2O5固体
(3)硫代硫酸钠(Na2S2O3)俗称海波。从类别的角度分析,其属于___________(填标号)。
| A.盐 | B.碱 | C.酸 | D.氧化物 |
| A.Na2S+S | B.Na2SO3+S |
| C.Na2SO3+Na2SO4 | D.SO2+Na2SO4 |
您最近半年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】“价一类”二维图是研究物质性质的重要工具,如图是硫元素的“价一类”二维图。
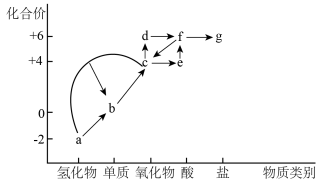
回答下列问题:
(1)c→d反应的化学方程式为________ 。
(2)反应a+c→b中,氧化产物与还原产物的物质的量之比为______ 。
(3)溶液e久置于空气中会生成f,该过程溶液的酸性______ (填“增强”或“减弱”)。
(4)可用铜与f的浓溶液反应制备c,反应的化学方程式为____________ 。
(5)将c通入到酸性KMnO₄溶液中,溶液颜色逐渐变浅,该反应中c表现出______ (填“还原”或“漂白”)性。
(6)实验室产生c排放到大气中会引起酸雨,应用_____ 溶液吸收,发生的反应方程式为__ 。

回答下列问题:
(1)c→d反应的化学方程式为
(2)反应a+c→b中,氧化产物与还原产物的物质的量之比为
(3)溶液e久置于空气中会生成f,该过程溶液的酸性
(4)可用铜与f的浓溶液反应制备c,反应的化学方程式为
(5)将c通入到酸性KMnO₄溶液中,溶液颜色逐渐变浅,该反应中c表现出
(6)实验室产生c排放到大气中会引起酸雨,应用
您最近半年使用:0次

 和浓盐酸在一定温度下反应会生成黄绿色的易爆物二氧化氯,其化学方程式为:
和浓盐酸在一定温度下反应会生成黄绿色的易爆物二氧化氯,其化学方程式为: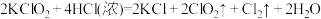 。(
。( 中氯元素的化合价为
中氯元素的化合价为 价)
价) 的
的

