 和浓盐酸在一定温度下反应会生成黄绿色的易爆物二氧化氯,其化学方程式为:
和浓盐酸在一定温度下反应会生成黄绿色的易爆物二氧化氯,其化学方程式为: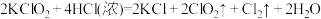 。(
。( 中氯元素的化合价为
中氯元素的化合价为 价)
价)(1)浓盐酸在反应中体现出来的性质是
(2)产生0.1molCl2时,转电子的数目为
(3)
 具有很强的氧化性,常用作消毒剂,其消毒效率(以同质量的物质到的电子数多少来衡量)是
具有很强的氧化性,常用作消毒剂,其消毒效率(以同质量的物质到的电子数多少来衡量)是 的
的
20-21高一上·江西·阶段练习 查看更多[1]
(已下线)【南昌新东方】莲塘一中化学高一10月份
更新时间:2020-04-03 16:15:11
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】实验室可用 和浓盐酸反应制取氯气。其变化可表述为
和浓盐酸反应制取氯气。其变化可表述为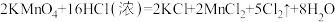 。
。
(1)请将上述化学方程式改写为离子方程式:_______ 。
(2)浓盐酸在反应中显示出来的性质是______ (填序号)。
①只有还原性 ②还原性和酸性
③只有氧化性 ④氧化性和酸性
(3)此反应中氧化产物是______ (填化学式)。
(4)用双线桥法表示该反应电子转移的方向和数目:_______ 。
 和浓盐酸反应制取氯气。其变化可表述为
和浓盐酸反应制取氯气。其变化可表述为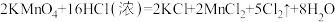 。
。(1)请将上述化学方程式改写为离子方程式:
(2)浓盐酸在反应中显示出来的性质是
①只有还原性 ②还原性和酸性
③只有氧化性 ④氧化性和酸性
(3)此反应中氧化产物是
(4)用双线桥法表示该反应电子转移的方向和数目:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】实验室中可以利用反应KClO3+6HCl=KCl+3Cl2↑+3H2O来制取氯气。
(1)用双线桥标出该反应中电子转移的方向和数目:_______
KClO3+6HCl(浓)=KCl+3Cl2+3H2O
(2)该反应中还原剂是___________ ,还原产物是___________ 。氧化剂是___________ 。氧化产物是___________ 。
(1)用双线桥标出该反应中电子转移的方向和数目:
KClO3+6HCl(浓)=KCl+3Cl2+3H2O
(2)该反应中还原剂是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】化合物Q是一种具有耐高温等优异性能的新型陶瓷.工业上可用以下方法制取:3SiO2+6C+2N2 Q+6CO
Q+6CO
(1)根据上述反应,推测Q的化学式为________ .
(2)上述反应中的还原剂是___________ .
(3)上述反应中,每消耗90g SiO2,可生成产物Q_______ g.
 Q+6CO
Q+6CO(1)根据上述反应,推测Q的化学式为
(2)上述反应中的还原剂是
(3)上述反应中,每消耗90g SiO2,可生成产物Q
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】铝热反应装置如下图:
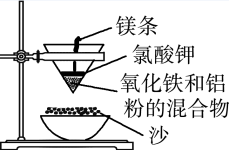
(1)该反应的化学方程式是_______ ;当消耗54g铝时,转移的电子数为_______ NA。
(2)若反应物无剩余,欲将生成物中的铁单质分离出来,采取的方法是:向生成物中加入足量的某种溶液,然后过滤。则这种溶液可以是:_______ (填序号)
①Ba(OH)2溶液 ②HCl溶液 ③NaOH溶液 ④H2SO4溶液
(3)写出反应物(Fe2O3、Al)分别与盐酸反应的离子方程式:_______ ;_______ 。

(1)该反应的化学方程式是
(2)若反应物无剩余,欲将生成物中的铁单质分离出来,采取的方法是:向生成物中加入足量的某种溶液,然后过滤。则这种溶液可以是:
①Ba(OH)2溶液 ②HCl溶液 ③NaOH溶液 ④H2SO4溶液
(3)写出反应物(Fe2O3、Al)分别与盐酸反应的离子方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】Na、Mg、Al、Fe、Cu、Zn是中学常见的金属率质,其合金在生活中有广泛应用。回答下列问题:
(1)实验室保存在煤油中的金属是___________ 。在潮湿空气中久置会生成绿色锈的金属是___________ 。
(2)铝合金广泛用于门窗,其耐腐蚀的主要原因是___________ 。
(3)一包钠铝合金与水恰好完全反应,收集到8960mLH₂(标准状况)。则这包合金中钠的物质的量为___________ ,铝的质量为___________ 。写出上述过程中涉及的两个反应的离子方程式:___________ 、___________ 。
(4)现有10g两种金属组成的合金与足量的稀硫酸反应产生11.2LH₂(标准状况)。则合金组成可能是___________(填字母)。
(5)等质量的镁、铝、锌与足量相同浓度的盐酸反应,产生H₂体积与时间关系如图所示。根据图像推知a、b、c曲线代表的金属依次是___________ (填元素符号)。
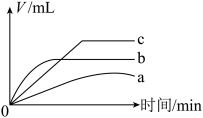
(1)实验室保存在煤油中的金属是
(2)铝合金广泛用于门窗,其耐腐蚀的主要原因是
(3)一包钠铝合金与水恰好完全反应,收集到8960mLH₂(标准状况)。则这包合金中钠的物质的量为
(4)现有10g两种金属组成的合金与足量的稀硫酸反应产生11.2LH₂(标准状况)。则合金组成可能是___________(填字母)。
| A.Mg和Cu | B.Al和Fe | C.Mg和Zn | D.Al和Cu |

您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】我国科学家用电化学装置实现了二氧化碳的资源化利用,反应的化学方程式为:CO2+NaCl CO+NaClO
CO+NaClO
(1)作还原剂的物质是___________ ,碳元素的化合价___________ (填“升高”或“降低”)。
(2)反应中每生成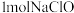 ,消耗
,消耗  的物质的量是
的物质的量是___________  ,转移电子的物质的量是
,转移电子的物质的量是___________  。
。
(3) 是一种常见的消毒剂,因在空气中转化成次氯酸而发挥消毒功能补全该反应的化学方程式
是一种常见的消毒剂,因在空气中转化成次氯酸而发挥消毒功能补全该反应的化学方程式________

 CO+NaClO
CO+NaClO(1)作还原剂的物质是
(2)反应中每生成
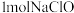 ,消耗
,消耗  的物质的量是
的物质的量是 ,转移电子的物质的量是
,转移电子的物质的量是 。
。(3)
 是一种常见的消毒剂,因在空气中转化成次氯酸而发挥消毒功能补全该反应的化学方程式
是一种常见的消毒剂,因在空气中转化成次氯酸而发挥消毒功能补全该反应的化学方程式
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】铜能与浓硝酸反应,化学方程式为:Cu+4HNO3=Cu(NO3)2+2NO2↑+2H2O
(1)用单线桥标出电子转移的方向和数目_______ 。
(2)上述反应中发生还原反应的物质是_______ ,被氧化的元素是_______ ,化合价降低的元素是_______ 。
(3)3个Cu被硝酸完全溶解后,Cu失去的电子数是_______ 个,产生气体_______ 个
(4)写出该反应的离子方程式_______ 。
(1)用单线桥标出电子转移的方向和数目
(2)上述反应中发生还原反应的物质是
(3)3个Cu被硝酸完全溶解后,Cu失去的电子数是
(4)写出该反应的离子方程式
您最近一年使用:0次



