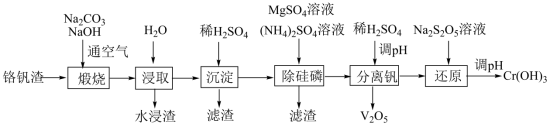
铬和钒具有广泛用途。铬钒渣中铬和钒以低价态含氧酸盐形式存在,主要杂质为铁、铝、硅、磷等的化合物,从铬钒渣中分离提取铬和钒的一种流程如下图所示: 存在,在碱性介质中以CrO
存在,在碱性介质中以CrO 存在。
存在。
回答下列问题:
(1)“沉淀”步骤调pH到弱碱性,主要除去的杂质是___________ 。
(2)“除硅磷”步骤中,使硅、磷分别以MgSiO3和MgNH4PO4的形式沉淀,该步需要控制溶液的pH≈9以达到最好的除杂效果,若pH<9时,会导致___________ ;pH>9时,会导致___________ 。
(3)“分离钒”步骤中,将溶液pH调到1.8左右得到V2O5沉淀,V2O5在pH<1时,溶解为VO 或VO3+在碱性条件下,溶解为VO
或VO3+在碱性条件下,溶解为VO 或VO
或VO ,上述性质说明V2O5具有
,上述性质说明V2O5具有___________ (填标号)。
A.酸性 B.碱性 C.两性
 存在,在碱性介质中以CrO
存在,在碱性介质中以CrO 存在。
存在。回答下列问题:
(1)“沉淀”步骤调pH到弱碱性,主要除去的杂质是
(2)“除硅磷”步骤中,使硅、磷分别以MgSiO3和MgNH4PO4的形式沉淀,该步需要控制溶液的pH≈9以达到最好的除杂效果,若pH<9时,会导致
(3)“分离钒”步骤中,将溶液pH调到1.8左右得到V2O5沉淀,V2O5在pH<1时,溶解为VO
 或VO3+在碱性条件下,溶解为VO
或VO3+在碱性条件下,溶解为VO 或VO
或VO ,上述性质说明V2O5具有
,上述性质说明V2O5具有A.酸性 B.碱性 C.两性
2024高三下·全国·专题练习 查看更多[1]
(已下线)大题01 化工流程综合题(逐空突破)-【大题精做】冲刺2024年高考化学大题突破+限时集训(新高考专用)
更新时间:2024-04-20 07:51:40
|
相似题推荐
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐1】乳酸亚铁固体{[CH3CH(OH)COO]2Fe,相对分子质量234}常用于治疗缺铁性贫血,易溶于水,难溶于乙醇。制备乳酸亚铁固体并测定其纯度的实验如下,回答下列问题:
I.制备碳酸亚铁
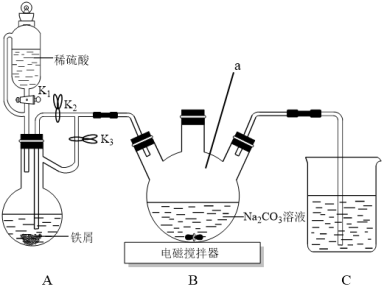
实验步骤:
第1步:组装仪器,检查装置气密性,加入试剂;
第2步:控制开关并制取氢气,排尽装置内的空气;
第3步:一段时间后,启动电磁搅拌器,并控制开关,制备FeCO3;
第4步:抽滤,洗涤干燥。
(1)仪器a名称_______ ;实验中所用蒸馏水均需经煮沸后快速冷却,目的是_______ 。
(2)第3步中“控制开关”的具体操作是_______ 。
(3)装置B中Na2CO3溶液可用NaHCO3溶液代替,反应的离子方程式为_______ 。
II.制备乳酸亚铁
向制得的FeCO3固体加入足量乳酸溶液,在75℃下搅拌使之充分反应。
(4)该反应的化学方程式为_______ 。反应结束后,从所得溶液中获得乳酸亚铁晶体的方法是低温蒸发、冷却结晶、过滤、_______ 、干燥。
III.乳酸亚铁晶体纯度的测量
(5)用铈量法测定产品中Fe2+的含量。称取3.9g样品配制成250mL溶液,取25.00mL,用0.10mol·L-1(NH4)4Ce(SO4)4标准溶液滴定(Ce元素被还原为Ce3+),重复滴定2~3次,平均消耗标准液15.00mL。
①称取3.9g样品配制成250mL溶液时,除用到托盘天平、烧杯、玻璃棒、量筒外,还用到的玻璃仪器有_______ 。
②产品中乳酸亚铁晶体的纯度为_______ 。
I.制备碳酸亚铁

实验步骤:
第1步:组装仪器,检查装置气密性,加入试剂;
第2步:控制开关并制取氢气,排尽装置内的空气;
第3步:一段时间后,启动电磁搅拌器,并控制开关,制备FeCO3;
第4步:抽滤,洗涤干燥。
(1)仪器a名称
(2)第3步中“控制开关”的具体操作是
(3)装置B中Na2CO3溶液可用NaHCO3溶液代替,反应的离子方程式为
II.制备乳酸亚铁
向制得的FeCO3固体加入足量乳酸溶液,在75℃下搅拌使之充分反应。
(4)该反应的化学方程式为
III.乳酸亚铁晶体纯度的测量
(5)用铈量法测定产品中Fe2+的含量。称取3.9g样品配制成250mL溶液,取25.00mL,用0.10mol·L-1(NH4)4Ce(SO4)4标准溶液滴定(Ce元素被还原为Ce3+),重复滴定2~3次,平均消耗标准液15.00mL。
①称取3.9g样品配制成250mL溶液时,除用到托盘天平、烧杯、玻璃棒、量筒外,还用到的玻璃仪器有
②产品中乳酸亚铁晶体的纯度为
您最近半年使用:0次
解答题-工业流程题
|
较难
(0.4)
【推荐2】电池级CoSO4可用于制备CoCO3和CoC2O4等钴盐。一种以Co(OH)3粗渣(含有Fe3O4、CuO、CaO、MgO、ZnO、SiO2等杂质)为原料制备电池级CoSO4·7H2O的工艺流程如图所示:
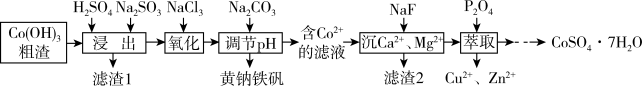
已知:黄钠铁矾化学式为NaFe3(SO4)2(OH)6,是一种淡黄色难溶物。
请回答下列问题:
(1)滤渣1的主要成分为_____ ,请写出一条提高钴元素浸出率的措施:______ 。
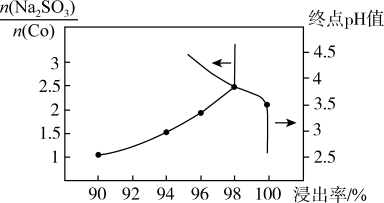
(2)“浸出”过程中加入Na2SO3的主要目的是_______ 。“浸出”过程中,Na2SO3用量、终点pH对钴浸出率的影响如图所示,则“浸出”过程中应控制的适宜条件是_______ 。
(3)“氧化”过程中加入NaClO3与Fe2+发生反应的离子方程式为_______ 。
(4)“调节pH”过程中,调节pH=5,写出生成黄钠铁矾[NaF3(SO4)2(OH)6]的离子方程式:_______ 。
(5)常温下,Ksp(CoCO3)=1.6×10-13,Ksp(CoC2O4)=6.4×10-8。向浓度均为0.01mol/L的Na2CO3和Na2C2O4混合溶液中加入CoSO4固体,当 完全沉淀的时候c(
完全沉淀的时候c( )∙c(
)∙c( )=
)=_______ [当c( )<1×10-5mol·L-1时,认为
)<1×10-5mol·L-1时,认为 完全沉淀]。
完全沉淀]。
(6)用CoSO4可制备CoC2O4。在空气中煅烧CoC2O4至恒重,得金属氧化物固体A和CO2。测得m(A)=12.05g,m(CO2)=13.2g,则A的化学式为_______ 。

已知:黄钠铁矾化学式为NaFe3(SO4)2(OH)6,是一种淡黄色难溶物。
请回答下列问题:
(1)滤渣1的主要成分为
(2)“浸出”过程中加入Na2SO3的主要目的是

(3)“氧化”过程中加入NaClO3与Fe2+发生反应的离子方程式为
(4)“调节pH”过程中,调节pH=5,写出生成黄钠铁矾[NaF3(SO4)2(OH)6]的离子方程式:
(5)常温下,Ksp(CoCO3)=1.6×10-13,Ksp(CoC2O4)=6.4×10-8。向浓度均为0.01mol/L的Na2CO3和Na2C2O4混合溶液中加入CoSO4固体,当
 完全沉淀的时候c(
完全沉淀的时候c( )∙c(
)∙c( )=
)= )<1×10-5mol·L-1时,认为
)<1×10-5mol·L-1时,认为 完全沉淀]。
完全沉淀]。(6)用CoSO4可制备CoC2O4。在空气中煅烧CoC2O4至恒重,得金属氧化物固体A和CO2。测得m(A)=12.05g,m(CO2)=13.2g,则A的化学式为
您最近半年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐3】将铜锌合金溶解后与足量KI溶液反应(Zn2+不与 反应),生成的I2用Na2S2O3标准溶液滴定,根据消耗的Na2S2O3溶液体积可测算合金中铜的含量。实验过程如下:
反应),生成的I2用Na2S2O3标准溶液滴定,根据消耗的Na2S2O3溶液体积可测算合金中铜的含量。实验过程如下:
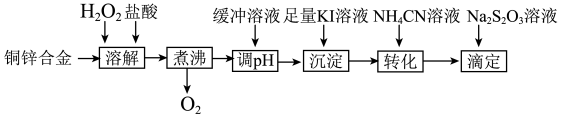
(1)“溶解”步骤中铜发生反应的离子方程式是_______ ,“煮沸”步骤的目的是_______ 。
(2)H2O2的电子式为_______ ,298K时,液态H2O2分解,每生成0.01molO2放出热量1.96kJ,该反应的热化学方程式为_______ 。
(3)“缓冲溶液”是浓度均为0.10 的CH3COOH和CH3COONH4的混合溶液。25℃时,缓冲溶液中各种离子浓度由大到小的顺序为____。[25℃时,
的CH3COOH和CH3COONH4的混合溶液。25℃时,缓冲溶液中各种离子浓度由大到小的顺序为____。[25℃时, ]
]
(4)“调pH”步骤将溶液pH由1调到6,如果缺少这一步,对实验的影响为___ 。
(5)“沉淀”步骤中有CuI沉淀产生,反应的离子方程式为_______ 。
(6)“转化”步骤中,CuI转化为CuSCN。沉淀完全转化后,溶液中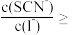
_______ 。[已知: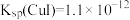 ;
; ]
]
 反应),生成的I2用Na2S2O3标准溶液滴定,根据消耗的Na2S2O3溶液体积可测算合金中铜的含量。实验过程如下:
反应),生成的I2用Na2S2O3标准溶液滴定,根据消耗的Na2S2O3溶液体积可测算合金中铜的含量。实验过程如下:
(1)“溶解”步骤中铜发生反应的离子方程式是
(2)H2O2的电子式为
(3)“缓冲溶液”是浓度均为0.10
 的CH3COOH和CH3COONH4的混合溶液。25℃时,缓冲溶液中各种离子浓度由大到小的顺序为____。[25℃时,
的CH3COOH和CH3COONH4的混合溶液。25℃时,缓冲溶液中各种离子浓度由大到小的顺序为____。[25℃时, ]
](4)“调pH”步骤将溶液pH由1调到6,如果缺少这一步,对实验的影响为
(5)“沉淀”步骤中有CuI沉淀产生,反应的离子方程式为
(6)“转化”步骤中,CuI转化为CuSCN。沉淀完全转化后,溶液中
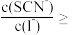
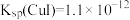 ;
; ]
]
您最近半年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐1】废钒催化剂的回收、提取和再利用具有显著的经济效益和环保效益。从某种废钒催化剂(含 、
、 、
、 、
、 、
、 等)中回收制备
等)中回收制备 的工艺流程如图:
的工艺流程如图:
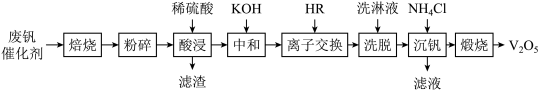
回答下列问题:
(1)工业生产中的钒催化剂一般以硅藻土为载体的优点是___________ 。
(2)“焙烧”的目的有___________ (填字母)、使低价元素转化为+5价钒元素。“焙烧”时低价钒元素被氧化生成 ,还生成的另一种氧化物为
,还生成的另一种氧化物为___________ (写化学式)。
A.改变废钒催化剂的结构,便于后续“酸浸”
B.除去废钒催化剂中的有机杂质
C.使废钒催化剂中的杂质氧化,便于除去
(3)“酸浸”时, 转化为
转化为 的化学方程式是
的化学方程式是___________ 。
(4)不同酸碱性的溶液中,+5价钒元素的存在形式不同,如图:
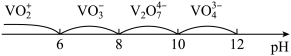
“中和”使溶液pH=7.5左右,则该步操作的目的是___________ 。
(5)“离子交换”效率与钒溶液通过离子交换树脂的流速及钒溶液的pH有关。
①钒溶液通过离子交换树脂的流速过慢,会导致溶液滞留,离子交换时间太长:而流速过快也会影响离子交换效果,原因是___________ 。
②吸附容量指在一定温度、一定浓度下,单位交换树脂吸附钒的最大量。某次实验中,测得溶液流速与吸附率、吸附容量的关系数据如表:
选用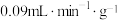 的吸附流速作为工作流速的理由是
的吸附流速作为工作流速的理由是___________ 。
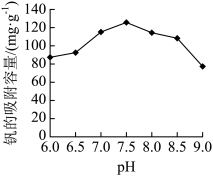
③钒吸附液的pH对吸附效果的影响如图所示,“离子交换”时应选用的pH=___________ 。
 、
、 、
、 、
、 、
、 等)中回收制备
等)中回收制备 的工艺流程如图:
的工艺流程如图:
回答下列问题:
(1)工业生产中的钒催化剂一般以硅藻土为载体的优点是
(2)“焙烧”的目的有
 ,还生成的另一种氧化物为
,还生成的另一种氧化物为A.改变废钒催化剂的结构,便于后续“酸浸”
B.除去废钒催化剂中的有机杂质
C.使废钒催化剂中的杂质氧化,便于除去
(3)“酸浸”时,
 转化为
转化为 的化学方程式是
的化学方程式是(4)不同酸碱性的溶液中,+5价钒元素的存在形式不同,如图:

“中和”使溶液pH=7.5左右,则该步操作的目的是
(5)“离子交换”效率与钒溶液通过离子交换树脂的流速及钒溶液的pH有关。
①钒溶液通过离子交换树脂的流速过慢,会导致溶液滞留,离子交换时间太长:而流速过快也会影响离子交换效果,原因是
②吸附容量指在一定温度、一定浓度下,单位交换树脂吸附钒的最大量。某次实验中,测得溶液流速与吸附率、吸附容量的关系数据如表:
吸附流速/(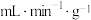 ) ) |  平均吸附率/% 平均吸附率/% | 工作吸附容量/( ) ) |
| 0.07 | 99.12 | 155.5 |
| 0.09 | 98.99 | 135.4 |
| 0.11 | 98.35 | 99.7 |
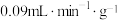 的吸附流速作为工作流速的理由是
的吸附流速作为工作流速的理由是③钒吸附液的pH对吸附效果的影响如图所示,“离子交换”时应选用的pH=

您最近半年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐2】 是化工生产中重要的催化剂,可用于制备硫酸和彩色玻璃。一种以含钒废料(主要成分为
是化工生产中重要的催化剂,可用于制备硫酸和彩色玻璃。一种以含钒废料(主要成分为 ,还含有
,还含有 、
、 、
、 、有机物杂质)制备
、有机物杂质)制备 的工艺流程如下图所示。
的工艺流程如下图所示。

已知:①含钒离子在溶液中的存在形式与溶液 的关系
的关系
②该流程温度下: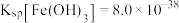 ;
; ;
;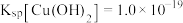
请回答下列问题:
(1)“焙烧”的目的之一是将 转化为
转化为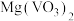 ,还有一个目的是
,还有一个目的是___________ ;
(2)已知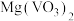 难溶于水,能溶于酸,写出在“酸浸”时(
难溶于水,能溶于酸,写出在“酸浸”时(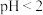 )发生的离子反应方程式
)发生的离子反应方程式___________ 。为提高酸浸速率,可采取的措施___________ (填序号)。
a.使用98%的硫酸 b.加速搅拌 c.升高温度 d.增大压强
(3)“调 净化Ⅰ”时需将
净化Ⅰ”时需将 、
、 、
、 三种离子去除干净(浓度
三种离子去除干净(浓度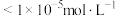 时视为去除干净),需调节
时视为去除干净),需调节 范围为
范围为___________ 。
(4)“净化Ⅱ”时,若加入过量 ,可能导致的结果是
,可能导致的结果是___________ 。
(5)“煅烧”时,改变环境会得到不同产物,但都会有 生成。若煅烧时隔绝空气,还生成物质A和水,且A可在该流程中循环使用;若煅烧时通入空气,物质A会继续被氧化为无毒气体,则在空气中煅烧的化学方程式为
生成。若煅烧时隔绝空气,还生成物质A和水,且A可在该流程中循环使用;若煅烧时通入空气,物质A会继续被氧化为无毒气体,则在空气中煅烧的化学方程式为___________ 。
 是化工生产中重要的催化剂,可用于制备硫酸和彩色玻璃。一种以含钒废料(主要成分为
是化工生产中重要的催化剂,可用于制备硫酸和彩色玻璃。一种以含钒废料(主要成分为 ,还含有
,还含有 、
、 、
、 、有机物杂质)制备
、有机物杂质)制备 的工艺流程如下图所示。
的工艺流程如下图所示。
已知:①含钒离子在溶液中的存在形式与溶液
 的关系
的关系溶液 | 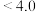 | 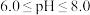 | 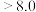 |
| 钒元素存在形式 |  |  |  |
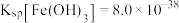 ;
; ;
;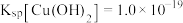
请回答下列问题:
(1)“焙烧”的目的之一是将
 转化为
转化为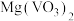 ,还有一个目的是
,还有一个目的是(2)已知
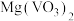 难溶于水,能溶于酸,写出在“酸浸”时(
难溶于水,能溶于酸,写出在“酸浸”时(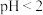 )发生的离子反应方程式
)发生的离子反应方程式a.使用98%的硫酸 b.加速搅拌 c.升高温度 d.增大压强
(3)“调
 净化Ⅰ”时需将
净化Ⅰ”时需将 、
、 、
、 三种离子去除干净(浓度
三种离子去除干净(浓度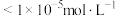 时视为去除干净),需调节
时视为去除干净),需调节 范围为
范围为(4)“净化Ⅱ”时,若加入过量
 ,可能导致的结果是
,可能导致的结果是(5)“煅烧”时,改变环境会得到不同产物,但都会有
 生成。若煅烧时隔绝空气,还生成物质A和水,且A可在该流程中循环使用;若煅烧时通入空气,物质A会继续被氧化为无毒气体,则在空气中煅烧的化学方程式为
生成。若煅烧时隔绝空气,还生成物质A和水,且A可在该流程中循环使用;若煅烧时通入空气,物质A会继续被氧化为无毒气体,则在空气中煅烧的化学方程式为
您最近半年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
【推荐3】钒的用途十分广泛,有金属“维生素”之称。以含钒石煤(主要成分是V2O3、V2O4,含有的杂质有SiO2、FeS2及Mg、Al、Mn等的化合物)制备单质钒的工艺流程如图所示。
②Ksp(CaCO3)=2.8×10-9,Ksp(CaSiO3)=2.5×10-8,Ksp[Ca(VO3)2]远大于Ksp(CaCO3)。
回答下列问题:
(1)写出Cr3+的核外电子排布式为________ 。
(2)为了提高“焙烧”效率,可采取的措施有______ 。
(3)“焙烧”时,V2O3、V2O4都转化为Ca(VO3)2,写出V2O4转化为Ca(VO3)2的化学方程式:_____ 。
(4)“水浸”加入Na2CO3调节溶液的pH为8.5,可完全除去的金属离子有______ ;“水浸”加入过量Na2CO3不能使CaSiO3完全转化为CaCO3,原因是_______ 。(列式计算平衡常数分析该反应进行的趋势,一般认为,K>105时反应进行较完全,K<105时反应难以进行)
(5)“离子交换”与“洗脱”可表示为[RCl4]+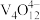
 [R-V4O12]+4Cl- ([RCl4]为强碱性阴离子交换树脂,
[R-V4O12]+4Cl- ([RCl4]为强碱性阴离子交换树脂,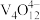 为
为 在水溶液中的实际存在形式),则“洗脱”过程中“淋洗液”最好选用
在水溶液中的实际存在形式),则“洗脱”过程中“淋洗液”最好选用_____ 。
(6)下列金属冶炼方法中,与本工艺流程中冶炼钒的方法相似的是____ (填字母)。
A.铝热反应制锰 B.电解熔融氯化钠制钠 C.氧化汞分解制汞

| 金属离子 | Fe3+ | Mg2+ | Al3+ | Mn2+ |
| 开始沉淀时的pH | 1.9 | 7.0 | 3.0 | 8.1 |
| 完全沉淀时的pH | 3.2 | 9.0 | 4.7 | 10.1 |
回答下列问题:
(1)写出Cr3+的核外电子排布式为
(2)为了提高“焙烧”效率,可采取的措施有
(3)“焙烧”时,V2O3、V2O4都转化为Ca(VO3)2,写出V2O4转化为Ca(VO3)2的化学方程式:
(4)“水浸”加入Na2CO3调节溶液的pH为8.5,可完全除去的金属离子有
(5)“离子交换”与“洗脱”可表示为[RCl4]+
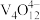
 [R-V4O12]+4Cl- ([RCl4]为强碱性阴离子交换树脂,
[R-V4O12]+4Cl- ([RCl4]为强碱性阴离子交换树脂,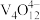 为
为 在水溶液中的实际存在形式),则“洗脱”过程中“淋洗液”最好选用
在水溶液中的实际存在形式),则“洗脱”过程中“淋洗液”最好选用(6)下列金属冶炼方法中,与本工艺流程中冶炼钒的方法相似的是
A.铝热反应制锰 B.电解熔融氯化钠制钠 C.氧化汞分解制汞
您最近半年使用:0次
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐1】实验室利用Cr2O3固体和CCl4反应制备无水CrCl3,并收集该反应产生的光气(COCl2),实验装置如图所示(夹持及加热装置已省略)。
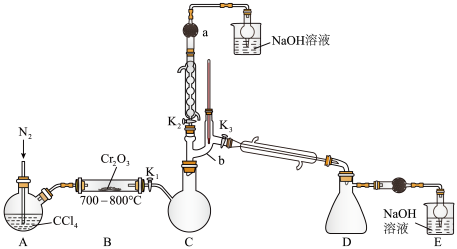
已知:I.光气与水易反应,能溶于CCl4溶液
II.有关物质熔沸点:
回答下列问题:
(1)开始通入N2的作用为______ 。
(2)B中发生反应的化学方程式为_____ ,分离出光气(COCl2)的操作为_____ (填操作名称)。
(3)实验步骤如下:
检查完装置气密性,打开K1、K2、K3,通入氮气;一段时间后,开关K1、K2、K3的状态分别为_____ ,将装置A在85℃下进行水浴加热:待B中反应结束后,停止高温加热,将装置C在30℃下进行水浴加热,此时开关K1、K2、K3的状态分别为_____ ;实验结束,停止通入氮气。
(4)取B中所得产品加入稀硫酸,完全溶解后分为两等份,进行如下操作:
i.取其中一份,加入NaOH溶液形成绿色的Cr(OH)3沉淀后,再加入过量H2O2,小火加热至沉淀完全转变为Na2CrO4溶液后,再继续加热一段时间;继续加水至溶液体积为100mL,取20mL溶液酸化,再滴入指示剂,用新配制的0.2mol•L-1的(NH4)2Fe(SO4)2溶液进行滴定,到达滴定终点时,消耗(NH4)2Fe(SO4)2溶液36.00mL。
ii.取另外一份加入过量NaOH溶液,经过滤、洗涤、干燥后,将所得固体在空气中灼烧,得到铬的氧化物1.2g。
①写出i中滴定过程反应的离子方程式:______ 。
②步骤ii中得到的铬的氧化物的化学式为______ 。步骤i中,若最后不再加热一段时间,步骤ii中铬的氧化物中铬元素的化合价将______ (填“偏高”“偏低”或“不变”)。

已知:I.光气与水易反应,能溶于CCl4溶液
II.有关物质熔沸点:
| Cr2O3 | CrCl3 | CCl4 | COCl2 | |
| 熔点/℃ | 1435 | 1152 | -23 | -118 |
| 沸点/℃ | 4000 | 1300 | 76 | 8.2 |
(1)开始通入N2的作用为
(2)B中发生反应的化学方程式为
(3)实验步骤如下:
检查完装置气密性,打开K1、K2、K3,通入氮气;一段时间后,开关K1、K2、K3的状态分别为
(4)取B中所得产品加入稀硫酸,完全溶解后分为两等份,进行如下操作:
i.取其中一份,加入NaOH溶液形成绿色的Cr(OH)3沉淀后,再加入过量H2O2,小火加热至沉淀完全转变为Na2CrO4溶液后,再继续加热一段时间;继续加水至溶液体积为100mL,取20mL溶液酸化,再滴入指示剂,用新配制的0.2mol•L-1的(NH4)2Fe(SO4)2溶液进行滴定,到达滴定终点时,消耗(NH4)2Fe(SO4)2溶液36.00mL。
ii.取另外一份加入过量NaOH溶液,经过滤、洗涤、干燥后,将所得固体在空气中灼烧,得到铬的氧化物1.2g。
①写出i中滴定过程反应的离子方程式:
②步骤ii中得到的铬的氧化物的化学式为
您最近半年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐2】含铬化合物在生产生活中有着广泛的用途。利用含铬废液(主要含 、
、 、
、 、
、 等)可制备强氧化剂
等)可制备强氧化剂 。
。

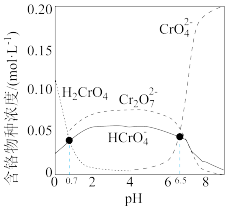
已知:室温下 总浓度为
总浓度为 溶液中,含铬物种浓度随
溶液中,含铬物种浓度随 的分布如图所示。
的分布如图所示。
(1)写出含铬废液中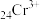 的电子排布式
的电子排布式_______ 。
(2)混合时温度为什么不宜过高_______ 。
(3)写出调节 约为12时
约为12时 氧化为
氧化为 的离子方程式
的离子方程式_______ 。
(4)利用 制备
制备 ,向密闭反应釜中加入
,向密闭反应釜中加入

 溶液,再加入蔗糖
溶液,再加入蔗糖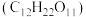 充分反应生成
充分反应生成 、
、 和
和 。熔烧
。熔烧 得到
得到 ,理论上需要向反应釜中加入蔗糖的物质的量为
,理论上需要向反应釜中加入蔗糖的物质的量为_______ mol。
(5)纳米零价铁可将水体中 还原为
还原为 ,再将
,再将 转化为
转化为 (两性氢氧化物)从水体中除去。
(两性氢氧化物)从水体中除去。
① 的
的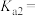
_______ 。
②调节溶液 ,可使
,可使 转化为
转化为 沉淀而被除去。当
沉淀而被除去。当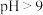 时,铬的去除率却降低,其原因是
时,铬的去除率却降低,其原因是_______ 。
 、
、 、
、 、
、 等)可制备强氧化剂
等)可制备强氧化剂 。
。
已知:室温下
 总浓度为
总浓度为 溶液中,含铬物种浓度随
溶液中,含铬物种浓度随 的分布如图所示。
的分布如图所示。
(1)写出含铬废液中
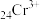 的电子排布式
的电子排布式(2)混合时温度为什么不宜过高
(3)写出调节
 约为12时
约为12时 氧化为
氧化为 的离子方程式
的离子方程式(4)利用
 制备
制备 ,向密闭反应釜中加入
,向密闭反应釜中加入

 溶液,再加入蔗糖
溶液,再加入蔗糖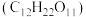 充分反应生成
充分反应生成 、
、 和
和 。熔烧
。熔烧 得到
得到 ,理论上需要向反应釜中加入蔗糖的物质的量为
,理论上需要向反应釜中加入蔗糖的物质的量为(5)纳米零价铁可将水体中
 还原为
还原为 ,再将
,再将 转化为
转化为 (两性氢氧化物)从水体中除去。
(两性氢氧化物)从水体中除去。①
 的
的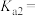
②调节溶液
 ,可使
,可使 转化为
转化为 沉淀而被除去。当
沉淀而被除去。当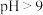 时,铬的去除率却降低,其原因是
时,铬的去除率却降低,其原因是
您最近半年使用:0次
解答题-工业流程题
|
较难
(0.4)
【推荐3】钒铬还原渣是钠化提钒过程的固体废弃物,其主要成分为VO2 ·xH2O、Cr(OH)3及少量的SiO2, 一种初步分离钒铬还原渣中钒铬并获得Na2Cr2O7的工艺流程如图所示:

已知:①“酸浸”后VO2 ·xH2O转化为VO2+;
②当pH>4. 1时,Cr3+开始沉淀:
③Na2Cr2O7和Na2SO4的溶解度随温度变化的曲线如图所示:

回答下列问题:
(1)Na2S2O8名称为过二硫酸钠、该物质中存在−O−O−, 则该化合物中硫元素的化合价是_______ 价;写出滤渣的一种用途: ___________ 。
(2)已知“氧化”生成 ,“水解沉钒”过程中,生成V2O5·xH2O的离子方程式为
,“水解沉钒”过程中,生成V2O5·xH2O的离子方程式为___________ ;若“水解沉钒”后溶液(常温)中(Cr3+)=0. 1mol·L-1,则此温度下Ksp[Cr(OH)3]=___________ 。
(3)“溶液1”过程中,铬元素由Cr3+转化为 , 当有3mol
, 当有3mol  生成时,理论上消耗
生成时,理论上消耗___________ mol H2O2。
(4)“多步操作”包括蒸发浓缩、___________ 、冷却结晶、过滤、洗涤等步骤。
(5)研究温度对Na2S2O8与 H2O2的氧化一水解沉钒率的影响,得到如图所示结果。钒铬还原渣酸浸液初始温度在90°C左右,降低温度能耗增加。由图可知,分别采用 H2O2、Na2S2O8进行“氧化”时,应选择的适宜温度分别是___________ 、___________ 。

(6)获得Na2Cr2O7后,残留的含铬废水不能直接排放,处理时需要经过“酸化→还原→沉降”三个步骤,用Na2S2O3溶液还原时,还原产物为Cr3+, 则反应的离子方程式为___________ 。

已知:①“酸浸”后VO2 ·xH2O转化为VO2+;
②当pH>4. 1时,Cr3+开始沉淀:
③Na2Cr2O7和Na2SO4的溶解度随温度变化的曲线如图所示:

回答下列问题:
(1)Na2S2O8名称为过二硫酸钠、该物质中存在−O−O−, 则该化合物中硫元素的化合价是
(2)已知“氧化”生成
 ,“水解沉钒”过程中,生成V2O5·xH2O的离子方程式为
,“水解沉钒”过程中,生成V2O5·xH2O的离子方程式为(3)“溶液1”过程中,铬元素由Cr3+转化为
 , 当有3mol
, 当有3mol  生成时,理论上消耗
生成时,理论上消耗(4)“多步操作”包括蒸发浓缩、
(5)研究温度对Na2S2O8与 H2O2的氧化一水解沉钒率的影响,得到如图所示结果。钒铬还原渣酸浸液初始温度在90°C左右,降低温度能耗增加。由图可知,分别采用 H2O2、Na2S2O8进行“氧化”时,应选择的适宜温度分别是

(6)获得Na2Cr2O7后,残留的含铬废水不能直接排放,处理时需要经过“酸化→还原→沉降”三个步骤,用Na2S2O3溶液还原时,还原产物为Cr3+, 则反应的离子方程式为
您最近半年使用:0次



