在自然界中存在反应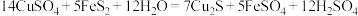 (
( 中Fe为+2价,S为-1价)。下列说法正确的是
中Fe为+2价,S为-1价)。下列说法正确的是
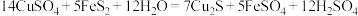 (
( 中Fe为+2价,S为-1价)。下列说法正确的是
中Fe为+2价,S为-1价)。下列说法正确的是A. 为还原剂,发生氧化反应 为还原剂,发生氧化反应 |
B.生成物中的 和 和 皆为氧化产物 皆为氧化产物 |
C. 中的S被氧化和被还原的个数比为3∶7 中的S被氧化和被还原的个数比为3∶7 |
D.每生成lmol ,反应中转移的电子是2mol ,反应中转移的电子是2mol |
更新时间:2024-04-23 15:48:48
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】在常温下发生下列反应,根据反应,判断下列结论中正确的是
①16H++10Z-+2XO =2X2++5Z2+8H2O;
=2X2++5Z2+8H2O;
②2A2++B2=2A3++2B-;
③2B-+Z2=B2+2Z-。
①16H++10Z-+2XO
 =2X2++5Z2+8H2O;
=2X2++5Z2+8H2O;②2A2++B2=2A3++2B-;
③2B-+Z2=B2+2Z-。
| A.Z2在①、③反应中均为氧化剂 |
| B.溶液中可能发生:2A3++2Z-=Z2+2A2+ |
| C.还原性强弱顺序为:A2+>B->Z->X2+ |
| D.若消耗1molH+反应①中转移1.6mol电子 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】在标准状况下将3.2g铜粉投入一定量浓 中,随着铜粉的溶解,反应生成的气体颜色逐渐变浅,当铜粉完全溶解后共收集到由
中,随着铜粉的溶解,反应生成的气体颜色逐渐变浅,当铜粉完全溶解后共收集到由 和NO组成的混合气体1.344L(已转化为标况下的体积),则混合气体中NO的体积为
和NO组成的混合气体1.344L(已转化为标况下的体积),则混合气体中NO的体积为
 中,随着铜粉的溶解,反应生成的气体颜色逐渐变浅,当铜粉完全溶解后共收集到由
中,随着铜粉的溶解,反应生成的气体颜色逐渐变浅,当铜粉完全溶解后共收集到由 和NO组成的混合气体1.344L(已转化为标况下的体积),则混合气体中NO的体积为
和NO组成的混合气体1.344L(已转化为标况下的体积),则混合气体中NO的体积为| A.112mL | B.224mL | C.448mL | D.1008mL |
您最近一年使用:0次
【推荐1】实验室利用Bi(OH)3制取高锰酸钠的相关反应的离子方程式如下:
I.ClO +6H++5Cl-=3Cl2+3H2O;
+6H++5Cl-=3Cl2+3H2O;
II.Bi(OH)3+3OH-+Cl2+Na+=NaBiO3↓+2Cl-+3H2O;
III.5NaBiO3+2Mn2++14H+=2MnO +5Bi3++5Na++7H2O。
+5Bi3++5Na++7H2O。
下列说法正确的是
A.反应I中氧化产物和还原产物的物质的量比为1∶5
B.酸性条件下的氧化性:ClO > Cl2 > NaBiO3 > MnO
> Cl2 > NaBiO3 > MnO
C.NaBiO3可与盐酸发生反应:NaBiO3+6H++2Cl-=Bi3++Cl2↑+3H2O+Na+
D.制得142g高锰酸钠时,理论上消耗氯酸钠的物质的量为1mol
I.ClO
 +6H++5Cl-=3Cl2+3H2O;
+6H++5Cl-=3Cl2+3H2O;II.Bi(OH)3+3OH-+Cl2+Na+=NaBiO3↓+2Cl-+3H2O;
III.5NaBiO3+2Mn2++14H+=2MnO
 +5Bi3++5Na++7H2O。
+5Bi3++5Na++7H2O。下列说法正确的是
A.反应I中氧化产物和还原产物的物质的量比为1∶5
B.酸性条件下的氧化性:ClO
 > Cl2 > NaBiO3 > MnO
> Cl2 > NaBiO3 > MnO
C.NaBiO3可与盐酸发生反应:NaBiO3+6H++2Cl-=Bi3++Cl2↑+3H2O+Na+
D.制得142g高锰酸钠时,理论上消耗氯酸钠的物质的量为1mol
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】向重铬酸盐酸性溶液中加入乙醚和 ,水层发生反应:
,水层发生反应: (已知
(已知 的结构为
的结构为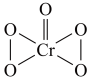 ),乙醚层发生反应:
),乙醚层发生反应: 。反应上层出现蓝色,一段时间后溶液蓝色褪去,且水相变为绿色(
。反应上层出现蓝色,一段时间后溶液蓝色褪去,且水相变为绿色( ),下列说法正确的是
),下列说法正确的是
 ,水层发生反应:
,水层发生反应: (已知
(已知 的结构为
的结构为 ),乙醚层发生反应:
),乙醚层发生反应: 。反应上层出现蓝色,一段时间后溶液蓝色褪去,且水相变为绿色(
。反应上层出现蓝色,一段时间后溶液蓝色褪去,且水相变为绿色( ),下列说法正确的是
),下列说法正确的是A.由水层反应可知,氧化性: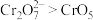 |
| B.乙醚在检验过程中可用乙醇代替 |
C.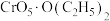 中不存在非极性键 中不存在非极性键 |
D.水相变为绿色的离子反应为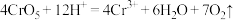 ,该反应生成 ,该反应生成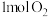 转移 转移 电子 电子 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】高铁酸钾( )是一种新型、高效、多功能水处理剂,工业上采用向KOH溶液中通氯气,然后再加入
)是一种新型、高效、多功能水处理剂,工业上采用向KOH溶液中通氯气,然后再加入 溶液的方法制备
溶液的方法制备 ,发生如下反应:①
,发生如下反应:①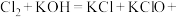
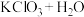 (未配平)、②
(未配平)、②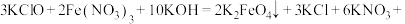
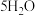 ,下列说法正确的是
,下列说法正确的是
 )是一种新型、高效、多功能水处理剂,工业上采用向KOH溶液中通氯气,然后再加入
)是一种新型、高效、多功能水处理剂,工业上采用向KOH溶液中通氯气,然后再加入 溶液的方法制备
溶液的方法制备 ,发生如下反应:①
,发生如下反应:①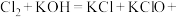
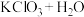 (未配平)、②
(未配平)、②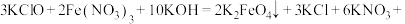
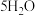 ,下列说法正确的是
,下列说法正确的是A.若反应①中有标准状况下11.2L 参加反应,则消耗1molKOH 参加反应,则消耗1molKOH |
B.若反应①中 ,则氧化剂与还原剂的物质的量之比为1:3 ,则氧化剂与还原剂的物质的量之比为1:3 |
C.氧化性: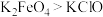 |
D.反应②中每消耗1mol 转移6mol电子 转移6mol电子 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】以不同类别物质间的转化为线索,认识钠及其化合物。下列分析不正确的是
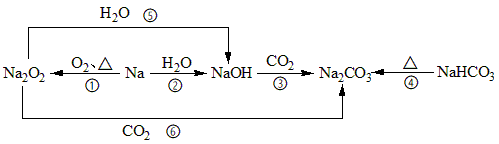

| A.1molNa和O2发生反应①转移1mol电子 |
| B.②中发生的离子方程式:2Na+2H2O=2Na++2OH-+H2↑ |
| C.反应⑤表明Na2O2是碱性氧化物 |
| D.上述转化中发生的反应有分解反应、化合反应、置换反应 |
您最近一年使用:0次

 反应中,若有213 g氯气生成,则反应中转移电子的数目为6NA
反应中,若有213 g氯气生成,则反应中转移电子的数目为6NA 被还原为
被还原为 的一些性质或用途如图,下列说法正确的是
的一些性质或用途如图,下列说法正确的是
 ,则反应过程中转移12mol电子
,则反应过程中转移12mol电子 和
和 的化学计量数均为1
的化学计量数均为1 ,含
,含 等杂质)提取钛单质,同时获得绿矾。工艺流程如图:
等杂质)提取钛单质,同时获得绿矾。工艺流程如图:
 水解为难溶的
水解为难溶的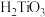 。下列说法错误的是
。下列说法错误的是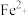 被氧化
被氧化 ,可循环使用
,可循环使用 ,则转移电子数为
,则转移电子数为


