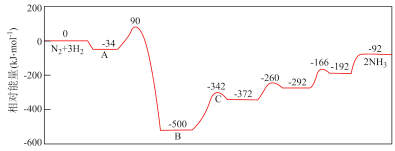
基元反应过渡态理论认为,基元反应在从反应物到产物的变化过程中要经历一个中间状态,这个状态称为过渡态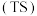 。某反应在催化剂作用下的反应进程如图所示,下列说法正确的是
。某反应在催化剂作用下的反应进程如图所示,下列说法正确的是
 。某反应在催化剂作用下的反应进程如图所示,下列说法正确的是
。某反应在催化剂作用下的反应进程如图所示,下列说法正确的是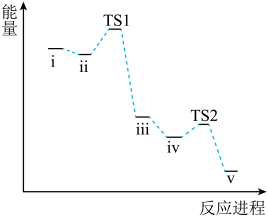
| A.步骤ii→iii为决速步 |
| B.使用催化剂降低了反应的焓变 |
| C.基于上述理论,该反应进程中包含四步基元反应 |
| D.升高温度,反应物分子中活化分子的百分数不变 |
更新时间:2024-05-18 14:13:41
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】已知反应 的反应机理如下:
的反应机理如下:
①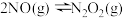 (快)
(快)
② (慢)
(慢)
③ (快)
(快)
下列有关说法错误的是
 的反应机理如下:
的反应机理如下:①
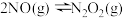 (快)
(快)②
 (慢)
(慢)③
 (快)
(快)下列有关说法错误的是
| A.①的逆反应速率大于②的正反应速率 |
B.②中 与 与 的碰撞仅部分有效 的碰撞仅部分有效 |
C. 和 和 是该反应的催化剂 是该反应的催化剂 |
| D.总反应中逆反应的活化能比正反应的活化能大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】CH4与Cl2生成CH3Cl的反应过程中,中间态物质的能量关系如图所示(Ea表示活化能)。下列说法不正确 的是


A.已知Cl•是由Cl2在光照条件下化学键断裂生成的,该过程可表示为: |
| B.相同条件下,Ea越大相应的反应速率越慢 |
| C.图中ΔH<0,其大小与Ea1、Ea2无关 |
D.CH4+Cl2 CH3Cl+HCl是一步就能完成的反应 CH3Cl+HCl是一步就能完成的反应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】水煤气变换反应为:CO(g)+H2O(g)=CO2(g)+H2(g)。我国学者结合实验与计算机模拟结果,研究了在金催化剂表面上水煤气变换的反应历程,如图所示,其中吸附在金催化剂表面上的物种用•标注。下列说法正确的是


| A.水煤气变换反应的△H>0 |
| B.步骤③的化学方程式为:CO•+OH•=COOH• |
| C.步骤⑤的热化学方程式可写为:COOH•+2H•+OH•=CO2(g)+H2(g)+H2O• △H=-2.24eV•mol-1 |
| D.该历程中最大能垒(活化能)E正=2.02eV |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】利用 -丁内酯制备四氢呋喃,反应过程中伴有生成1-丁醇的副反应,涉及反应如下:
-丁内酯制备四氢呋喃,反应过程中伴有生成1-丁醇的副反应,涉及反应如下:
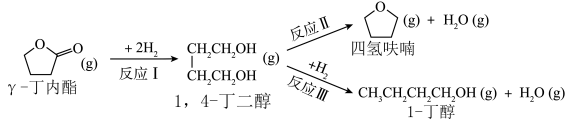
已知:反应Ⅰ为快速反应,反应Ⅱ、Ⅲ为慢速反应。在493K、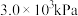 的高压
的高压 氛围下(
氛围下( 压强近似等于总压),以
压强近似等于总压),以
 -丁内酯为初始原料,x(
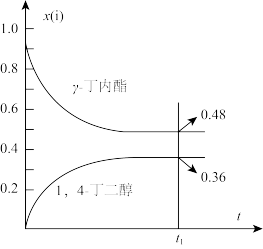
-丁内酯为初始原料,x( -丁内酯)和x(1,4-丁二醇)随时间t变化关系如图所示[x(i)表示某物种i的物质的量与除
-丁内酯)和x(1,4-丁二醇)随时间t变化关系如图所示[x(i)表示某物种i的物质的量与除 外其它各物种总物质的量之比]。下列说法正确的是
外其它各物种总物质的量之比]。下列说法正确的是
 -丁内酯制备四氢呋喃,反应过程中伴有生成1-丁醇的副反应,涉及反应如下:
-丁内酯制备四氢呋喃,反应过程中伴有生成1-丁醇的副反应,涉及反应如下:
已知:反应Ⅰ为快速反应,反应Ⅱ、Ⅲ为慢速反应。在493K、
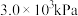 的高压
的高压 氛围下(
氛围下( 压强近似等于总压),以
压强近似等于总压),以
 -丁内酯为初始原料,x(
-丁内酯为初始原料,x( -丁内酯)和x(1,4-丁二醇)随时间t变化关系如图所示[x(i)表示某物种i的物质的量与除
-丁内酯)和x(1,4-丁二醇)随时间t变化关系如图所示[x(i)表示某物种i的物质的量与除 外其它各物种总物质的量之比]。下列说法正确的是
外其它各物种总物质的量之比]。下列说法正确的是
A. -丁内酯分子中 -丁内酯分子中 键与 键与 键数目之比为6∶1 键数目之比为6∶1 |
| B.生成四氢呋喃的速率主要决定于反应Ⅰ |
C. 时刻 时刻 |
D.增大 的压强一定有利于提高四氢呋喃产率 的压强一定有利于提高四氢呋喃产率 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】已知反应: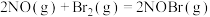
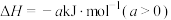 ,其反应机理如下:
,其反应机理如下:
①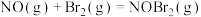
 快反应;
快反应;
②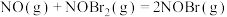
 慢反应。
慢反应。
下列说法不正确的是
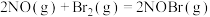
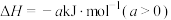 ,其反应机理如下:
,其反应机理如下:①
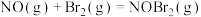
 快反应;
快反应;②
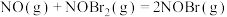
 慢反应。
慢反应。下列说法不正确的是
A.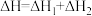 |
| B.该反应的反应速率主要取决于反应② |
| C.NOBr2是该反应的中间产物,不是催化剂 |
| D.恒容时,增大Br2(g)的浓度能增加单位体积内活化分子百分数,加快反应速率 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下图是用钌 (Ru )基催化剂催化CO2(g)和H2(g)的反应的示意图,当反应生成46g液态HCOOH时放出31.2 kJ的热量。下列说法正确的是
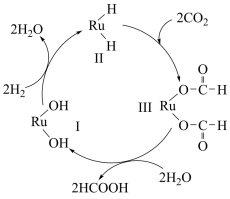
| A.图示中物质I、II、III均为该反应的催化剂 |
| B.使用催化剂可以降低反应的活化能,从而改变反应的焓变 |
| C.由题意知:HCOOH(l)=CO2(g)+H2(g) ΔH = +31.2kJ· mol-1 |
| D.因使用钌基催化剂使反应CO2(g) + H2(g)= HCOOH(l)分两步进行 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】中国科学家首次用 改性铜基催化剂,将草酸二甲酯加氢制乙二醇的反应条件从高压降至常压。草酸二甲酯加氢的主要反应有:
改性铜基催化剂,将草酸二甲酯加氢制乙二醇的反应条件从高压降至常压。草酸二甲酯加氢的主要反应有:
反应Ⅰ:
反应Ⅱ:
反应Ⅲ:
其他条件相同时,相同时间内温度对产物选择性的影响结果如图。 (生成B所用的草酸二甲酯)/n(转化的草酸二甲酯)×100%;ⅱ.450~500K,反应Ⅲ的平衡常数远大于反应Ⅰ和反应Ⅱ的平衡常数)
(生成B所用的草酸二甲酯)/n(转化的草酸二甲酯)×100%;ⅱ.450~500K,反应Ⅲ的平衡常数远大于反应Ⅰ和反应Ⅱ的平衡常数)
下列说法不正确的是
 改性铜基催化剂,将草酸二甲酯加氢制乙二醇的反应条件从高压降至常压。草酸二甲酯加氢的主要反应有:
改性铜基催化剂,将草酸二甲酯加氢制乙二醇的反应条件从高压降至常压。草酸二甲酯加氢的主要反应有:反应Ⅰ:

反应Ⅱ:

反应Ⅲ:

其他条件相同时,相同时间内温度对产物选择性的影响结果如图。

 (生成B所用的草酸二甲酯)/n(转化的草酸二甲酯)×100%;ⅱ.450~500K,反应Ⅲ的平衡常数远大于反应Ⅰ和反应Ⅱ的平衡常数)
(生成B所用的草酸二甲酯)/n(转化的草酸二甲酯)×100%;ⅱ.450~500K,反应Ⅲ的平衡常数远大于反应Ⅰ和反应Ⅱ的平衡常数)下列说法不正确的是
| A.制乙二醇适宜的温度范围是470~480K |
| B.减压可提高乙二醇的平衡产率 |
| C.实验条件下反应Ⅲ的活化能最高,升温更有利于反应Ⅲ |
D.铜基催化剂用 改性后反应速率增大,可以降低反应所需的压强 改性后反应速率增大,可以降低反应所需的压强 |
您最近一年使用:0次