按要求回答下列问题:
(1)下列各组微粒:
① 与
与 ;②
;② 和
和 ;③H、D、T;④金刚石和石墨;⑤
;③H、D、T;④金刚石和石墨;⑤ 和
和 ;⑥
;⑥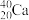 和
和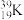 。
。
互为同位素的是___________ (填序号),透过蓝色钴玻璃观察K元素燃烧时的焰色为___________ 色。
(2)现有如下三个反应:
A.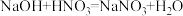
B.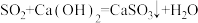
C.
根据三个反应本质,能设计成原电池的是___________ (填“A”、“B”或“C”)。该原电池的负极材料为___________ ,若导线上转移电子0.6mol,则电极减少的质量是___________ g。
(1)下列各组微粒:
①
 与
与 ;②
;② 和
和 ;③H、D、T;④金刚石和石墨;⑤
;③H、D、T;④金刚石和石墨;⑤ 和
和 ;⑥
;⑥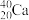 和
和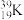 。
。互为同位素的是
(2)现有如下三个反应:
A.
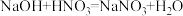
B.
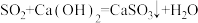
C.

根据三个反应本质,能设计成原电池的是
更新时间:2024-05-04 16:31:50
|
相似题推荐
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】如图所示,是原电池的装置图。请回答:
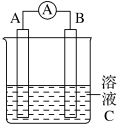
(1)若C为稀H2SO4溶液,电流表指针发生偏转,B电极材料为Fe且做负极,则A电极的材料是_________ (选锌或铜);反应进行一段时间后溶液C的浓度将________ (填“升高”“降低”或“基本不变”)。
(2)若需将反应:Cu+2Fe3+=Cu2++2Fe2+设计成如图所示的原电池装置,则正极电极反应式_________ ,溶液C是________ 。
(3)若C为CuCl2溶液,Zn是________ 极,Cu极发生________ 反应,电极反应为_________ 。反应过程溶液中c(Cu2+)________ (填“变大”“变小”或“不变”)。
(4)CO与H2反应还可制备CH3OH,CH3OH可作为燃料使用,用CH3OH和O2组合形成的质子交换膜燃料电池的结构示意图如图:
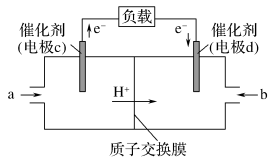
电池总反应为2CH3OH+3O2=2CO2+4H2O,则d电极是_______ (填“正极”或“负极”),c电极的反应方程式为_______ 。d电极反应式______ ,若线路中转移6mol电子,则上述CH3OH燃料电池,消耗的O2在标准状况下的体积为________ L。

(1)若C为稀H2SO4溶液,电流表指针发生偏转,B电极材料为Fe且做负极,则A电极的材料是
(2)若需将反应:Cu+2Fe3+=Cu2++2Fe2+设计成如图所示的原电池装置,则正极电极反应式
(3)若C为CuCl2溶液,Zn是
(4)CO与H2反应还可制备CH3OH,CH3OH可作为燃料使用,用CH3OH和O2组合形成的质子交换膜燃料电池的结构示意图如图:

电池总反应为2CH3OH+3O2=2CO2+4H2O,则d电极是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】依据氧化还原反应: 设计的原电池如图所示。
设计的原电池如图所示。
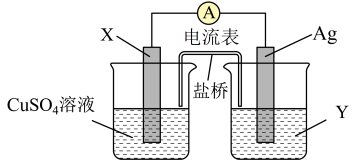
请回答下列问题:
(1)电极X的材料是___________ ;电解质溶液Y是___________ 。
(2)银电极为电池的___________ 极,发生的电极反应为___________ ;X电极上发生的电极反应为___________ 。
(3)外电路中的电子从___________ 电极流向___________ 电极。
 设计的原电池如图所示。
设计的原电池如图所示。
请回答下列问题:
(1)电极X的材料是
(2)银电极为电池的
(3)外电路中的电子从
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】原电池正负极的判断
(1)一般情况下活泼的金属做原电池的________ ,另一极做正极。
(2)根据实验现象:一般情况下,有气体或者固体生成的一极为________ ,溶解或者质量减少的一极为_________ 。
(3)电子流出的一极是_______ ,流入的一极是_______ 。
(4)发生_______ 反应的一极是负极,发生_______ 反应的一极是正极。
(5)溶液中阴离子向_______ 极移动,阳离子向_______ 极移动。
(1)一般情况下活泼的金属做原电池的
(2)根据实验现象:一般情况下,有气体或者固体生成的一极为
(3)电子流出的一极是
(4)发生
(5)溶液中阴离子向
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
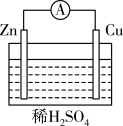
【推荐2】由铜、锌和硫酸溶液组成的原电池中,作正极的是____ (填化学式),正极的电极反应式为____ ;作负极的是____ (填化学式),电子由____ (填“正”或“负”,下同)极经导线移向_____ 极。

您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】利用人工光合作用合成甲酸的原理为2CO2+2H2O 2HCOOH+O2,装置如图所示。
2HCOOH+O2,装置如图所示。
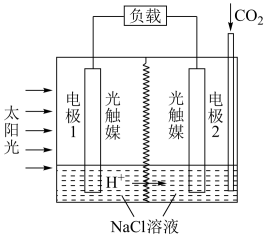
请回答下列问题:
(1)从能量角度分析,该装置将太阳能转化为___________ 。
(2)NaCl溶液的作用是___________ 。
(3)电极1为___________ (填“正极”或“负极”),电极2的电极反应式为___________ 。
(4)产生O2的电极是___________ (填“电极1”或“电极2”),每消耗0.5molCO2时,理论上生成O2体积为___________ (标准状况下)。
 2HCOOH+O2,装置如图所示。
2HCOOH+O2,装置如图所示。
请回答下列问题:
(1)从能量角度分析,该装置将太阳能转化为
(2)NaCl溶液的作用是
(3)电极1为
(4)产生O2的电极是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】按要求填空。
(1)2016年IUPAC将第117号元素命名为Ts,则中子数为176的Ts的核素符号是________ 。
(2)漂粉精可做漂白棉、麻、纸张的漂白剂,也可用于游泳池等场所的消毒剂,其主要成分是________ 。
(3)目前,汽车尾气系统中均安装了催化转化器。在催化转化器中,汽车尾气中的CO和NO在催化剂的作用下发生反应,生成 和
和 。指出上述反应中的氧化剂与氧化产物的物质的量之比
。指出上述反应中的氧化剂与氧化产物的物质的量之比________ 。
(4)现有NaCl、 ,和
,和 三种无色溶液,选用一种试剂把它们鉴别出来,请写出该试剂与
三种无色溶液,选用一种试剂把它们鉴别出来,请写出该试剂与 反应的离子方程式
反应的离子方程式________ 。
(1)2016年IUPAC将第117号元素命名为Ts,则中子数为176的Ts的核素符号是
(2)漂粉精可做漂白棉、麻、纸张的漂白剂,也可用于游泳池等场所的消毒剂,其主要成分是
(3)目前,汽车尾气系统中均安装了催化转化器。在催化转化器中,汽车尾气中的CO和NO在催化剂的作用下发生反应,生成
 和
和 。指出上述反应中的氧化剂与氧化产物的物质的量之比
。指出上述反应中的氧化剂与氧化产物的物质的量之比(4)现有NaCl、
 ,和
,和 三种无色溶液,选用一种试剂把它们鉴别出来,请写出该试剂与
三种无色溶液,选用一种试剂把它们鉴别出来,请写出该试剂与 反应的离子方程式
反应的离子方程式
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】请按要求填写下列空白:
(1)写出表示含有8个质子、10个中子的原子的核组成符号:________ ;
(2)CO2的电子式是________ ,NH4Cl的电子式是________ ;
(3)物质在下列变化过程中克服的是:①共价键②离子键。(填序号)
HCl溶于水____ ;电解熔融NaCl制Na____ ;电解水分解生成O2和H2______ 。
(4)下列物质中:互为同分异构体的有_________ ;互为同素异形体的有________ ;
属于同位素的有________ ; 属于同一种物质的有________ 。(填序号)
①液氯 ②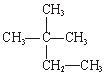 ③白磷 ④氯气 ⑤
③白磷 ④氯气 ⑤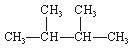 ⑥
⑥ Cl ⑦
Cl ⑦ Cl ⑧红磷
Cl ⑧红磷
(1)写出表示含有8个质子、10个中子的原子的核组成符号:
(2)CO2的电子式是
(3)物质在下列变化过程中克服的是:①共价键②离子键。(填序号)
HCl溶于水
(4)下列物质中:互为同分异构体的有
属于同位素的有
①液氯 ②
 ③白磷 ④氯气 ⑤
③白磷 ④氯气 ⑤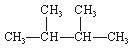 ⑥
⑥ Cl ⑦
Cl ⑦ Cl ⑧红磷
Cl ⑧红磷
您最近一年使用:0次

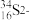 微粒中的质子数是
微粒中的质子数是

