某实验小组设计如图所示实验装置来制取乙炔,并粗略测定电石(含有N、P、S等元素)中碳化钙的质量分数。回答下列问题:_________ 。
(2)仪器b中发生反应的化学方程式为_________ ,实验过程中为了减缓水与电石的反应速率,可采取的措施是_________ (写一条即可)。
(3)将生成的气体通入酸性KMnO4溶液中,观察到酸性KMnO4溶液褪色。
①_______ (填“能”或“不能”)说明生成的气体全部为乙炔,原因是______ 。
②实验小组发现该实验不能用启普发生器来制取乙炔,理由是______ (写一条即可)。
(4)为了安全,点燃乙炔前应_______ ,乙炔燃烧时的现象是____________ 。
(5)取mg电石样品,使其与水完全反应,实验结束后测得排入量筒中水的体积为VmL,则电石中碳化钙的质量分数为______ (用含V和m的代数式表示,忽略导管中残留的水和气体中含有的水蒸气,所有气体均已换算成标准状况下)。
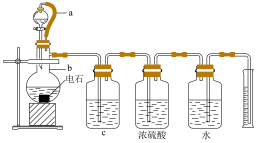
(2)仪器b中发生反应的化学方程式为
(3)将生成的气体通入酸性KMnO4溶液中,观察到酸性KMnO4溶液褪色。
①
②实验小组发现该实验不能用启普发生器来制取乙炔,理由是
(4)为了安全,点燃乙炔前应
(5)取mg电石样品,使其与水完全反应,实验结束后测得排入量筒中水的体积为VmL,则电石中碳化钙的质量分数为
更新时间:2024-05-05 14:45:51
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】实验室用乙醇制取乙烯,用电石(主要成分为CaC2,含少量CaS)制取乙炔。
(1)实验室制取乙烯的化学方程式为_____________________________ ,可用于制取乙烯的发生装置是_______ 。(选填编号)
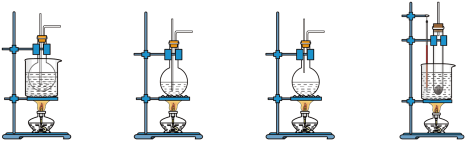
(2)制备乙烯气体时,常因温度过高而观察到溶液变黑,同时能闻到有刺激性气味的气体生成。在乙烯气体的制备过程中,浓硫酸没有体现的性质是________ 。
a 吸水性 b 脱水性 c 强氧化性 d 酸性
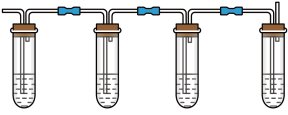
有同学设计下列实验确认上述混合气体中有乙烯和二氧化硫。
上图中①、②、③、④装置盛放的试剂分别是(根据需要进行选择,填标号):
①_______________ ,②_______________ ,③_______________ ,④______________ 。
A 品红溶液 B NaOH溶液 C 浓硫酸 D 酸性高锰酸钾溶液
(3)实验室制备乙炔的化学反应方程式为_________________________________ 。实验室制乙炔时为避免电石和水反应过于激烈,除用分液漏斗控制滴速外,通常还可用_________ 代替水。为除去乙炔中混有的少量硫化氢杂质,可将气体通过___________ (选填编号)。
a酸性KMnO4溶液 b CCl4 c NaOH溶液 d CuSO4溶液
(1)实验室制取乙烯的化学方程式为

a b c d
(2)制备乙烯气体时,常因温度过高而观察到溶液变黑,同时能闻到有刺激性气味的气体生成。在乙烯气体的制备过程中,浓硫酸没有体现的性质是
a 吸水性 b 脱水性 c 强氧化性 d 酸性

① ② ③ ④
有同学设计下列实验确认上述混合气体中有乙烯和二氧化硫。
上图中①、②、③、④装置盛放的试剂分别是(根据需要进行选择,填标号):
①
A 品红溶液 B NaOH溶液 C 浓硫酸 D 酸性高锰酸钾溶液
(3)实验室制备乙炔的化学反应方程式为
a酸性KMnO4溶液 b CCl4 c NaOH溶液 d CuSO4溶液
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】为探究乙炔与溴的加成反应,甲同学设计并进行了如下实验:先取一定量工业用电石与水反应,将生成的气体通入溴水中,发现溶液褪色,即证明乙炔与溴水发生了加成反应。乙同学发现在甲同学的实验中,褪色后的溶液里有少许淡黄色浑浊,推测在制得的乙炔中还可能含有少量还原性的杂质气体,由此他提出必须先除去之,再与溴水反应。请你回答下列问题:
(1)写出甲同学实验中两个主要的化学方程式:__________________________ ;_____________ 。
(2)甲同学设计的实验________ (填“能”或“不能”)验证乙炔与溴发生加成反应,其理由是________ 。
a.使溴水褪色的反应,未必是加成反应
b.使溴水褪色的反应,就是加成反应
c.使溴水褪色的物质,未必是乙炔
d.使溴水褪色的物质,就是乙炔
(3)乙同学推测此乙炔中必定含有的一种杂质气体是______ ,它与溴水反应的化学方程式是______________________________ ,在验证过程中必须全部除去。
(4)请你选用下列四个装置(可重复使用)来实现乙同学的实验方案,将它们的编号填入方框,并写出装置内所放的化学药品______ ,______ ,______ 。
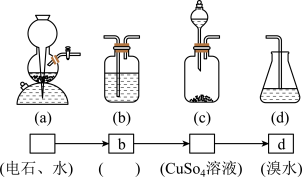
(5)为验证这一反应是加成而不是取代,丙同学提出可用pH试纸来测试反应后溶液的酸性,理由是_______________________ 。
(1)写出甲同学实验中两个主要的化学方程式:
(2)甲同学设计的实验
a.使溴水褪色的反应,未必是加成反应
b.使溴水褪色的反应,就是加成反应
c.使溴水褪色的物质,未必是乙炔
d.使溴水褪色的物质,就是乙炔
(3)乙同学推测此乙炔中必定含有的一种杂质气体是
(4)请你选用下列四个装置(可重复使用)来实现乙同学的实验方案,将它们的编号填入方框,并写出装置内所放的化学药品

(5)为验证这一反应是加成而不是取代,丙同学提出可用pH试纸来测试反应后溶液的酸性,理由是
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
【推荐3】C是一种合成树脂,用于制备塑料和合成纤维,D是一种植物生长调节剂,用它可以催熟果实。根据以下化学反应框图填空:

(1)写出A的电子式_______________ ;
(2)写出碳化钙与水反应制取A的化学方程式________________ ;B→C的化学方程式________________ ,其反应类型为_______________ 。
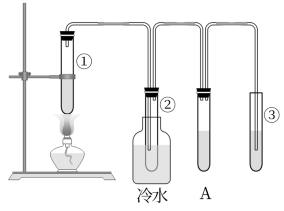
(3)D还可以用石蜡油制取,石蜡油(17个碳原子以上的液态烷烃混合物)的分解实验装置如图所示(部分仪器已省略)。在试管①中加入石蜡油和氧化铝(催化石蜡分解);试管②放在冷水中,试管③中加入溴水。
实验现象:
试管①中加热一段时间后,可以看到试管内液体沸腾;
试管②中有少量液体凝结,闻到汽油的气味,往液体中滴加几滴高锰酸钾酸性溶液颜色褪去。根据实验现象回答下列问题:
(4)装置A的作用是__________________
(5)试管①中发生的主要反应有:C17H36 C8H18+C9H18;C8H18
C8H18+C9H18;C8H18 C4H10+C4H8。丁烷可进一步裂解,除得到甲烷和乙烷外,还可以得到另两种有机物,它们的结构简式为
C4H10+C4H8。丁烷可进一步裂解,除得到甲烷和乙烷外,还可以得到另两种有机物,它们的结构简式为_____________ 和____________ ,这两种有机物混合后在一定条件下其可能结构为____________ 。
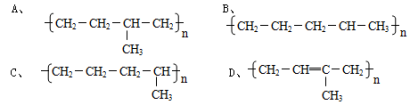
(6)写出试管③中反应的一个化学方程式_______________________ 。

(1)写出A的电子式
(2)写出碳化钙与水反应制取A的化学方程式
(3)D还可以用石蜡油制取,石蜡油(17个碳原子以上的液态烷烃混合物)的分解实验装置如图所示(部分仪器已省略)。在试管①中加入石蜡油和氧化铝(催化石蜡分解);试管②放在冷水中,试管③中加入溴水。

实验现象:
试管①中加热一段时间后,可以看到试管内液体沸腾;
试管②中有少量液体凝结,闻到汽油的气味,往液体中滴加几滴高锰酸钾酸性溶液颜色褪去。根据实验现象回答下列问题:
(4)装置A的作用是
(5)试管①中发生的主要反应有:C17H36
 C8H18+C9H18;C8H18
C8H18+C9H18;C8H18 C4H10+C4H8。丁烷可进一步裂解,除得到甲烷和乙烷外,还可以得到另两种有机物,它们的结构简式为
C4H10+C4H8。丁烷可进一步裂解,除得到甲烷和乙烷外,还可以得到另两种有机物,它们的结构简式为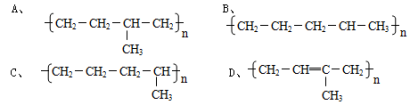
(6)写出试管③中反应的一个化学方程式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】工业废水中常含有一定量氧化性较强的 ,利用滴定原理测定
,利用滴定原理测定 含量(通常以
含量(通常以 废水中的微粒质量计量)的方法如下:
废水中的微粒质量计量)的方法如下:
步骤I:量取 废水于锥形瓶中,加入适量稀酸酸化。
废水于锥形瓶中,加入适量稀酸酸化。
步骤II:加入过量的碘化钾溶液充分反应:
步骤III:向锥形瓶中滴入几滴指示剂。用滴定管量取 溶液进行滴定(
溶液进行滴定( ),数据记录如表:
),数据记录如表:
(1)取 固体配制
固体配制 溶液,需要的定量仪器有托盘天平、量筒和
溶液,需要的定量仪器有托盘天平、量筒和___________ 。
(2)步骤I量取 废水选择的仪器是①
废水选择的仪器是①_______ 。
②排除碱式滴定管中气泡的方法应采用如图所示操作中的_______ ,然后小心操作使尖嘴部分充满碱液。
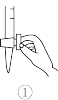


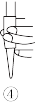
③步骤I中加入适量的酸酸化,该酸可以是_______ (填标号)。
A.盐酸 B.稀硫酸 C.草酸 D.浓硝酸
(3)步骤III中滴加的指示剂为_______ ;滴定达到终点时的实验现象是___________ 。
(4)步骤III中a的读数如图所示,则:
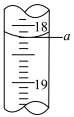
①a=___________ mL。
②计算废水中 含量为
含量为___________ g/L。
(5)以下操作会造成废水中 含量测定值偏高的是___________(填字母)。
含量测定值偏高的是___________(填字母)。
(6)若用25mL滴定管进行实验,当滴定管中的液面在刻度“10”处,则管内液体的体积___________ (填序号)。
(7)
(8)①=10mL ②=15mL ③<10mL ④>15mL
 ,利用滴定原理测定
,利用滴定原理测定 含量(通常以
含量(通常以 废水中的微粒质量计量)的方法如下:
废水中的微粒质量计量)的方法如下:步骤I:量取
 废水于锥形瓶中,加入适量稀酸酸化。
废水于锥形瓶中,加入适量稀酸酸化。步骤II:加入过量的碘化钾溶液充分反应:

步骤III:向锥形瓶中滴入几滴指示剂。用滴定管量取
 溶液进行滴定(
溶液进行滴定( ),数据记录如表:
),数据记录如表:| 滴定次数 |  溶液起始读数/mL 溶液起始读数/mL |  溶液终点读数/mL 溶液终点读数/mL |
| 第一次 | 1.02 | 19.03 |
| 第二次 | 2.00 | 19.99 |
| 第三次 | 0.20 | a |
(1)取
 固体配制
固体配制 溶液,需要的定量仪器有托盘天平、量筒和
溶液,需要的定量仪器有托盘天平、量筒和(2)步骤I量取
 废水选择的仪器是①
废水选择的仪器是①②排除碱式滴定管中气泡的方法应采用如图所示操作中的
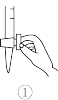


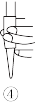
③步骤I中加入适量的酸酸化,该酸可以是
A.盐酸 B.稀硫酸 C.草酸 D.浓硝酸
(3)步骤III中滴加的指示剂为
(4)步骤III中a的读数如图所示,则:

①a=
②计算废水中
 含量为
含量为(5)以下操作会造成废水中
 含量测定值偏高的是___________(填字母)。
含量测定值偏高的是___________(填字母)。| A.滴定终点读数时,俯视滴定管的刻度 |
| B.盛装待测液的锥形瓶用蒸馏水洗过,未用待测液润洗 |
| C.滴定到终点读数时发现滴定管尖嘴处悬挂一滴溶液 |
D.量取 溶液的滴定管用蒸馏水洗后未用标准液润洗 溶液的滴定管用蒸馏水洗后未用标准液润洗 |
(6)若用25mL滴定管进行实验,当滴定管中的液面在刻度“10”处,则管内液体的体积
(7)
(8)①=10mL ②=15mL ③<10mL ④>15mL
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】学习小组探究了铜的氧化过程及铜的氧化物的组成。回答下列问题:
(1)铜与浓硝酸反应的装置如下图,
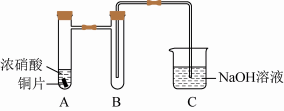
仪器A的名称为___________ ,装置B的作用为___________ 。
(2)铜与过量H2O2反应的探究如下:
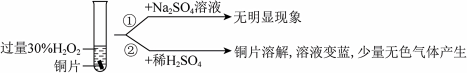
实验②中Cu溶解的离子方程式为___________ ;产生的气体为___________ 。比较实验①和②,H+既不是氧化剂,又不是还原剂、但可增强H2O2的氧化性。
(3)用足量NaOH处理实验②溶液得沉淀X,元素分析表明为铜的氧化物,提纯干燥后的X在惰性氛围下加热mgX完全分解为ng黑色氧化物Y,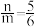 。X的化学式为
。X的化学式为___________ 。
(4)取含X粗品0.0500g(杂质不参加反应)与过量的酸性KI溶液完全反应后,调节溶液至弱酸性。以淀粉为指示剂,用0.1000mol/LNa2S2O3标准溶液滴定,滴定终点时消耗Na2S2O3标准溶液15.00mL。(已知:2Cu2++4I-=2CuI↓+I2,I2+2 =2I-+
=2I-+ )标志滴定终点的现象是
)标志滴定终点的现象是___________ ,粗品中X的相对含量为___________ 。
(5)对于上述实验,下列说法正确的是___________。
(1)铜与浓硝酸反应的装置如下图,

仪器A的名称为
(2)铜与过量H2O2反应的探究如下:

实验②中Cu溶解的离子方程式为
(3)用足量NaOH处理实验②溶液得沉淀X,元素分析表明为铜的氧化物,提纯干燥后的X在惰性氛围下加热mgX完全分解为ng黑色氧化物Y,
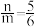 。X的化学式为
。X的化学式为(4)取含X粗品0.0500g(杂质不参加反应)与过量的酸性KI溶液完全反应后,调节溶液至弱酸性。以淀粉为指示剂,用0.1000mol/LNa2S2O3标准溶液滴定,滴定终点时消耗Na2S2O3标准溶液15.00mL。(已知:2Cu2++4I-=2CuI↓+I2,I2+2
 =2I-+
=2I-+ )标志滴定终点的现象是
)标志滴定终点的现象是(5)对于上述实验,下列说法正确的是___________。
| A.容量瓶用于配制标准溶液,进行容量瓶检漏时,倒置一次即可 |
| B.盛Na2S2O3的滴定管用蒸馏水洗净后未用标准液润洗会使测定结果偏低 |
| C.滴定读数时,应单手持滴定管上端并保持其自然垂直 |
| D.滴定前平视读数,滴定终点俯视读数会使测定结果偏高 |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】NaNO2可用作食品添加剂。NaNO2能发生以下反应:3NO2-+2H+=NO3-+2NO↑+H2O
NO2-+Ag+=AgNO2↓(淡黄色)
某化学兴趣小组进行以下探究。回答有关问题:
(l)制取NaNO2反应原理:Na2CO3+2NO2=NaNO2+NaNO3+CO2 Na2CO3+NO+NO2=2NaNO2+CO2
用下图所示装置进行实验。

①铜与浓硝酸反应的化学方程式为______________________________ 。
②实验过程中,需控制B中溶液的pH>7,否则产率会下降,理由是_________ 。
③往C中通入空气的目的是____________________ (用化学方程式表示)。
④反应结束后,B中溶液经蒸发浓缩、冷却结晶、___________ 等操作,可得到粗产品晶体和母液。
(2)测定粗产品中NaNO2的含量
称取5.000g粗产品,溶解后稀释至250mL。取出25.00 mL溶液,用0.1000 mol·L-1KMNO4酸性溶液平行滴定三次,平均消耗的体积为20.00mL。已知:2MnO4-+6H++5NO2-=5NO3-+2Mn2++3H2O
①稀释溶液时,需使用的玻璃仪器除烧杯、玻璃棒外,还有_________ (填标号)。
A.容量瓶 B.量筒 C.胶头滴管 D.锥形瓶
②当观察到_________________ 时,滴定达到终点。
③粗产品中NaNO2的质量分数为____________ (用代数式表示)。
NO2-+Ag+=AgNO2↓(淡黄色)
某化学兴趣小组进行以下探究。回答有关问题:
(l)制取NaNO2反应原理:Na2CO3+2NO2=NaNO2+NaNO3+CO2 Na2CO3+NO+NO2=2NaNO2+CO2
用下图所示装置进行实验。

①铜与浓硝酸反应的化学方程式为
②实验过程中,需控制B中溶液的pH>7,否则产率会下降,理由是
③往C中通入空气的目的是
④反应结束后,B中溶液经蒸发浓缩、冷却结晶、
(2)测定粗产品中NaNO2的含量
称取5.000g粗产品,溶解后稀释至250mL。取出25.00 mL溶液,用0.1000 mol·L-1KMNO4酸性溶液平行滴定三次,平均消耗的体积为20.00mL。已知:2MnO4-+6H++5NO2-=5NO3-+2Mn2++3H2O
①稀释溶液时,需使用的玻璃仪器除烧杯、玻璃棒外,还有
A.容量瓶 B.量筒 C.胶头滴管 D.锥形瓶
②当观察到
③粗产品中NaNO2的质量分数为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】硫氰化钾(KSCN)俗称玫瑰红酸钾,是一种用途广泛的化学药品。实验室模拟工业制备硫氰化钾的实验装置如图所示:
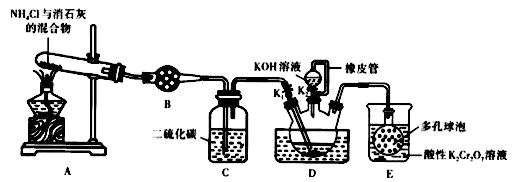
已知:
①NH3不溶于CS2,CS2的密度比水大且不溶于水
②三颈烧瓶内盛放CS2、水和催化剂
③CS2+3NH3 =NH4SCN+NH4HS,该反应比较缓慢且NH4SCN在高于170℃时易分解
回答下列问题:
(1)装置A中反应的化学方程式是_______
(2)装置B中的试剂是_______
(3)制备KSCN溶液:①反应一段时间后,熄灭装置A中的酒精灯,关闭K,保持三颈烧瓶内液温105℃一段时间,这样操作的目的是_______
②然后打开K2,继续保持液温105℃,缓缓滴入适量的KOH溶液,写出装置D中生成KSCN的化学方程式:______
(4)装置E的作用是:_______
(5)制备硫氰化钾晶体:先滤去三颈烧瓶中的固体催化剂,再减压蒸发浓缩、_______ 、_______ 洗涤、干燥,得到硫氰化钾晶体。
(6)测定晶体中KSCN的含量:称取10.0g样品,配成1000mL溶液。从中量取20.00mL溶液于锥形瓶中,加入适量稀硝酸,再加入几滴Fe(NO)3溶液作指示剂,用0.1000 mol L-1AgNO3标准溶液滴定,达到滴定终点时消耗AgNO3准溶液18.00mL。[已知滴定时发生的反应为SCN-+Ag+=AgSCN↓(白色)
L-1AgNO3标准溶液滴定,达到滴定终点时消耗AgNO3准溶液18.00mL。[已知滴定时发生的反应为SCN-+Ag+=AgSCN↓(白色)
①达到滴定终点时的现象是_______
②样品中KSCN的质量分数为_______

已知:
①NH3不溶于CS2,CS2的密度比水大且不溶于水
②三颈烧瓶内盛放CS2、水和催化剂
③CS2+3NH3 =NH4SCN+NH4HS,该反应比较缓慢且NH4SCN在高于170℃时易分解
回答下列问题:
(1)装置A中反应的化学方程式是
(2)装置B中的试剂是
(3)制备KSCN溶液:①反应一段时间后,熄灭装置A中的酒精灯,关闭K,保持三颈烧瓶内液温105℃一段时间,这样操作的目的是
②然后打开K2,继续保持液温105℃,缓缓滴入适量的KOH溶液,写出装置D中生成KSCN的化学方程式:
(4)装置E的作用是:
(5)制备硫氰化钾晶体:先滤去三颈烧瓶中的固体催化剂,再减压蒸发浓缩、
(6)测定晶体中KSCN的含量:称取10.0g样品,配成1000mL溶液。从中量取20.00mL溶液于锥形瓶中,加入适量稀硝酸,再加入几滴Fe(NO)3溶液作指示剂,用0.1000 mol
 L-1AgNO3标准溶液滴定,达到滴定终点时消耗AgNO3准溶液18.00mL。[已知滴定时发生的反应为SCN-+Ag+=AgSCN↓(白色)
L-1AgNO3标准溶液滴定,达到滴定终点时消耗AgNO3准溶液18.00mL。[已知滴定时发生的反应为SCN-+Ag+=AgSCN↓(白色)①达到滴定终点时的现象是
②样品中KSCN的质量分数为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】三氯化六氨合钴(III){[Co(NH3)6]Cl3}是一种重要的原料。实验室以活性炭为催化剂,用H2O2、CoCl2为原料制备[Co(NH3)6]Cl3,反应过程中会放出大量的热。
已知:①Co2+不易被氧化,Co3+具有强氧化性;[Co(NH3)6]2+具有较强还原性,[Co(NH3)6]3+性质稳定。
②[Co(NH3)6]Cl3在水中的溶解度曲线图所示。
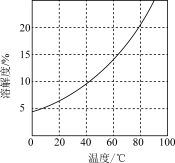
③加入少量浓盐酸有利于[Co(NH3)6]Cl3析出。
制备[Co(NH3)6]Cl3实验步骤如下:
I.称取研细的CoCl2•6H2O10.0g和NH4Cl5.0g于烧杯中溶解,将溶液转入三颈烧瓶,加入25mL浓氨水和适量活性炭粉末,控制温度在10℃以下,逐滴加入5mL30%的H2O2溶液。实验装置如图所示。
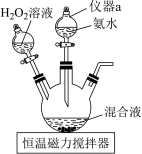
II.将混合物在水浴1中反应一段时间,再改用水浴2处理,充分结晶后过滤。
III.……
(1)上图中仪器a的名称为___________ 。
(2)步骤I将Co2+转化[Co(NH3)6]3+过程中,先加浓氨水,后加H2O2溶液的目的是________ 。
(3)步骤II中采用“冰水浴”的是_______ (填“水浴1”或“水浴2”)。制备[Co(NH3)6]Cl3的总反应化学方程式为_______ 。
(4)[Co(NH3)6]Cl3配合物的内界为________ (用化学式表示)。
(5)步骤III是为了获得纯净的[Co(NH3)6]Cl3。设计由步骤II过滤后的滤渣获取[Co(NH3)6]Cl3的实验方案:向滤渣中加入80℃左右的热水,充分搅拌后,___________ ,低温干燥(实验中须使用的试剂:浓盐酸、无水乙醇)。
已知:①Co2+不易被氧化,Co3+具有强氧化性;[Co(NH3)6]2+具有较强还原性,[Co(NH3)6]3+性质稳定。
②[Co(NH3)6]Cl3在水中的溶解度曲线图所示。

③加入少量浓盐酸有利于[Co(NH3)6]Cl3析出。
制备[Co(NH3)6]Cl3实验步骤如下:
I.称取研细的CoCl2•6H2O10.0g和NH4Cl5.0g于烧杯中溶解,将溶液转入三颈烧瓶,加入25mL浓氨水和适量活性炭粉末,控制温度在10℃以下,逐滴加入5mL30%的H2O2溶液。实验装置如图所示。

II.将混合物在水浴1中反应一段时间,再改用水浴2处理,充分结晶后过滤。
III.……
(1)上图中仪器a的名称为
(2)步骤I将Co2+转化[Co(NH3)6]3+过程中,先加浓氨水,后加H2O2溶液的目的是
(3)步骤II中采用“冰水浴”的是
(4)[Co(NH3)6]Cl3配合物的内界为
(5)步骤III是为了获得纯净的[Co(NH3)6]Cl3。设计由步骤II过滤后的滤渣获取[Co(NH3)6]Cl3的实验方案:向滤渣中加入80℃左右的热水,充分搅拌后,
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】实验探究是化学学科的重要特征。
Ⅰ.根据下列装置图,回答有关问题:
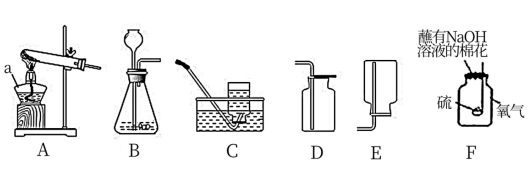
(1)a仪器的名称是________ 。
(2)如用装置A制取氧气,其反应的化学方程式为_______________________________ ;如用装置B制取氧气,往长颈漏斗中倒入的液体药品是__________ ;如用装置D收集氧气,则验满的方法是_____________________________ 。
(3)小明用装置F做硫在氧气中燃烧的实验,该改进实验最大优点是________________ 。
Ⅱ.粗盐提纯中得到的“精盐”常还含有可溶性杂质(假设只有CaCl2一种),为得到更纯净的氯化钠,同学们做了如下处理:
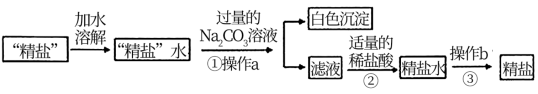
(1)操作b的名称是_________ 。
(2)步骤①加入过量的Na2CO3溶液的目的是________________ 。
(3)步骤②反应的化学方程式:___________________________ 。
(4)如何证明经过步骤②后过量的Na2CO3已除尽?_________________________ (写出实验操作、现象、结论)。
(5)若不考虑损耗,经过上述处理得到的精盐质量_______ (填“大于”、“小于”或“等于”)原“精盐”质量,原因是__________________________________________________ 。
Ⅰ.根据下列装置图,回答有关问题:

(1)a仪器的名称是
(2)如用装置A制取氧气,其反应的化学方程式为
(3)小明用装置F做硫在氧气中燃烧的实验,该改进实验最大优点是
Ⅱ.粗盐提纯中得到的“精盐”常还含有可溶性杂质(假设只有CaCl2一种),为得到更纯净的氯化钠,同学们做了如下处理:

(1)操作b的名称是
(2)步骤①加入过量的Na2CO3溶液的目的是
(3)步骤②反应的化学方程式:
(4)如何证明经过步骤②后过量的Na2CO3已除尽?
(5)若不考虑损耗,经过上述处理得到的精盐质量
您最近一年使用:0次



