实验探究是化学学科的重要特征。
Ⅰ.根据下列装置图,回答有关问题:
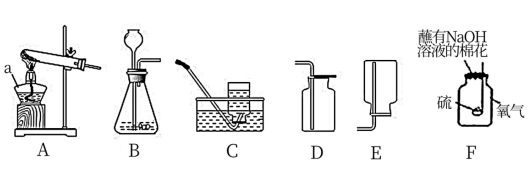
(1)a仪器的名称是________ 。
(2)如用装置A制取氧气,其反应的化学方程式为_______________________________ ;如用装置B制取氧气,往长颈漏斗中倒入的液体药品是__________ ;如用装置D收集氧气,则验满的方法是_____________________________ 。
(3)小明用装置F做硫在氧气中燃烧的实验,该改进实验最大优点是________________ 。
Ⅱ.粗盐提纯中得到的“精盐”常还含有可溶性杂质(假设只有CaCl2一种),为得到更纯净的氯化钠,同学们做了如下处理:
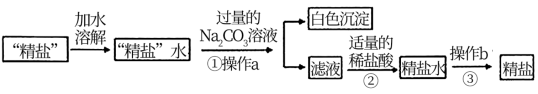
(1)操作b的名称是_________ 。
(2)步骤①加入过量的Na2CO3溶液的目的是________________ 。
(3)步骤②反应的化学方程式:___________________________ 。
(4)如何证明经过步骤②后过量的Na2CO3已除尽?_________________________ (写出实验操作、现象、结论)。
(5)若不考虑损耗,经过上述处理得到的精盐质量_______ (填“大于”、“小于”或“等于”)原“精盐”质量,原因是__________________________________________________ 。
Ⅰ.根据下列装置图,回答有关问题:

(1)a仪器的名称是
(2)如用装置A制取氧气,其反应的化学方程式为
(3)小明用装置F做硫在氧气中燃烧的实验,该改进实验最大优点是
Ⅱ.粗盐提纯中得到的“精盐”常还含有可溶性杂质(假设只有CaCl2一种),为得到更纯净的氯化钠,同学们做了如下处理:

(1)操作b的名称是
(2)步骤①加入过量的Na2CO3溶液的目的是
(3)步骤②反应的化学方程式:
(4)如何证明经过步骤②后过量的Na2CO3已除尽?
(5)若不考虑损耗,经过上述处理得到的精盐质量
更新时间:2018-09-19 15:57:07
|
相似题推荐
【推荐1】碱式硫酸铁[Fe(OH)SO4]是黄褐色固体,常用作媒染剂和净水剂。一种利用废铁屑(含少量 Al、Al2O3、Fe2O3等杂质)生产碱式硫酸铁的工艺流程如图所示:

已知:①部分金属阳离子生成氢氧化物沉淀时溶液的 pH 如表:
②Fe(OH) 2+发生电离:Fe(OH)2+⇌Fe3++OH-。请回答下列问题:
(1)加入少量 NaHCO3,调节 pH 的范围是_______ 。
(2)“氧化”过程中,发生反应的离子方程式为_______ ;该过程某同学选用稀硝酸代替 H2O2 溶液完成反应, 你认为不足之处是_______ 。
(3)“氧化”过程中,若硫酸加入量过小,容易生成_______ (填化学式)沉淀;若硫酸加入量过大,不利于产品形成,试从平衡移动的角度分析原因是_______ 。
(4)碱式硫酸铁溶于水后产生的 Fe(OH)2+可部分水解生成 Fe2(OH) 聚合离子。该反应的离子方程式为
聚合离子。该反应的离子方程式为_______ 。

已知:①部分金属阳离子生成氢氧化物沉淀时溶液的 pH 如表:
| 金属阳离子 | Fe2+ | Fe3+ | Al3+ |
| 开始沉淀 | 7.5 | 2.3 | 3.4 |
| 沉淀完全 | 9.7 | 3.2 | 4.4 |
②Fe(OH) 2+发生电离:Fe(OH)2+⇌Fe3++OH-。请回答下列问题:
(1)加入少量 NaHCO3,调节 pH 的范围是
(2)“氧化”过程中,发生反应的离子方程式为
(3)“氧化”过程中,若硫酸加入量过小,容易生成
(4)碱式硫酸铁溶于水后产生的 Fe(OH)2+可部分水解生成 Fe2(OH)
 聚合离子。该反应的离子方程式为
聚合离子。该反应的离子方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】食盐是日常生活的必需品,也是重要的化工原料。
(1)粗食盐常含有少量 、
、 、
、 、
、 、
、 等杂质离子,实验室提纯NaCl的流程如下:
等杂质离子,实验室提纯NaCl的流程如下:
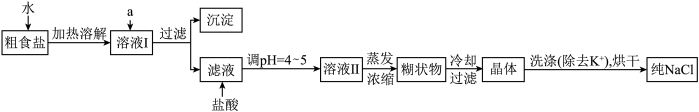
提供的试剂:饱和 溶液、饱和
溶液、饱和 溶液、NaOH溶液、
溶液、NaOH溶液、  溶液、
溶液、 溶液、75%乙醇、四氯化碳
溶液、75%乙醇、四氯化碳
①欲除去溶液Ⅰ中的 、
、 、
、 、
、 离子,选出a所代表的试剂,按滴加顺序依次是
离子,选出a所代表的试剂,按滴加顺序依次是_______ (只填化学式);
②洗涤除去NaCl晶体表面附带的少量KCl,选用的试剂为_______ ;
(2)用提纯的NaCl配制500 mL 4.00 NaCl溶液,所用仪器除药匙、玻璃棒外还有
NaCl溶液,所用仪器除药匙、玻璃棒外还有_______ 。
(3)电解饱和食盐水的装置如图所示,若收集的 为2 L,则同样条件下收集的
为2 L,则同样条件下收集的
_______ (填“>”、“=”或“<”)2 L,原因是_______ ,装置改进后可用于制备NaOH溶液。
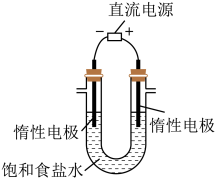
(4)实验室制备 和
和 通常采用下列反应:
通常采用下列反应: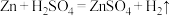 ,
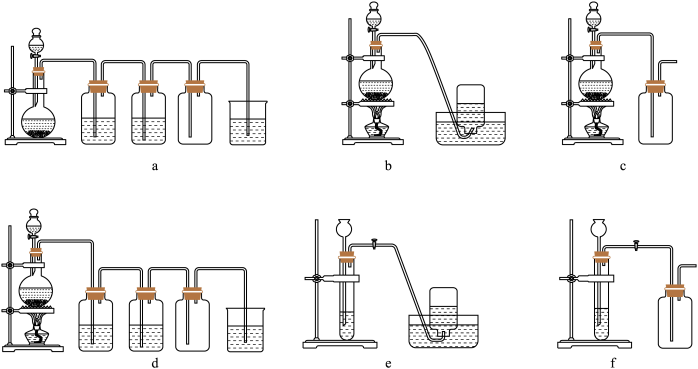
, ,据此,从下列所给仪器装置中选择制备并收集
,据此,从下列所给仪器装置中选择制备并收集 的装置
的装置_______ (填代号)和制备并收集干燥、纯净 的装置
的装置_______ (填代号)。可选用制备气体的装置见上图。
(1)粗食盐常含有少量
 、
、 、
、 、
、 、
、 等杂质离子,实验室提纯NaCl的流程如下:
等杂质离子,实验室提纯NaCl的流程如下:
提供的试剂:饱和
 溶液、饱和
溶液、饱和 溶液、NaOH溶液、
溶液、NaOH溶液、  溶液、
溶液、 溶液、75%乙醇、四氯化碳
溶液、75%乙醇、四氯化碳①欲除去溶液Ⅰ中的
 、
、 、
、 、
、 离子,选出a所代表的试剂,按滴加顺序依次是
离子,选出a所代表的试剂,按滴加顺序依次是②洗涤除去NaCl晶体表面附带的少量KCl,选用的试剂为
(2)用提纯的NaCl配制500 mL 4.00
 NaCl溶液,所用仪器除药匙、玻璃棒外还有
NaCl溶液,所用仪器除药匙、玻璃棒外还有(3)电解饱和食盐水的装置如图所示,若收集的
 为2 L,则同样条件下收集的
为2 L,则同样条件下收集的

(4)实验室制备
 和
和 通常采用下列反应:
通常采用下列反应: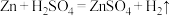 ,
, ,据此,从下列所给仪器装置中选择制备并收集
,据此,从下列所给仪器装置中选择制备并收集 的装置
的装置 的装置
的装置
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】软锰矿的主要成分是 ,其悬浊液可吸收烟气中的
,其悬浊液可吸收烟气中的 ,所得酸性浸出液又可用于制备高纯硫酸锰,其一种工艺流程如下图所示。已知金属单质的活动性顺序为
,所得酸性浸出液又可用于制备高纯硫酸锰,其一种工艺流程如下图所示。已知金属单质的活动性顺序为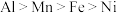 。回答下列问题:
。回答下列问题:

(1)用离子方程式表示加入“氧化剂(软锰矿)”的作用:___________ 。
(2)已知: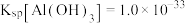 、
、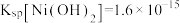 、
、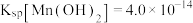 、
、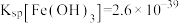 。“水解沉降”中:“中和剂”可以是
。“水解沉降”中:“中和剂”可以是___________ (填标号)。
A. B.
B. C.
C. D.
D.
溶液的 应不低于
应不低于___________ (离子浓度小于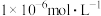 时,即可认为该离子沉淀完全)
时,即可认为该离子沉淀完全)
(3)“置换”的目的是___________ (用离子方程式表示)。
(4)“结晶分离”中的部分物质的溶解度曲线如下图所示。结晶与过滤过程中,体系温度均应维持在___________ (填“27”“60”或“70”)℃。

(5)“草酸钠-高锰酸钾返滴法”可测定软锰矿中 的纯度(假设杂质不参与反应):取ag
的纯度(假设杂质不参与反应):取ag 样品于锥形瓶中,加入适量稀硫酸,再加入
样品于锥形瓶中,加入适量稀硫酸,再加入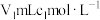
 溶液(足量)发生反应:
溶液(足量)发生反应: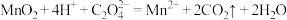 ;最后用
;最后用 的
的 溶液滴定剩余的
溶液滴定剩余的 ,达到终点时消耗
,达到终点时消耗 标准
标准 溶液。该样品中
溶液。该样品中 的质量分数为
的质量分数为___________ (列出表达式即可)。
(6)锰及其化合物应用越来越广泛, 是一种重要的无机功能材料,制备
是一种重要的无机功能材料,制备 的方法之一是以石墨为电极,电解酸化的
的方法之一是以石墨为电极,电解酸化的 溶液,阳极的电极反应式为
溶液,阳极的电极反应式为___________ 。
 ,其悬浊液可吸收烟气中的
,其悬浊液可吸收烟气中的 ,所得酸性浸出液又可用于制备高纯硫酸锰,其一种工艺流程如下图所示。已知金属单质的活动性顺序为
,所得酸性浸出液又可用于制备高纯硫酸锰,其一种工艺流程如下图所示。已知金属单质的活动性顺序为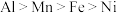 。回答下列问题:
。回答下列问题:
(1)用离子方程式表示加入“氧化剂(软锰矿)”的作用:
(2)已知:
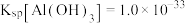 、
、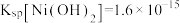 、
、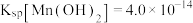 、
、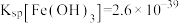 。“水解沉降”中:“中和剂”可以是
。“水解沉降”中:“中和剂”可以是A.
 B.
B. C.
C. D.
D.
溶液的
 应不低于
应不低于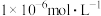 时,即可认为该离子沉淀完全)
时,即可认为该离子沉淀完全)(3)“置换”的目的是
(4)“结晶分离”中的部分物质的溶解度曲线如下图所示。结晶与过滤过程中,体系温度均应维持在

(5)“草酸钠-高锰酸钾返滴法”可测定软锰矿中
 的纯度(假设杂质不参与反应):取ag
的纯度(假设杂质不参与反应):取ag 样品于锥形瓶中,加入适量稀硫酸,再加入
样品于锥形瓶中,加入适量稀硫酸,再加入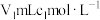
 溶液(足量)发生反应:
溶液(足量)发生反应: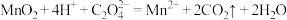 ;最后用
;最后用 的
的 溶液滴定剩余的
溶液滴定剩余的 ,达到终点时消耗
,达到终点时消耗 标准
标准 溶液。该样品中
溶液。该样品中 的质量分数为
的质量分数为(6)锰及其化合物应用越来越广泛,
 是一种重要的无机功能材料,制备
是一种重要的无机功能材料,制备 的方法之一是以石墨为电极,电解酸化的
的方法之一是以石墨为电极,电解酸化的 溶液,阳极的电极反应式为
溶液,阳极的电极反应式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】氨既是一种重要的化工产品,又是一种重要的化工原料。
(1)如图是实验室制取NH3的装置。

①写出装置A中反应的化学方程式_______________________ 。
②若要收集一瓶氨气,请将上述装置B补充完整,在图中虚框内画出连接图_______ 。
③装置C为尾气处理装置,可选用下列中的_______ (填字母)。

(2)如图为工业合成氨以及氨氧化制硝酸的流程示意图。

①写出氧化炉中氨参与反应的化学方程式_______________________________ 。
②流程中B为_________ (填化学式),向吸收塔中通入A的作用为__________ 。
(1)如图是实验室制取NH3的装置。

①写出装置A中反应的化学方程式
②若要收集一瓶氨气,请将上述装置B补充完整,在图中虚框内画出连接图
③装置C为尾气处理装置,可选用下列中的

(2)如图为工业合成氨以及氨氧化制硝酸的流程示意图。

①写出氧化炉中氨参与反应的化学方程式
②流程中B为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】某小组同学用图1所示装置制取氨,并探究其性质。

(1)试管中发生反应的化学方程式是_______ 。
(2)请将方框中的收集装置补充完整______ 。
(3)甲同学设计了图2所示的装置进行尾气处理,乙同学认为该设计不合理,其理由是_______ 。
(4)将蘸有浓盐酸的棉球放在玻璃片上,用集满NH3的集气瓶扣住棉球,可观察到的现象是_______ 。
(5)利用湿润红色石蕊试纸检验氨气是否收集满的方法是(简述操作方法、现象和结论)_______ 。
(6)乙同学认为,上述装置中的NH4Cl和Ca(OH)2固体可用NH4HCO3固体代替制氨气,你认为_______ (填“能”或“不能”) 。

(1)试管中发生反应的化学方程式是
(2)请将方框中的收集装置补充完整
(3)甲同学设计了图2所示的装置进行尾气处理,乙同学认为该设计不合理,其理由是
(4)将蘸有浓盐酸的棉球放在玻璃片上,用集满NH3的集气瓶扣住棉球,可观察到的现象是
(5)利用湿润红色石蕊试纸检验氨气是否收集满的方法是(简述操作方法、现象和结论)
(6)乙同学认为,上述装置中的NH4Cl和Ca(OH)2固体可用NH4HCO3固体代替制氨气,你认为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】二氯化砜(SO2Cl2)是一种重要的有机合成试剂,实验室可利用SO2与Cl2反应制取少量的SO2Cl2。装置如图(有些支持装置省略了)所示。

已知SO2Cl2的熔点为-54.1℃,沸点为69.1℃;常温下比较稳定,受热易分解,遇水能发生剧烈的水解反应,产物之一为氯化氢气体。
(1)E中的试剂是饱和食盐水,戊是贮气装置,则F瓶中气体的实验室制法是_________ (用方程式表示);
(2)B处反应管冷却水应从(填“a”或“b”)接口通入_______ ;
(3)装置乙和丁的作用是____________ ;
(4)恒压漏斗具有特殊的结构,主要目的是___________ ;
(5)写出二氯化砜(SO2Cl2)水解反应的方程式________________ ;
(6)SO2溶于水生成亚硫酸,亚硫酸的酸性强于次氯酸,选用下面的装置和药品探究亚硫酸与次氯酸的酸性强弱:________


装置连接顺序为A、___ 、___ 、___ 、D、F,其中E的作用是______ ,通过_____ 现象即可证明亚硫酸的酸性强于次氯酸。

已知SO2Cl2的熔点为-54.1℃,沸点为69.1℃;常温下比较稳定,受热易分解,遇水能发生剧烈的水解反应,产物之一为氯化氢气体。
(1)E中的试剂是饱和食盐水,戊是贮气装置,则F瓶中气体的实验室制法是
(2)B处反应管冷却水应从(填“a”或“b”)接口通入
(3)装置乙和丁的作用是
(4)恒压漏斗具有特殊的结构,主要目的是
(5)写出二氯化砜(SO2Cl2)水解反应的方程式
(6)SO2溶于水生成亚硫酸,亚硫酸的酸性强于次氯酸,选用下面的装置和药品探究亚硫酸与次氯酸的酸性强弱:


装置连接顺序为A、
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】一化学兴趣小组,探究从某工业废水(含有大量的FeSO4、较多的Cu2+ 和少量的Na+)中回收FeSO4制备绿矾(FeSO4·7H2O),同时回收金属铜的方法,以减少污染并变废为宝。以下是他们设计出的回收流程图,回答有关问题:
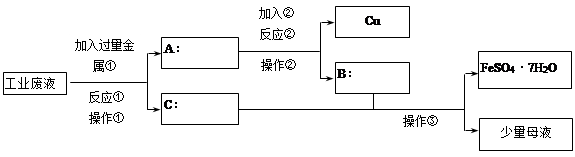
(1)加入的金属①为(填物质名称)______________ ,加入②后反应的离子方程式为_______________________ 。
(2)操作②的名称为_________________ ,用到的玻璃仪器有______________________ 。
(3)反应①和②都是氧化还原反应,写出反应①的离子方程式并用单线桥标出电子转移的方向和数目________________________ 。
(4)母液中含有的离子有(填离子符号):_______________________________ 。

(1)加入的金属①为(填物质名称)
(2)操作②的名称为
(3)反应①和②都是氧化还原反应,写出反应①的离子方程式并用单线桥标出电子转移的方向和数目
(4)母液中含有的离子有(填离子符号):
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】工业上常通过石煤灰渣(主要成分有 、
、 、
、 、
、 、
、 、
、 、
、 、
、 )回收钒的氧化物,有关工艺流程如图:
)回收钒的氧化物,有关工艺流程如图:
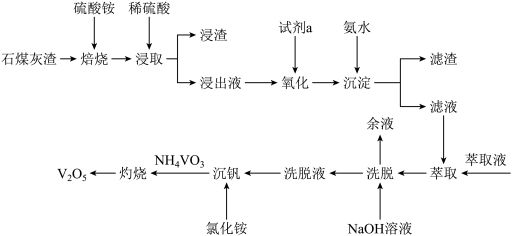
已知:①“焙烧”时,在空气的作用下, 被氧化为
被氧化为 。
。
② 在稀硫酸作用下生成
在稀硫酸作用下生成 。
。
③已知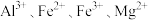 开始生成沉淀和沉淀完全的
开始生成沉淀和沉淀完全的 如表:
如表:
根据所学知识回答下列问题:
(1)在“焙烧”之前,要先将硫酸铵固体和石煤灰进行混磨处理,其目的是_______ 。
(2) 中V的化合价为
中V的化合价为_______ ,“浸渣”的主要成分除了 ,还有
,还有_______ (填化学式)。
(3)“氧化”时加入的试剂a常用 ,写出反应的离子方程式
,写出反应的离子方程式_______ 。 也能氧化
也能氧化 ,工业生产中不选用
,工业生产中不选用 的原因是
的原因是_______ 。
(4)“沉淀”时,控制溶液 在4.5~6.5之间,“滤渣”的主要成分是
在4.5~6.5之间,“滤渣”的主要成分是_______ (填化学式)。
(5)在500℃灼烧脱氨可制得产品 ,写出该反应的化学方程式:
,写出该反应的化学方程式:_______ 。在硫酸酸化条件下, 可与草酸(H2C2O4)溶液反应得到含
可与草酸(H2C2O4)溶液反应得到含 的溶液,写出发生反应的离子方程式:
的溶液,写出发生反应的离子方程式:_______ 。
(6)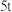 某批次的石煤灰渣中
某批次的石煤灰渣中 的含量为
的含量为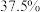 工业生产中钒的漫出率为
工业生产中钒的漫出率为 ,若后续步骤中钒损耗为
,若后续步骤中钒损耗为 ,则理论上制得的
,则理论上制得的 的质量最多为
的质量最多为_______ t(保留三位有效数字)。
 、
、 、
、 、
、 、
、 、
、 、
、 、
、 )回收钒的氧化物,有关工艺流程如图:
)回收钒的氧化物,有关工艺流程如图:
已知:①“焙烧”时,在空气的作用下,
 被氧化为
被氧化为 。
。②
 在稀硫酸作用下生成
在稀硫酸作用下生成 。
。③已知
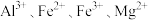 开始生成沉淀和沉淀完全的
开始生成沉淀和沉淀完全的 如表:
如表:| 离子 |  |  |  |  |
开始沉淀 | 2.8 | 8.1 | 1.2 | 9.0 |
完全沉淀 | 4.5 | 9.6 | 3.2 | 11.1 |
(1)在“焙烧”之前,要先将硫酸铵固体和石煤灰进行混磨处理,其目的是
(2)
 中V的化合价为
中V的化合价为 ,还有
,还有(3)“氧化”时加入的试剂a常用
 ,写出反应的离子方程式
,写出反应的离子方程式 也能氧化
也能氧化 ,工业生产中不选用
,工业生产中不选用 的原因是
的原因是(4)“沉淀”时,控制溶液
 在4.5~6.5之间,“滤渣”的主要成分是
在4.5~6.5之间,“滤渣”的主要成分是(5)在500℃灼烧脱氨可制得产品
 ,写出该反应的化学方程式:
,写出该反应的化学方程式: 可与草酸(H2C2O4)溶液反应得到含
可与草酸(H2C2O4)溶液反应得到含 的溶液,写出发生反应的离子方程式:
的溶液,写出发生反应的离子方程式:(6)
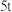 某批次的石煤灰渣中
某批次的石煤灰渣中 的含量为
的含量为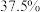 工业生产中钒的漫出率为
工业生产中钒的漫出率为 ,若后续步骤中钒损耗为
,若后续步骤中钒损耗为 ,则理论上制得的
,则理论上制得的 的质量最多为
的质量最多为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】氨基甲酸铵(NH2COONH4)是一种白色固体,易分解、易水解,可用做肥料、灭火剂、洗涤剂等。某化学兴趣小组模拟制备氨基甲酸铵,反应的化学方程式如下:2NH3(g)+CO2(g) NH2COONH4(s)+Q(Q>0)
NH2COONH4(s)+Q(Q>0)
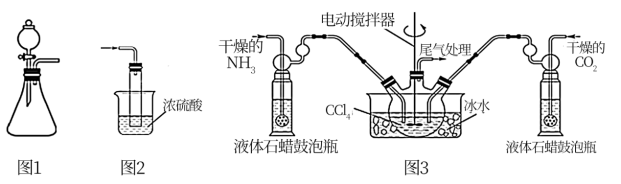
(1)如用图1装置制取氨气,你所选择的试剂是___________ 。制备氨基甲酸铵的装置如图3所示,把氨气和二氧化碳通入四氯化碳中,不断搅拌混合,生成的氨基甲酸铵小晶体悬浮在四氯化碳中。当悬浮物较多时,停止制备。
注:四氯化碳与液体石蜡均为惰性介质。
(2)发生器用冰水冷却的原因是___________ 。
(3)液体石蜡鼓泡瓶的作用是___________ 。
(4)从反应后的混合物中分离出产品的实验方法是___________ (填写操作名称)。为了得到干燥产品,应采取的方法是___________ (填写选项序号)。
a.常压加热烘干b.高压加热烘干c.真空40℃以下烘干
(5)尾气处理装置如图2所示。双通玻璃管的作用:___________ ;浓硫酸的作用:___________ 、___________ 。
(6)取因部分变质而混有碳酸氢铵的氨基甲酸铵样品0.7820g,用足量石灰水充分处理后,使碳元素完全转化为碳酸钙,过滤、洗涤、干燥,测得质量为1.000g.则样品中氨基甲酸铵的物质的量分数为___________ 。[Mr(NH2COONH4)=78、Mr(NH4HCO3)=79、Mr(CaCO3)=100]
 NH2COONH4(s)+Q(Q>0)
NH2COONH4(s)+Q(Q>0)
(1)如用图1装置制取氨气,你所选择的试剂是
注:四氯化碳与液体石蜡均为惰性介质。
(2)发生器用冰水冷却的原因是
(3)液体石蜡鼓泡瓶的作用是
(4)从反应后的混合物中分离出产品的实验方法是
a.常压加热烘干b.高压加热烘干c.真空40℃以下烘干
(5)尾气处理装置如图2所示。双通玻璃管的作用:
(6)取因部分变质而混有碳酸氢铵的氨基甲酸铵样品0.7820g,用足量石灰水充分处理后,使碳元素完全转化为碳酸钙,过滤、洗涤、干燥,测得质量为1.000g.则样品中氨基甲酸铵的物质的量分数为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】某化学兴趣小组欲研究一种镁铝合金,以下是部分实验。请完成填空。
[实验一]从镁铝合金片上剪下一小块,先称重,然后投到盛有10mL 10mol·L-1NaOH溶液(足量)的锥形瓶里。
(1)从反应开始至反应结束,依次可观察到的现象有:①切口断面处先产生气泡,反应由慢到快;②小块合金在溶液中上下翻腾;③溶液升温;④反应后,溶液中残留黑色固体。
(2)开始时产生气泡速率慢,其主要原因(除温度、电化学因素外)是_____________ 。
(3)欲利用此反应测定合金中铝的含量,请仿照方法①写出另一种不同方法所需数据。
[实验二]向实验一的锥形瓶里滴加1 mol·L-1HCl,使镁、铝两种元素恰好只以氯化物的形式存在。
[实验三]请设计合理实验检验实验二所得溶液中的Mg2+、Al3+。
限选实验用品与试剂:烧杯、试管、滴管、1 mol·L-1NaOH溶液、1 mol·L-1HCl溶液、蒸馏水。
根据你设计的实验方案,叙述实验操作、预期现象和结论。(可填满、可不填满)
[实验四]粉末状试样A是由MgO和Fe2O3组成的混合物。取适量A进行铝热反应,产物中有单质B生成。产物中的单质B是______________ (填化学式)。
[实验一]从镁铝合金片上剪下一小块,先称重,然后投到盛有10mL 10mol·L-1NaOH溶液(足量)的锥形瓶里。
(1)从反应开始至反应结束,依次可观察到的现象有:①切口断面处先产生气泡,反应由慢到快;②小块合金在溶液中上下翻腾;③溶液升温;④反应后,溶液中残留黑色固体。
(2)开始时产生气泡速率慢,其主要原因(除温度、电化学因素外)是
(3)欲利用此反应测定合金中铝的含量,请仿照方法①写出另一种不同方法所需数据。
| 方法 | 需测定的数据 |
| ① | 测定产生的H2的体积 |
| ② |
[实验二]向实验一的锥形瓶里滴加1 mol·L-1HCl,使镁、铝两种元素恰好只以氯化物的形式存在。
[实验三]请设计合理实验检验实验二所得溶液中的Mg2+、Al3+。
限选实验用品与试剂:烧杯、试管、滴管、1 mol·L-1NaOH溶液、1 mol·L-1HCl溶液、蒸馏水。
根据你设计的实验方案,叙述实验操作、预期现象和结论。(可填满、可不填满)
| 实验操作 | 预期现象和结论 |
| 步骤1: | |
| 步骤2: | |
| …… |
[实验四]粉末状试样A是由MgO和Fe2O3组成的混合物。取适量A进行铝热反应,产物中有单质B生成。产物中的单质B是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】某化学兴趣小组制取氯酸钾和氯水并进行有关探究实验。
实验一:制取氯酸钾和氯水
利用如图所示的实验装置进行实验。
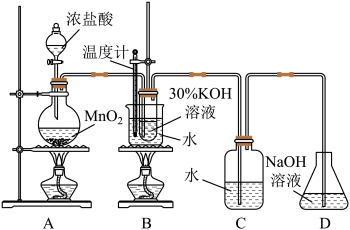
(1)制取实验结束后,取出B中试管冷却结晶、过滤、洗涤。该实验操作过程需要的玻璃仪器有__ 。
(2)若对调B和C装置的位置,__ (填“能”或“不能”)提高B中氯酸钾的产率。
实验二:氯酸钾与碘化钾反应的探究
(3)在不同条件下KClO3可将KI氧化为I2或KIO3。该小组设计了系列实验研究反应条件对反应产物的影响,其中系列a实验的记录表如下(实验在室温下进行):
①系列a实验的实验目的是__ 。
②设计1号试管实验的作用是__ 。
③若2号试管实验现象为“黄色溶液”,取少量该溶液加入淀粉溶液显蓝色;假设氧化产物唯一,还原产物为KCl,则此反应的离子方程式为__ 。
实验三:测定饱和氯水中氯元素的总量
(4)该小组设计的实验方案为:使用如图装置,加热15.0ml饱和氯水试样,测定产生气体的体积。此方案不可行的主要原因是__ 。(不考虑实验装置及操作失误导致不可行的原因)
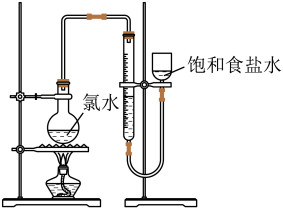
(5)根据下列资料,为该小组设计一个可行的实验方案(不必描述操作过程的细节):__ 。
资料:i.次氯酸会破坏酸碱指示剂;
ii.次氯酸或氯水可被SO2、H2O2、FeCl2等物质还原成Cl-。
实验一:制取氯酸钾和氯水
利用如图所示的实验装置进行实验。

(1)制取实验结束后,取出B中试管冷却结晶、过滤、洗涤。该实验操作过程需要的玻璃仪器有
(2)若对调B和C装置的位置,
实验二:氯酸钾与碘化钾反应的探究
(3)在不同条件下KClO3可将KI氧化为I2或KIO3。该小组设计了系列实验研究反应条件对反应产物的影响,其中系列a实验的记录表如下(实验在室温下进行):
| 试管编号 | 1 | 2 | 3 | 4 |
| 0.20mol·L-1KI/mL | 1.0 | 1.0 | 1.0 | 1.0 |
| KClO3(s)/g | 0.10 | 0.10 | 0.10 | 0.10 |
| 6.0mol·L-1H2SO4/mL | 0 | 3.0 | 6.0 | 9.0 |
| 蒸馏水 | 9.0 | 6.0 | 3.0 | 0 |
| 实验现象 |
②设计1号试管实验的作用是
③若2号试管实验现象为“黄色溶液”,取少量该溶液加入淀粉溶液显蓝色;假设氧化产物唯一,还原产物为KCl,则此反应的离子方程式为
实验三:测定饱和氯水中氯元素的总量
(4)该小组设计的实验方案为:使用如图装置,加热15.0ml饱和氯水试样,测定产生气体的体积。此方案不可行的主要原因是

(5)根据下列资料,为该小组设计一个可行的实验方案(不必描述操作过程的细节):
资料:i.次氯酸会破坏酸碱指示剂;
ii.次氯酸或氯水可被SO2、H2O2、FeCl2等物质还原成Cl-。
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】某研究小组利用下图装置探究温度对CO还原Fe2O3的影响(固定装置略)。
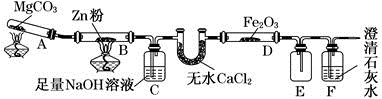
(1)写出MgCO3分解的化学方程式__________________________ 。
(2)装置C的作用是__________________________ ,处理尾气的方法为__________ 。
(3)将研究小组分为两组,按上图装置进行对比实验,甲组用酒精灯、乙组用酒精喷灯对装置D加热,反应产物均为黑色粉末(纯净物)。两组分别用产物进行以下实验:
①乙组得到的黑色粉末是_________ 。
②甲组步骤1中反应的离子方程式为_______________________________________________ 。
③乙组步骤4中,溶液变红的原因为_______________________________________________ 。
④从实验安全考虑,题图装置还可采取的改进措施是________________________________ 。

(1)写出MgCO3分解的化学方程式
(2)装置C的作用是
(3)将研究小组分为两组,按上图装置进行对比实验,甲组用酒精灯、乙组用酒精喷灯对装置D加热,反应产物均为黑色粉末(纯净物)。两组分别用产物进行以下实验:
| 步骤 | 操作 | 甲组现象 | 乙组现象 |
| 1 | 取黑色粉末加入稀盐酸 | 溶解,无气泡 | 溶解,有气泡 |
| 2 | 取步骤1中溶液,滴加K3[Fe(CN)6]溶液 | 蓝色沉淀 | 蓝色沉淀 |
| 3 | 取步骤1中溶液,滴加KSCN溶液 | 变红 | 无现象 |
| 4 | 向步骤3溶液中滴加新制氯水 | 红色褪去 | 先变红,后褪色 |
①乙组得到的黑色粉末是
②甲组步骤1中反应的离子方程式为
③乙组步骤4中,溶液变红的原因为
④从实验安全考虑,题图装置还可采取的改进措施是
您最近一年使用:0次



