运用化学反应原理研究合成氨反应有重要意义,请完成下列探究。
生产氢气:将水蒸气通过红热的炭即产生水煤气,其反应为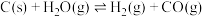
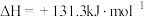 ,
,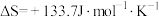
(1)试判断该反应在常温下能否自发进行_________ 。(写出计算过程)
(2)写出该反应的平衡常数表达式___________ 。
生产氢气:将水蒸气通过红热的炭即产生水煤气,其反应为
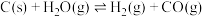
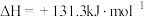 ,
,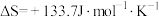
(1)试判断该反应在常温下能否自发进行
(2)写出该反应的平衡常数表达式
更新时间:2024-05-05 22:51:01
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】合成氨是人类科技发展史上的一项重大突破,已知:25℃时,合成氨反应的热化学为:N2(g)+3H2(g) ⇌2NH3(g) ΔH=-92.4kJ/mol,请回答下列问题:
(1)其他条件不变时,升高温度,化学反应速率_____ (填“增大”或“减小”);
(2)25℃时,取1mol N2和3mol H2置于2L的密闭容器中,在催化剂存在下进行反应,达到平衡时放出的热量_____
A.大于92.4 kJ B.等于92.4 kJ C.小于92.4 kJ
(3)一定条件下,上述反应达到化学平衡状态的标志是_______ ;
A.N2、H2、NH3的浓度相等
B.容器内压强不再变化
C.单位时间内消耗amol N2,同时生成2amol NH3
(4)25℃时,上述反应平衡常数的表达式为:K=_______ 。
(1)其他条件不变时,升高温度,化学反应速率
(2)25℃时,取1mol N2和3mol H2置于2L的密闭容器中,在催化剂存在下进行反应,达到平衡时放出的热量
A.大于92.4 kJ B.等于92.4 kJ C.小于92.4 kJ
(3)一定条件下,上述反应达到化学平衡状态的标志是
A.N2、H2、NH3的浓度相等
B.容器内压强不再变化
C.单位时间内消耗amol N2,同时生成2amol NH3
(4)25℃时,上述反应平衡常数的表达式为:K=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】SO2的含量是衡量大气污染的一个重要指标。工业上常采用催化还原法或吸收法处理SO2。利用催化还原SO2法不仅可消除SO2污染,而且可得到有经济价值的单质S。
(1)在复合组分催化剂作用下,CH4可使SO2转化为S,同时生成CO2和液态H2O。已知CH4和S的燃烧热(ΔH)分别为-890.3 kJ/mol和-297.2 kJ/mol,则CH4和SO2反应的热化学方程式为_________________ 。
(2)在恒容密闭容器中,用H2还原SO2生成S的反应分两步完成(如图1所示),该过程中相关物质的物质的量浓度随时间的变化关系如图2所示:

①分析可知X为___________ (填化学式),0~t1时间段的温度为_____________ ,0~t1时间段用SO2表示的化学反应速率为_________________ 。
②用H2还原SO2生成S的总反应的化学方程式为__________________ 。
(3)焦炭催化还原SO2生成S2,化学方程式为2C(s)+2SO2(g)⇌S2(g)+2CO2(g),恒容密闭容器中,1 mol/L SO2与足量的焦炭反应,SO2的转化率随温度的变化如图3所示。
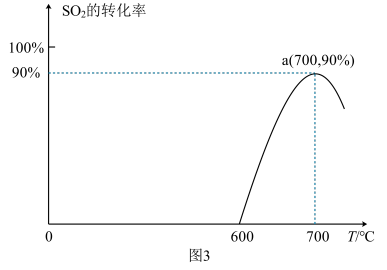
①该反应的ΔH_______ (填“>”或“<”)0。
②计算a点的平衡常数为______________ 。
(1)在复合组分催化剂作用下,CH4可使SO2转化为S,同时生成CO2和液态H2O。已知CH4和S的燃烧热(ΔH)分别为-890.3 kJ/mol和-297.2 kJ/mol,则CH4和SO2反应的热化学方程式为
(2)在恒容密闭容器中,用H2还原SO2生成S的反应分两步完成(如图1所示),该过程中相关物质的物质的量浓度随时间的变化关系如图2所示:

①分析可知X为
②用H2还原SO2生成S的总反应的化学方程式为
(3)焦炭催化还原SO2生成S2,化学方程式为2C(s)+2SO2(g)⇌S2(g)+2CO2(g),恒容密闭容器中,1 mol/L SO2与足量的焦炭反应,SO2的转化率随温度的变化如图3所示。

①该反应的ΔH
②计算a点的平衡常数为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】丙烯和氨分别是重要的有机和无机化工原料。丙烯主要用于生产聚丙烯、丙烯腈、环氧丙烷等。“丁烯裂解法”是一种重要的丙烯生产法,生产过程中会有生成乙烯的副反应发生。反应如下:
主反应: ;
;
副反应: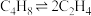 。
。
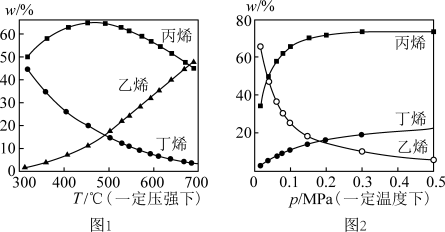
测得上述两反应的平衡体系中,各组分的质量分数(w%)随温度(T)和压强(p)变化的趋势分别如图1和图2所示:
(1)在10L恒容密闭容器中,投入1mol丁烯,在一定温度下进行反应,5分钟后测得体系压强变为开始时的1.2倍,乙烯0.1mol,则以丙烯表示的主反应的速率为___________ 。
(2)主反应的平衡常数表达式
___________ ,如果反应的平衡常数K值变大,该反应___________ (选填编号)。
a.一定向正反应方向移动 b.平衡移动时,正反应速率先减小后增大
c.一定向逆反应方向移动 d.平衡移动时,逆反应速率先增大后减小
(3)平衡体系中的丙烯和乙烯的质量比 是工业生产丙烯时选择反应条件的重要指标之一,从产物的纯度考虑,该数值越高越好,从图1和图2中表现的趋势来看,下列反应条件最适宜的是___________(填字母)。
是工业生产丙烯时选择反应条件的重要指标之一,从产物的纯度考虑,该数值越高越好,从图1和图2中表现的趋势来看,下列反应条件最适宜的是___________(填字母)。
(4)有研究者结合图1数据并综合考虑各种因素,认为450℃的反应温度比300℃或700℃更合适,从反应原理角度分析其理由可能是___________ 。
(5)图2中,随压强增大,平衡体系中丙烯的质量分数呈上升趋势,从平衡角度解释其原因是___________ 。
主反应:
 ;
; 副反应:
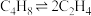 。
。测得上述两反应的平衡体系中,各组分的质量分数(w%)随温度(T)和压强(p)变化的趋势分别如图1和图2所示:

(1)在10L恒容密闭容器中,投入1mol丁烯,在一定温度下进行反应,5分钟后测得体系压强变为开始时的1.2倍,乙烯0.1mol,则以丙烯表示的主反应的速率为
(2)主反应的平衡常数表达式

a.一定向正反应方向移动 b.平衡移动时,正反应速率先减小后增大
c.一定向逆反应方向移动 d.平衡移动时,逆反应速率先增大后减小
(3)平衡体系中的丙烯和乙烯的质量比
 是工业生产丙烯时选择反应条件的重要指标之一,从产物的纯度考虑,该数值越高越好,从图1和图2中表现的趋势来看,下列反应条件最适宜的是___________(填字母)。
是工业生产丙烯时选择反应条件的重要指标之一,从产物的纯度考虑,该数值越高越好,从图1和图2中表现的趋势来看,下列反应条件最适宜的是___________(填字母)。A.300℃  | B.700℃  |
C.300℃ 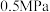 | D.700℃ 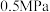 |
(5)图2中,随压强增大,平衡体系中丙烯的质量分数呈上升趋势,从平衡角度解释其原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
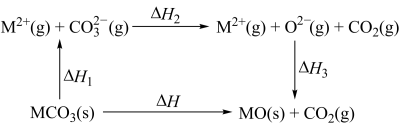
【推荐1】在煤炭中加入碳酸钙可减少酸雨的形成。在研究碳酸盐分解时发现MgCO3和CaCO3的能量关系如图所示(M=Ca、Mg),ΔH表达式为___________ ;已知CaCO3(s)=CaO(s)+CO2(g)ΔH>0,则该反应能自发进行的条件是___________ 。___________ 。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】在化学反应A(g)+B(g) 2C(g)+D(g) ΔH=Q kJ·mol-1过程中的能量变化如图所示,回答下列问题。
2C(g)+D(g) ΔH=Q kJ·mol-1过程中的能量变化如图所示,回答下列问题。

(1)Q___________ 0 (填“>”“<”或“=”)。
(2)熵变ΔS___________ 0(填“>”“<”或“=”)。
(3)该反应___________ 自发进行(填“能”或“不能”)。
(4)升高温度,平衡常数K___________ (填“增大”“减小”或“不变”),平衡向___________ 方向移动,平衡向该方向移动的理由是___________ 。
 2C(g)+D(g) ΔH=Q kJ·mol-1过程中的能量变化如图所示,回答下列问题。
2C(g)+D(g) ΔH=Q kJ·mol-1过程中的能量变化如图所示,回答下列问题。
(1)Q
(2)熵变ΔS
(3)该反应
(4)升高温度,平衡常数K
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】正确判断反应自发进行的方向对于生产实践具有重要的意义。回答下列问题:
(1)用钌的配合物作催化剂,一定条件下可直接光催化分解 ,发生反应:
,发生反应: 。该反应的
。该反应的
___________ (填“>”、“<”或“=”,下同)0,
___________ 0,在低温下,该反应___________ (填“能”或“不能”)自发进行。
(2)超音速飞机在平流层飞行时,尾气中的 会破坏臭氧层。科学家正在研究利用催化技术将尾气中的
会破坏臭氧层。科学家正在研究利用催化技术将尾气中的 和
和 转变成
转变成 和
和 ,反应的方程式为
,反应的方程式为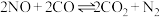 。反应在常温下能够自发进行,则反应的
。反应在常温下能够自发进行,则反应的
___________ (填“>”、“<”或“=”)0。
(3)某吸热反应能自发进行,则该反应的
___________ (填“>”或“<”)0。
(1)用钌的配合物作催化剂,一定条件下可直接光催化分解
 ,发生反应:
,发生反应: 。该反应的
。该反应的

(2)超音速飞机在平流层飞行时,尾气中的
 会破坏臭氧层。科学家正在研究利用催化技术将尾气中的
会破坏臭氧层。科学家正在研究利用催化技术将尾气中的 和
和 转变成
转变成 和
和 ,反应的方程式为
,反应的方程式为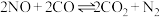 。反应在常温下能够自发进行,则反应的
。反应在常温下能够自发进行,则反应的
(3)某吸热反应能自发进行,则该反应的

您最近一年使用:0次



