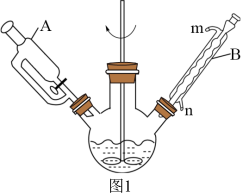
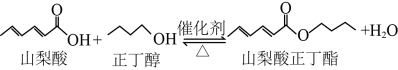
山梨酸酯具有解毒作用,可以减轻肝脏负担,促进肝细胞修复,保护肝脏健康。实验室用如图1所示装置(夹持、加热装置省略),依据下面的原理制备山梨酸正丁酯。
实验步骤:
①在三颈烧瓶中加入16.8g山梨酸、7.4g正丁醇、少量催化剂和几粒沸石,水浴加热三颈烧瓶,使反应体系保持微沸。
②回流4小时后停止加热和搅拌,反应液冷却至室温。
③滤去催化剂和沸石,将滤液倒入200mL水中,加入50mL乙醚,倒入分液漏斗中,分液。
④分离出的有机层先用ρ=10mg/L的NaHCO3溶液洗涤至中性,再用水洗涤分液,收集有机层。
⑤在有机层中加入少量无水MgSO4,静置片刻,过滤。
⑥将滤液进行蒸馏,除去杂质得到纯净的山梨酸正丁酯6.0g。
回答下列问题:
(1)仪器A的名称是___________ ;冷却水由___________ (填“m”或“n”)口通入。
(2)洗涤、分液过程中,加入ρ=10mg/L的NaHCO3溶液的目的是___________ 。
(3)在实验步骤④中加入少量无水MgSO₄的目的是___________ 。
(4)在实验步骤⑥中进行蒸馏,蒸馏至120℃除去的杂质是___________ 。
(5)本实验中,山梨酸正丁酯的产率是___________ (精确至0.1%)。
(6)为了提高反应正向进行的程度,实验室常使用如图2所示装置(夹持、加热装置已略去)代替图1装置制备山梨酸正丁酯以提高产物的产率,请结合环己烷的物理性质,解释在该装置中环己烷的主要作用___________ 。
| 物质 | 相对分子质量 | 密度/(g·cm-3) | 沸点/℃ | 水溶性 |
| 山梨酸 | 112 | 1.204 | 228 | 易溶 |
| 正丁醇 | 74 | 0.8089 | 117 | 溶 |
| 山梨酸正丁酯 | 168 | 0.926 | 195 | 难溶 |
| 乙醚 | 74 | 0.714 | 34.6 | 难溶 |
| 环己烷 | 84 | 0.779 | 80.7 | 难溶 |
①在三颈烧瓶中加入16.8g山梨酸、7.4g正丁醇、少量催化剂和几粒沸石,水浴加热三颈烧瓶,使反应体系保持微沸。
②回流4小时后停止加热和搅拌,反应液冷却至室温。
③滤去催化剂和沸石,将滤液倒入200mL水中,加入50mL乙醚,倒入分液漏斗中,分液。
④分离出的有机层先用ρ=10mg/L的NaHCO3溶液洗涤至中性,再用水洗涤分液,收集有机层。
⑤在有机层中加入少量无水MgSO4,静置片刻,过滤。
⑥将滤液进行蒸馏,除去杂质得到纯净的山梨酸正丁酯6.0g。
回答下列问题:
(1)仪器A的名称是
(2)洗涤、分液过程中,加入ρ=10mg/L的NaHCO3溶液的目的是
(3)在实验步骤④中加入少量无水MgSO₄的目的是
(4)在实验步骤⑥中进行蒸馏,蒸馏至120℃除去的杂质是
(5)本实验中,山梨酸正丁酯的产率是
(6)为了提高反应正向进行的程度,实验室常使用如图2所示装置(夹持、加热装置已略去)代替图1装置制备山梨酸正丁酯以提高产物的产率,请结合环己烷的物理性质,解释在该装置中环己烷的主要作用

更新时间:2024-05-06 14:32:21
|
相似题推荐
【推荐1】已知葡萄糖在乳酸菌作用下可转化为乳酸(C3H6O3)。
(1)取9g乳酸与足量的金属Na反应,可生成2.24LH2(标准状况),另取等量乳酸与等物质的量的乙醇反应,生成0.1mol乳酸乙酯和1.8g水,由此可推断乳酸分子中含有的官能团名称为____________ 。
(2)乳酸在Cu作催化剂时可被氧化成丙酮酸(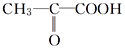 ),由以上事实推知乳酸的结构简式为
),由以上事实推知乳酸的结构简式为________________ 。
(3)两个乳酸分子在一定条件下脱水生成环脂(C6H8O4),则此环酯的结构简式是____ 。
(4)乳酸在浓H2SO4作用下,三分子相互反应,生成链状结构的物质,写出其生成物的结构简式:___________________________________________________________ 。
(1)取9g乳酸与足量的金属Na反应,可生成2.24LH2(标准状况),另取等量乳酸与等物质的量的乙醇反应,生成0.1mol乳酸乙酯和1.8g水,由此可推断乳酸分子中含有的官能团名称为
(2)乳酸在Cu作催化剂时可被氧化成丙酮酸(
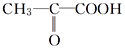 ),由以上事实推知乳酸的结构简式为
),由以上事实推知乳酸的结构简式为(3)两个乳酸分子在一定条件下脱水生成环脂(C6H8O4),则此环酯的结构简式是
(4)乳酸在浓H2SO4作用下,三分子相互反应,生成链状结构的物质,写出其生成物的结构简式:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】已知苯甲酸微溶于水,易溶于乙醇、乙醚,有弱酸性,酸性比醋酸强,它可用于制备苯甲酸乙酯。
制备苯甲酸乙酯的反应原理:
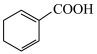 +C2H5OH
+C2H5OH
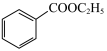 +H2O
+H2O
相关物质的部分物理性质如表格:
实验流程如图:

(1)制备苯甲酸乙酯,如图装置最合适的是___ ,反应液中的环己烷在本实验中的作用__ 。
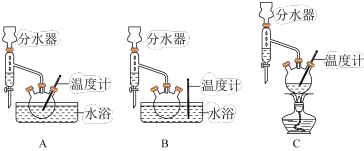
(2)步骤②控制温度在65~70℃缓慢加热液体回流,分水器中逐渐出现上、下两层液体,直到反应完成,停止加热。放出分水器中的下层液体后,继续加热,蒸出多余的乙醇和环己烷。反应完成的标志是____ 。
(3)步骤③碳酸钠的作用是___ ,碳酸钠固体需搅拌下分批加入的原因____ 。
(4)步骤④将中和后的液体转入分液漏斗分出有机层,水层用25mL乙醚萃取,然后合并至有机层,用无水MgSO4干燥。乙醚的作用___ 。
(5)步骤⑤蒸馏操作中,通常先低温蒸出乙醚,蒸馏乙醚时最好采用___ (水浴加热、直接加热、油浴加热)。
(6)最终得到5.45g纯品,则苯甲酸乙酯的产率是___ 。(保留3位有效数字)
制备苯甲酸乙酯的反应原理:
 +C2H5OH
+C2H5OH
 +H2O
+H2O相关物质的部分物理性质如表格:
| 沸点/℃ | 密度/g•cm-3 | |
| 苯甲酸 | 249 | 1.2659 |
| 苯甲酸乙酯 | 212.6 | 1.05 |
| 乙醇 | 78.5 | 0.7893 |
| 环己烷 | 80.8 | 0.7785 |
| 乙醚 | 34.51 | 0.7318 |
| 环己烷、乙醇和水共沸物 | 62.1 |

(1)制备苯甲酸乙酯,如图装置最合适的是

(2)步骤②控制温度在65~70℃缓慢加热液体回流,分水器中逐渐出现上、下两层液体,直到反应完成,停止加热。放出分水器中的下层液体后,继续加热,蒸出多余的乙醇和环己烷。反应完成的标志是
(3)步骤③碳酸钠的作用是
(4)步骤④将中和后的液体转入分液漏斗分出有机层,水层用25mL乙醚萃取,然后合并至有机层,用无水MgSO4干燥。乙醚的作用
(5)步骤⑤蒸馏操作中,通常先低温蒸出乙醚,蒸馏乙醚时最好采用
(6)最终得到5.45g纯品,则苯甲酸乙酯的产率是
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
解题方法
【推荐3】有机物A最早发现于酸牛奶中,它是人体内糖代谢的中间体,可由马铃薯、玉米、淀粉等发酵制得,A的钙盐是人们喜爱的补钙剂之一。在浓硫酸存在下,A可发生如图所示的反应。
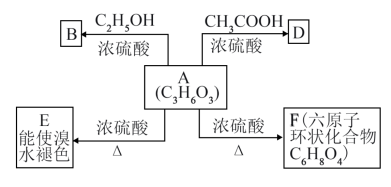
已知:
①通过红外光谱法测得A中含有-OH和-COOH。
②A的核磁共振氢谱图显示四组峰,峰面积之比为1:1:1:3。
回答下面问题:
(1)写出有机物A的结构简式_______ 。
(2)有机物E中官能团的名称_______ ,有机物B和有机物D中含有的相同官能团的名称_______ 。
(3)有机物D的结构简式_______ ,有机物B和有机物D_______ (“是”或“不是”)同分异构体。
(4)有机物A生成D的反应类型是_______ ,有机物A生成E的反应类型是_______ 。
(5)写出有机物A生成F的化学方程式_______ 。
(6)有机物E和有机物B在浓硫酸加热条件下也能发生酯化反应,写出反应的化学方程式_______ 。

已知:
①通过红外光谱法测得A中含有-OH和-COOH。
②A的核磁共振氢谱图显示四组峰,峰面积之比为1:1:1:3。
回答下面问题:
(1)写出有机物A的结构简式
(2)有机物E中官能团的名称
(3)有机物D的结构简式
(4)有机物A生成D的反应类型是
(5)写出有机物A生成F的化学方程式
(6)有机物E和有机物B在浓硫酸加热条件下也能发生酯化反应,写出反应的化学方程式
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】高铝粉煤灰提取铝既能缓解我国缺铝矿的现状,又能减少煤燃烧产生的污染。高铝粉煤灰含48.00% Al2O3、39.70% SiO2、5.08% CaO、2.09% Fe2O3和5.03%其他杂质。活化焙烧法从高铝粉煤灰中提取铝的工艺流程如图所示,回答下列问题:
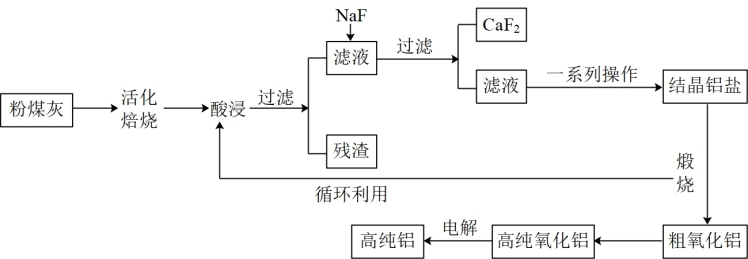
(1)碱石灰烧结法是利用高铝粉煤灰与纯碱1220℃烧结,Al2O3转化为易溶的偏铝酸钠,从而将铝元素分离出来,烧结过程无污染,氧化铝发生反应的化学方程式是_______ 。
(2)活化焙烧过程中,不同活化剂对铝、钙浸出率的影响不同(如下表),应选择_______ 做活化剂。
(3)①酸浸使用的酸是盐酸,酸的浓度与氧化铝溶出率的关系如图1,酸浓度为36%时达到最大溶出率,但实际工业使用32%的酸浓度,原因是_______ 。②酸溶温度与氧化铝溶出率的关系如图2,选择的最佳温度是_______ 。

(4)①流程图中的一系列操作应包括_______ 、过滤、洗涤、干燥;
②粗氧化铝中的主要杂质是_______ 。
(5)现有102 t高铝粉煤灰,如果总转化率为75%,可以得到_______ t铝(计算结果保留4位有效数字)。

(1)碱石灰烧结法是利用高铝粉煤灰与纯碱1220℃烧结,Al2O3转化为易溶的偏铝酸钠,从而将铝元素分离出来,烧结过程无污染,氧化铝发生反应的化学方程式是
(2)活化焙烧过程中,不同活化剂对铝、钙浸出率的影响不同(如下表),应选择
| 活化剂 | Na3PO4 | Na2HPO4 | NaF | Na2SO4 | CH3COONa |
| Al浸出率 | 83.82% | 83.62% | 85.64% | 77.55% | 90.96% |
| Ca浸出率 | 97.10% | 97.75% | 98.26% | 96.79% | 90.96% |
(3)①酸浸使用的酸是盐酸,酸的浓度与氧化铝溶出率的关系如图1,酸浓度为36%时达到最大溶出率,但实际工业使用32%的酸浓度,原因是

(4)①流程图中的一系列操作应包括
②粗氧化铝中的主要杂质是
(5)现有102 t高铝粉煤灰,如果总转化率为75%,可以得到
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】实验室中制备对氯苯甲酸的反应以及装置如图所示:
 ;
;

常温下,物质的有关数据和性质如表所示:
实验步骤:在规格为250mL的仪器A中加入一定量的催化剂、适量KMnO4、100mL水;安装好装置,在滴液漏斗中加入6.00mL对氯甲苯,在温度为93℃左右时,逐滴滴入对氯甲苯;控制温度在93℃左右,反应2h,过滤,将滤渣用热水洗涤,使洗涤液与滤液合并,加入稀硫酸酸化,加热浓缩,冷却,然后过滤,将滤渣用冷水进行洗涤,干燥后称量其质量。
请回答下列问题:
(1)仪器A的名称为___________ 。
(2)实验过程中,对仪器B和电炉的正确操作是:_________ 。
(3)实验过程中两次过滤、洗涤操作,第一次过滤的滤渣成分为___________ (填化学式),第二次过滤后,洗涤滤渣用冷水,目的是___________ 。
(4)过滤、洗涤操作中能用到的仪器是___________ (填选项字母)。
a.烧杯 b.分液漏斗 c.锥形瓶 d.玻璃棒
(5)第一次过滤后的滤液中加入硫酸,出现的现象是___________ 。
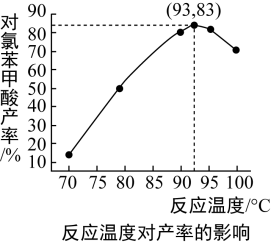
(6)如图是温度对对氯苯甲酸产率的影响关系,最后干燥、称量得到的对氯苯甲酸的质量为___________ (保留小数点后两位)。
 ;
;

常温下,物质的有关数据和性质如表所示:
| 熔点/℃ | 沸点/℃ | 密度/g·cm-3 | 颜色 | 水溶性 | ||
| 对氯甲苯 | 7.5 | 162 | 1.07 | 无色 | 难溶 | |
| 对氯苯甲酸 | 243 | 275 | 1.54 | 白色 | 微溶 | |
| 对氯苯甲酸钾 | 具有盐的通性,属于可溶性盐 | |||||
请回答下列问题:
(1)仪器A的名称为
(2)实验过程中,对仪器B和电炉的正确操作是:
(3)实验过程中两次过滤、洗涤操作,第一次过滤的滤渣成分为
(4)过滤、洗涤操作中能用到的仪器是
a.烧杯 b.分液漏斗 c.锥形瓶 d.玻璃棒
(5)第一次过滤后的滤液中加入硫酸,出现的现象是
(6)如图是温度对对氯苯甲酸产率的影响关系,最后干燥、称量得到的对氯苯甲酸的质量为

您最近一年使用:0次
【推荐3】钛被称为“二十一世纪金属”,工业上用钛铁矿制备金属钛的工艺流程如下:

请回答下列问题:
(1)铁在元素周期表中的位置为______________________ 。
(2)写出TiO2+水解的离子方程式:_________________________________________ 。
加入过量铁粉的作用是:①__________________ ;②______________________ 。
(3)操作 Ⅰ的实验步骤为:___________________ ,过滤。
(4)副产品主要成分的化学式为_________________ 。
(5)写出TiO2转化成TiCl4的化学方程式:__________________________________ 。

请回答下列问题:
(1)铁在元素周期表中的位置为
(2)写出TiO2+水解的离子方程式:
加入过量铁粉的作用是:①
(3)操作 Ⅰ的实验步骤为:
(4)副产品主要成分的化学式为
(5)写出TiO2转化成TiCl4的化学方程式:
您最近一年使用:0次



