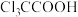对下列事实的解释不正确的是
选项 | 事实 | 解释 |
A | 稳定性:HF>HI | HF分子间存在氢键,HI分子间不存在氢键 |
B | 键角: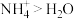 |  中O的,孤电子对数比 中O的,孤电子对数比 中N的孤电子对数多,孤电子对有较大的斥力 中N的孤电子对数多,孤电子对有较大的斥力 |
C | 熔点:石英>干冰 | 石英是共价晶体,干冰是分子晶体;共价键化分子间作用力强 |
D | 酸性: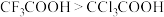 | F的电负性大于Cl, 的极性大 的极性大 ,使 ,使 —的极性大于 —的极性大于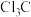 —的极性,从而使 —的极性,从而使 中 中 的极性大于 的极性大于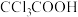 中 中 的极性 的极性 |
| A.A | B.B | C.C | D.D |
更新时间:2024-05-07 19:24:54
|
相似题推荐
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】25°C时,向10mL0.10mol/L的H3PO2溶液中逐滴加入0.10mol/LNaOH溶液,整个滴定过程中溶液的pH随加入NaOH溶液体积的变化关系如图所示。下列说法不正确的是
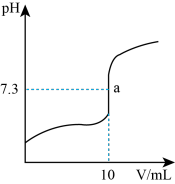

| A.H3PO2是一元弱酸 |
B.NaH2PO2溶液离子浓度: c(Na+)>c(H2PO )>c(OH- )>c(H+) )>c(OH- )>c(H+) |
C.a点: c(H2PO )+c(H3PO2) < c(Na+) )+c(H3PO2) < c(Na+) |
| D.NaH2PO2 水解平衡常数为Kh=2×10-12.4 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐2】下列有关说法不正确的是
A.咪唑为平面结构,结构为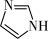 ,N的杂化方式为sp2杂化 ,N的杂化方式为sp2杂化 |
| B.H3AsO4、H3AsO3、H3AsO2三种酸中酸性最强的是H3AsO4 |
| C.某含钛配合物,化学式为[TiCl(H2O)5]Cl2,1mol该配合物中σ键的数目为16NA |
| D.SrCO3和CaCO3受热均可分解,且分解温度:SrCO3< CaCO3 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】镁锑合金因具有极低的本征晶格热导率而成为最具潜质的中文区热电材料之一,Sb位于周期表第五周期VA族, 和
和 均为三角锥形极性分子。一种镁锑合金的六方晶胞结构如图所示,下列有关说法错误的是
均为三角锥形极性分子。一种镁锑合金的六方晶胞结构如图所示,下列有关说法错误的是
 和
和 均为三角锥形极性分子。一种镁锑合金的六方晶胞结构如图所示,下列有关说法错误的是
均为三角锥形极性分子。一种镁锑合金的六方晶胞结构如图所示,下列有关说法错误的是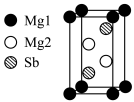
A.该合金的化学式为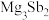 |
| B.Mg和Sb形成合金后,有更好的延展性 |
| C.该合金熔化时,需破坏金属键 |
D. 和 和 相比, 相比, 分子的极性更强,键角更小 分子的极性更强,键角更小 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】硫元素的很多化合物用途广泛。 可用于制杀虫剂、发光漆等。高温下木炭和
可用于制杀虫剂、发光漆等。高温下木炭和 可以反应生成
可以反应生成 。在潮湿的空气中
。在潮湿的空气中 极易发生水解生成硫氢化钙、氢氧化钙和碱式硫氢化钙的混合物。
极易发生水解生成硫氢化钙、氢氧化钙和碱式硫氢化钙的混合物。 与
与 反应可以释放出
反应可以释放出 。
。 能与
能与 溶液发生复分解反应生成黑色
溶液发生复分解反应生成黑色 沉淀。
沉淀。 的水溶液暴露在空气中,因缓慢氧化生成硫而变浑浊。下列有关说法正确的是
的水溶液暴露在空气中,因缓慢氧化生成硫而变浑浊。下列有关说法正确的是
 可用于制杀虫剂、发光漆等。高温下木炭和
可用于制杀虫剂、发光漆等。高温下木炭和 可以反应生成
可以反应生成 。在潮湿的空气中
。在潮湿的空气中 极易发生水解生成硫氢化钙、氢氧化钙和碱式硫氢化钙的混合物。
极易发生水解生成硫氢化钙、氢氧化钙和碱式硫氢化钙的混合物。 与
与 反应可以释放出
反应可以释放出 。
。 能与
能与 溶液发生复分解反应生成黑色
溶液发生复分解反应生成黑色 沉淀。
沉淀。 的水溶液暴露在空气中,因缓慢氧化生成硫而变浑浊。下列有关说法正确的是
的水溶液暴露在空气中,因缓慢氧化生成硫而变浑浊。下列有关说法正确的是A. 的空间构型为直线型 的空间构型为直线型 | B. 的价电子排布式为 的价电子排布式为 |
C. 的键角比 的键角比 的大 的大 | D. 中含有 中含有 键 键 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】下列两组命题中,M组命题能用N组命题加以解释的是
| 选项 | M组 | N组 |
| A. |  的稳定性大于 的稳定性大于 |  的分子间作用力更大 的分子间作用力更大 |
| B. | 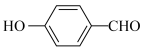 的沸点高于 的沸点高于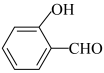 | 因为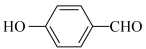 分子间范德华力更大 分子间范德华力更大 |
| C. | 金属具有导热性 | 当金属中存在温度差时,“自由电子”碰撞金属阳离子将能量进行传递 |
| D. | 过氧化氢分子是极性分子 | 过氧化氢分子中只含有极性键 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】化合物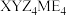 可作肥料,所含的5种元素位于主族,在每个短周期均有分布,仅有Y和M同族。Y的基态原子价层p轨道半充满,X的基态原子价层电子排布式为
可作肥料,所含的5种元素位于主族,在每个短周期均有分布,仅有Y和M同族。Y的基态原子价层p轨道半充满,X的基态原子价层电子排布式为 ,X与M同周期,E在地壳中含量最多。下列说法正确的是
,X与M同周期,E在地壳中含量最多。下列说法正确的是
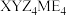 可作肥料,所含的5种元素位于主族,在每个短周期均有分布,仅有Y和M同族。Y的基态原子价层p轨道半充满,X的基态原子价层电子排布式为
可作肥料,所含的5种元素位于主族,在每个短周期均有分布,仅有Y和M同族。Y的基态原子价层p轨道半充满,X的基态原子价层电子排布式为 ,X与M同周期,E在地壳中含量最多。下列说法正确的是
,X与M同周期,E在地壳中含量最多。下列说法正确的是A.元素电负性: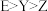 | B.氢化物沸点: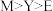 |
C.第一电离能: | D.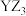 和 和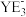 的空间结构均为三角锥形 的空间结构均为三角锥形 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐1】钛被誉为太空金属和亲生物金属,拥有卓越的金属特性。以钛铁矿(主要成分为 ,还含有少量
,还含有少量 )为原料制备钛的流程如图所示,已知
)为原料制备钛的流程如图所示,已知 沸点为136℃。下列说法错误的是
沸点为136℃。下列说法错误的是
 ,还含有少量
,还含有少量 )为原料制备钛的流程如图所示,已知
)为原料制备钛的流程如图所示,已知 沸点为136℃。下列说法错误的是
沸点为136℃。下列说法错误的是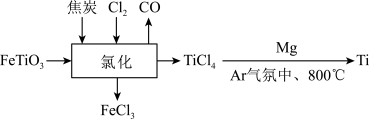
| A.为加快“氯化”速率,可将钛铁矿粉碎并与焦炭混合均匀 |
B.理论上,每制得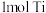 ,需要 ,需要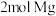 |
C. 固体为分子晶体 固体为分子晶体 |
| D.流程中的Ar气氛换成性质稳定的氮气也可以达到同样效果 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】物质的结构决定其性质,下列与物质的性质对应的解释正确的是
| 选项 | 物质的性质 | 解释 |
| A | 溶解性:乙酸>硬脂酸 | 乙酸分子可与水分子间形成氢键而硬脂酸不能 |
| B | 熔点:氟化铝 氯化铝 氯化铝 | 氟化铝中的离子键强于氯化铝中的离子键 |
| C | 热稳定性: |  的键能比 的键能比 大 大 |
| D | 酸性: | 氮元素的非金属性比硫元素强 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次

 胶体具有吸附性,可用于除去水中的悬浮颗粒物
胶体具有吸附性,可用于除去水中的悬浮颗粒物 分子的极性大于CH4
分子的极性大于CH4 存在3d、4s、4p等多个空轨道,可形成多种配位化合物
存在3d、4s、4p等多个空轨道,可形成多种配位化合物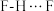 中的氢键键能小于
中的氢键键能小于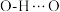 ,因此
,因此 高
高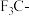 是吸电子基团,
是吸电子基团,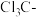 是推电子基团,因此
是推电子基团,因此 的酸性强于
的酸性强于