现有Q、X、Y、Z、W五种前四周期元素,它们的原子序数依次增大。Q原子核外成对电子数和未成对电子数之比为4∶3;X、Z同主族,它们形成的两种化合物中,两元素的原子的质子总数之比分别为1∶1:和2∶3;Y原子半径短周期中最大,W+的K、L、M层电子全充满。下列说法正确的是
| A.HnX的沸点比HnZ的沸点高是因为H-X键长比H-Z键长短,键能更大 |
| B.第一电离能:Q>X>Z |
| C.W2+比W+稳定 |
| D.X与Y形成的化合物中只含一种化学键 |
23-24高二下·安徽池州·期中 查看更多[3]
安徽省池州市贵池区2023-2024学年高二下学期期中教学质量检测化学试题(已下线)期末押题猜想卷02(范围:选择性必修2+3)-2023-2024学年高二化学下学期期末考点大串讲(人教版2019)四川省自贡市荣县中学校2023-2024学年高二下学期5月月考化学试题
更新时间:2024/05/01 20:13:44
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】某原子电子排布式为1s22s22p3,下列说法正确的是
| A.该元素位于第二周期IIIA族 | B.核外有3种能量不同的电子 |
| C.最外层电子占据3个轨道 | D.最外层上有3种运动状态不同的电子 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列各项叙述中,正确的是
| A.镁原子由1s22s22p63s2→1s22s22p63p2时,原子释放能量,由基态转化成激发态 |
| B.价电子排布为5s25p1的元素位于第五周期第ⅠA族,是s区元素 |
| C.硬度:金刚石>晶体硅 |
| D.24Cr原子的电子排布式是1s22s22p63s23p63d44s2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】短周期主族元素X、Y、Z、M、N的原子序数依次增大,其中基态Y原子s能级电子数是p能级的两倍,Z和M位于同一主族,由上述五种元素形成的化合物可作离子导体,结构如图所示。下列说法错误的是


| A.原子半径:M>Y>Z>X | B.非金属性:N>Z>M>Y |
| C.氢化物沸点:Z>N>M>Y | D.同周期中第一电离能小于Z的元素有5种 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】化合物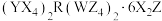 是一种常见补血剂。已知短周期主族元素X、Y、Z、W的原子序数依次增大,X原子半径最小,Z与Y、W相邻,基态Z原子的s能级与p能级电子数相同,R位于第四周期且基态原子有4个未成对电子。下列说法错误的是
是一种常见补血剂。已知短周期主族元素X、Y、Z、W的原子序数依次增大,X原子半径最小,Z与Y、W相邻,基态Z原子的s能级与p能级电子数相同,R位于第四周期且基态原子有4个未成对电子。下列说法错误的是
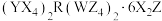 是一种常见补血剂。已知短周期主族元素X、Y、Z、W的原子序数依次增大,X原子半径最小,Z与Y、W相邻,基态Z原子的s能级与p能级电子数相同,R位于第四周期且基态原子有4个未成对电子。下列说法错误的是
是一种常见补血剂。已知短周期主族元素X、Y、Z、W的原子序数依次增大,X原子半径最小,Z与Y、W相邻,基态Z原子的s能级与p能级电子数相同,R位于第四周期且基态原子有4个未成对电子。下列说法错误的是A.第一电离能: |
B.简单氢化物的沸点: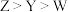 |
C.该化合物可溶于水,难溶于 |
D.最高价含氧酸根的键角: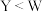 |
您最近一年使用:0次


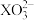 的空间构型为四面体形
的空间构型为四面体形

