Ⅰ.化学与生产、生活密切相关,回答下列问题。
(1)某品牌奶制品的外包装上有如图所示的说明。用化学反应速率的知识说明避免高温贮存该奶制品的理由_______ 。_______ 。
(3)碱液不能用玻璃塞,请用离子方程式解释化学原理_______ 。
Ⅱ.烷烃、烯烃都是重要的有机化合物。请回答下列问题:
(4)乙烷与氯气反应,生成的二氯乙烷的结构有_______ 种,其中第一步取代反应的化学方程式为_______ 。
(5)把乙烯通入溴的四氯化碳溶液中,充分振荡、静置,观察到溴的四氯化碳溶液褪色,写出该过程中发生反应的化学方程式为_____ 。
(6)烷烃A在同温同压下蒸气的密度是 的36倍,写出该烷烃的分子式:
的36倍,写出该烷烃的分子式:_______ ,符合该分子式且一氯代物种类最多的结构简式为_______ 。
(1)某品牌奶制品的外包装上有如图所示的说明。用化学反应速率的知识说明避免高温贮存该奶制品的理由

(3)碱液不能用玻璃塞,请用离子方程式解释化学原理
Ⅱ.烷烃、烯烃都是重要的有机化合物。请回答下列问题:
(4)乙烷与氯气反应,生成的二氯乙烷的结构有
(5)把乙烯通入溴的四氯化碳溶液中,充分振荡、静置,观察到溴的四氯化碳溶液褪色,写出该过程中发生反应的化学方程式为
(6)烷烃A在同温同压下蒸气的密度是
 的36倍,写出该烷烃的分子式:
的36倍,写出该烷烃的分子式:
更新时间:2024-05-10 10:07:24
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】1.下列说法中正确的是________ .
①硅酸易溶于水,酸性比碳酸弱
②水玻璃是纯净物
③硅胶是SiO2
④硅酸化学性质比较稳定,受热不分解
⑤实验室中可以用水玻璃与CO2反应生成硅酸
⑥SiO2溶于水即得硅胶
⑦生产水泥和玻璃的共同原料是石英
⑧高温结构陶瓷比金属材料具有更多优点,如不怕氧化、密度小等优点
⑨新型无机非金属材料具有光学特性、生物功能、电学特性、耐高温、强度高
⑩玛瑙手镯、水晶镜片、玻璃所用材料均为硅酸盐.
①硅酸易溶于水,酸性比碳酸弱
②水玻璃是纯净物
③硅胶是SiO2
④硅酸化学性质比较稳定,受热不分解
⑤实验室中可以用水玻璃与CO2反应生成硅酸
⑥SiO2溶于水即得硅胶
⑦生产水泥和玻璃的共同原料是石英
⑧高温结构陶瓷比金属材料具有更多优点,如不怕氧化、密度小等优点
⑨新型无机非金属材料具有光学特性、生物功能、电学特性、耐高温、强度高
⑩玛瑙手镯、水晶镜片、玻璃所用材料均为硅酸盐.
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】摩擦剂是牙膏的主体成分, 是一种常见的摩擦剂.
是一种常见的摩擦剂.
(1) 在元素周期表中的位置是
在元素周期表中的位置是_____________ .
(2)根据用途推测 在水中的溶解性:
在水中的溶解性:_____________ (填“易溶”或“难溶”).
(3)制备 的方法如下:
的方法如下:

①写出反应Ⅰ的离子方程式________________________ .
②比较酸性强弱:
_____________  (填“>”或“<”).
(填“>”或“<”).
③结合原子结构解释②中酸性关系: 和S电子层数相同,
和S电子层数相同,__________________________ .
(4)为满足不同需求,牙膏中会添加一些特殊物质,如含氟牙膏中添加氟化亚锡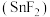 .
.
已知锡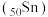 元素与
元素与 同族.下列说法正确的是
同族.下列说法正确的是_____________ (填序号).
a. 元素的最高正化合价为
元素的最高正化合价为 B.
B. 的原子半径比
的原子半径比 大
大
c. 和
和 均可以作良好的半导体材料 D.锡酸
均可以作良好的半导体材料 D.锡酸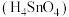 的酸性强于硅酸
的酸性强于硅酸
(5)工业上可以用木炭还原 制备粗硅(同时生成一种还原性气体),该反应的化学方程式为:
制备粗硅(同时生成一种还原性气体),该反应的化学方程式为:_____________ ;该反应能否验证 和C的非金属性强弱?
和C的非金属性强弱?_____________ (填“能”、“不能”)
(6)甲同学按如图所示的装置进行实验.打开分液漏斗活塞,一段时间后,观察试管中现象.甲认为该实验能验证C与 元素的非金属性强弱.你是否同意其观点?
元素的非金属性强弱.你是否同意其观点?_____________ (填“同意”、“不同意”);
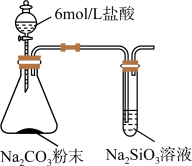
(a)若同意,指出试管中预期的现象,并写出锥形瓶中反应的离子方程式;(b)若不同意,请改进实验,写出实验方案._____________
 是一种常见的摩擦剂.
是一种常见的摩擦剂.(1)
 在元素周期表中的位置是
在元素周期表中的位置是(2)根据用途推测
 在水中的溶解性:
在水中的溶解性:(3)制备
 的方法如下:
的方法如下:
①写出反应Ⅰ的离子方程式
②比较酸性强弱:

 (填“>”或“<”).
(填“>”或“<”).③结合原子结构解释②中酸性关系:
 和S电子层数相同,
和S电子层数相同,(4)为满足不同需求,牙膏中会添加一些特殊物质,如含氟牙膏中添加氟化亚锡
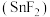 .
.已知锡
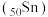 元素与
元素与 同族.下列说法正确的是
同族.下列说法正确的是a.
 元素的最高正化合价为
元素的最高正化合价为 B.
B. 的原子半径比
的原子半径比 大
大c.
 和
和 均可以作良好的半导体材料 D.锡酸
均可以作良好的半导体材料 D.锡酸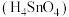 的酸性强于硅酸
的酸性强于硅酸(5)工业上可以用木炭还原
 制备粗硅(同时生成一种还原性气体),该反应的化学方程式为:
制备粗硅(同时生成一种还原性气体),该反应的化学方程式为: 和C的非金属性强弱?
和C的非金属性强弱?(6)甲同学按如图所示的装置进行实验.打开分液漏斗活塞,一段时间后,观察试管中现象.甲认为该实验能验证C与
 元素的非金属性强弱.你是否同意其观点?
元素的非金属性强弱.你是否同意其观点?
(a)若同意,指出试管中预期的现象,并写出锥形瓶中反应的离子方程式;(b)若不同意,请改进实验,写出实验方案.
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】A元素的一种单质是一种重要的半导体材料,含A元素的一种化合物C可用于制造高性能的现代通讯材料——光导纤维,C与烧碱反应生成含A元素的化合物D。
(1)写出C与酸发生反应的化学方程式是________________ 。
(2)将C与纯碱混合高温熔融时也发生化学反应生成D,同时还生成B的最高价氧化物E;将全部的E与全部的D在足量的水中混合后,又发生化学反应生成含A的化合物F。
①分别写出生成D和F的化学方程式:________________ ,________________ 。
②要将NaOH高温熔化,下列坩埚中可选用的是________ (填字母)。
A.普通玻璃坩埚 B.石英玻璃坩埚 C.氧化铝坩埚 D.铁坩埚
(3)100 g C与石灰石的混合物充分反应后生成的气体在标况下的体积为11.2 L,100 g混合物中石灰石的质量分数是________ 。
(1)写出C与酸发生反应的化学方程式是
(2)将C与纯碱混合高温熔融时也发生化学反应生成D,同时还生成B的最高价氧化物E;将全部的E与全部的D在足量的水中混合后,又发生化学反应生成含A的化合物F。
①分别写出生成D和F的化学方程式:
②要将NaOH高温熔化,下列坩埚中可选用的是
A.普通玻璃坩埚 B.石英玻璃坩埚 C.氧化铝坩埚 D.铁坩埚
(3)100 g C与石灰石的混合物充分反应后生成的气体在标况下的体积为11.2 L,100 g混合物中石灰石的质量分数是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】氨是重要的无机化工产品,合成氨工业对国民经济和社会发展具有重要的意义。其原理如下:N2(g)+3H2(g) 2NH3(g) △H<0。在恒温恒容密闭容器中进行合成氨反应,各组分浓度与时间的关系如图所示。
2NH3(g) △H<0。在恒温恒容密闭容器中进行合成氨反应,各组分浓度与时间的关系如图所示。
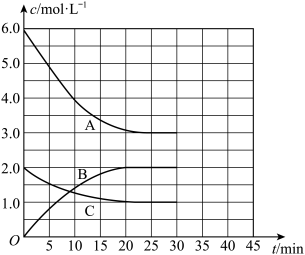
回答下列问题:
(1)表示N2浓度变化的曲线是__________ (填字母),25min时c(NH3)=___________ 。
(2)0~25min内,v(N2):v(H2):v(NH3)=___________ ,该反应的平衡常数K=_________ 。
(3)若升高温度,则平衡向______________ (填“正反应”或“逆反应”)方向移动;正反应速率___________ (填“增大”“减小”或“不变”,下同),逆反应速率___________ 。
 2NH3(g) △H<0。在恒温恒容密闭容器中进行合成氨反应,各组分浓度与时间的关系如图所示。
2NH3(g) △H<0。在恒温恒容密闭容器中进行合成氨反应,各组分浓度与时间的关系如图所示。
回答下列问题:
(1)表示N2浓度变化的曲线是
(2)0~25min内,v(N2):v(H2):v(NH3)=
(3)若升高温度,则平衡向
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】回答下列问题:
(1)化学反应速率可通过实验测定。要测定不同反应时刻反应物或生成物的浓度,可通过观察和测量体系中的某一物质的相关性质,再进行适当的转换和计算。如比较锌粒与不同浓度硫酸反应时的速率,可通过测定收集等体积 需要的
需要的___________ 来实现。
(2)已知: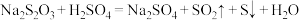 (该反应速率的快慢可通过出现浑浊所需要的时间来判断)。某同学探究影响硫代硫酸钠与稀硫酸反应速率的因素时(注:控制单一变量),设计了如下系列实验:
(该反应速率的快慢可通过出现浑浊所需要的时间来判断)。某同学探究影响硫代硫酸钠与稀硫酸反应速率的因素时(注:控制单一变量),设计了如下系列实验:
该实验①、②可探究___________ 对反应速率的影响,因此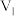 和
和 分别是
分别是___________ 、___________ 。
实验①、③可探究___________ 对反应速率的影响,因此 是
是___________ 。
(1)化学反应速率可通过实验测定。要测定不同反应时刻反应物或生成物的浓度,可通过观察和测量体系中的某一物质的相关性质,再进行适当的转换和计算。如比较锌粒与不同浓度硫酸反应时的速率,可通过测定收集等体积
 需要的
需要的(2)已知:
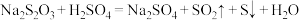 (该反应速率的快慢可通过出现浑浊所需要的时间来判断)。某同学探究影响硫代硫酸钠与稀硫酸反应速率的因素时(注:控制单一变量),设计了如下系列实验:
(该反应速率的快慢可通过出现浑浊所需要的时间来判断)。某同学探究影响硫代硫酸钠与稀硫酸反应速率的因素时(注:控制单一变量),设计了如下系列实验:| 实验序号 | 反应温度 |  浓度 浓度 | 稀硫酸 |  | ||
 | 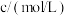 |  | 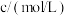 |  | ||
| ① | 20 | 10.0 | 0.10 | 10.0 | 0.50 | 0 |
| ② | 40 | 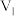 | 0.10 | 10.0 | 0.50 |  |
| ③ | 20 | 10.0 | 0.10 | 4.0 | 0.50 |  |
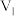 和
和 分别是
分别是实验①、③可探究
 是
是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】汽车尾气中含有CO、NO等有害气体。
(1)通过NO传感器可监测汽车尾气中NO的含量,其工作原理如下图所示:

①NiO电极上发生的是_________ 反应(填“氧化”或“还原”)。
②外电路中,电子的流动方向是从_____ 电极流向_____ 电极(填“NiO”或“Pt”);Pt电极上的电极反应式为___________ 。
(2)一种新型催化剂能使NO和CO发生反应:2NO+2CO 2CO2+N2。已知增大催化剂的比表面积可提高该反应速率。为了验证温度、催化剂的比表面积对化学反应速率的影响规律,某同学设计了三组实验,部分实验条件已经填在下表中。
2CO2+N2。已知增大催化剂的比表面积可提高该反应速率。为了验证温度、催化剂的比表面积对化学反应速率的影响规律,某同学设计了三组实验,部分实验条件已经填在下表中。
①请把表中数据补充完整:A_______________ ;B_______________ 。
②能验证温度对化学反应速率影响规律的是实验_______________ (填实验序号)。
③实验Ⅰ和实验Ⅱ中,NO的物质的量浓度c(NO)随时间t的变化曲线如下图所示,其中表示实验Ⅱ的是曲线_________ (填“甲”或“乙”)。

(1)通过NO传感器可监测汽车尾气中NO的含量,其工作原理如下图所示:

①NiO电极上发生的是
②外电路中,电子的流动方向是从
(2)一种新型催化剂能使NO和CO发生反应:2NO+2CO
 2CO2+N2。已知增大催化剂的比表面积可提高该反应速率。为了验证温度、催化剂的比表面积对化学反应速率的影响规律,某同学设计了三组实验,部分实验条件已经填在下表中。
2CO2+N2。已知增大催化剂的比表面积可提高该反应速率。为了验证温度、催化剂的比表面积对化学反应速率的影响规律,某同学设计了三组实验,部分实验条件已经填在下表中。| 实验 编号 | t(℃) | NO初始浓度 (mol/L) | CO初始浓度 (mol/L) | 催化剂的比表面积(m2/g) |
| Ⅰ | 280 | 1.20×10-3 | 5.80×10-3 | 82 |
| Ⅱ | 280 | 1.20×10-3 | B | 124 |
| Ⅲ | 350 | A | 5.80×10-3 | 82 |
①请把表中数据补充完整:A
②能验证温度对化学反应速率影响规律的是实验
③实验Ⅰ和实验Ⅱ中,NO的物质的量浓度c(NO)随时间t的变化曲线如下图所示,其中表示实验Ⅱ的是曲线

您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】按照要求回答下列问题。
(1)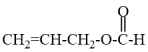 中含氧官能团的名称为
中含氧官能团的名称为__________ 。
(2)分子式为 含有苯环且苯环上只有一个取代基的同分异构体有
含有苯环且苯环上只有一个取代基的同分异构体有__________ 种。(不考虑立体异构)
(1)
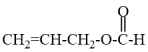 中含氧官能团的名称为
中含氧官能团的名称为(2)分子式为
 含有苯环且苯环上只有一个取代基的同分异构体有
含有苯环且苯环上只有一个取代基的同分异构体有
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】如下图所示是合成某药物的中间体分子(由9个碳原子和若干个氢、氧原子构成)的结构示意图:
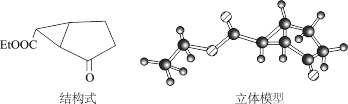
试回答下列问题:
(1)通过对比上面的结构简式与立体模型,请指出结构简式中的“Et”表示的基团是____________ (写结构简式);该药物中间体的分子式为____________ 。
(2)该药物中间体的类别是________ (填字母)。
a.酯 b.羧酸 c.醛
(3)该药物中间体分子中与碳原子结合的氢原子被溴原子取代,所得的一溴代物有________ 种。
(4)该药物中间体分子有多种含苯环的同分异构体,请写出其中一种的结构简式:______________ 。

试回答下列问题:
(1)通过对比上面的结构简式与立体模型,请指出结构简式中的“Et”表示的基团是
(2)该药物中间体的类别是
a.酯 b.羧酸 c.醛
(3)该药物中间体分子中与碳原子结合的氢原子被溴原子取代,所得的一溴代物有
(4)该药物中间体分子有多种含苯环的同分异构体,请写出其中一种的结构简式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】按要求回答下列问题:
(1) 的系统命名为
的系统命名为_______
(2)3-甲基-2-戊烯的键线式为_______ 。
(3) 中的官能团名称为
中的官能团名称为_______
(4) ,1H-核磁共振谱图中有
,1H-核磁共振谱图中有_______ 组特征峰。
(5)衡量一个国家石油化工水平的物质与水发生的加成反应_______
(6)分别只有一个碳原子的醇和酸发生的酯化反应_______
(7)检验工业废水中含有苯酚的试剂是_______
(1)
 的系统命名为
的系统命名为(2)3-甲基-2-戊烯的键线式为
(3)
 中的官能团名称为
中的官能团名称为(4)
 ,1H-核磁共振谱图中有
,1H-核磁共振谱图中有(5)衡量一个国家石油化工水平的物质与水发生的加成反应
(6)分别只有一个碳原子的醇和酸发生的酯化反应
(7)检验工业废水中含有苯酚的试剂是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】下列物品或设施:①光导纤维②计算机芯片③陶瓷餐具④太阳能电池(完成1-2问)
(1)使用了硅单质的是:_______ (填序号,下同)
(2)使用了硅酸盐材料的是:_______ 。
(3)工业上用焦炭还原石英砂制粗硅,请写出反应的化学方程式:_______ 。
(4)A~D是四种烃分子的球棍模型(如图)
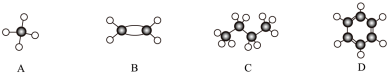
①与A互为同系物的是_______ (填序号)。
②除去A中的B,可以用溴水,写出相应的化学方程式:_______ 。
③C5H12的同分异构体数目为:_______ 。
(1)使用了硅单质的是:
(2)使用了硅酸盐材料的是:
(3)工业上用焦炭还原石英砂制粗硅,请写出反应的化学方程式:
(4)A~D是四种烃分子的球棍模型(如图)

①与A互为同系物的是
②除去A中的B,可以用溴水,写出相应的化学方程式:
③C5H12的同分异构体数目为:
您最近一年使用:0次

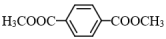 )的同分异构体,0.5molW与足量NaHCO3溶液反应生成44gCO2,W共有
)的同分异构体,0.5molW与足量NaHCO3溶液反应生成44gCO2,W共有



