碱式氧化镍是镍电池的正极活性材料。利用镍渣(主要含NiO,及少量 、CuO、CaO、
、CuO、CaO、 等杂质)制备碱式氧化镍的流程如下:
等杂质)制备碱式氧化镍的流程如下:
(2)浸渣的主要成分除CaSO4外还有______ 。
(3)“沉铜”过程中生成单质S的离子方程式为______ 。
(4)“氧化”中的目的是将 氧化为
氧化为 ,若试剂R选用
,若试剂R选用 ,写出“氧化”时反应的离子方程式:
,写出“氧化”时反应的离子方程式:_______ 。
(5)碱式氧化镍(NiOOH)可用作镍氢电池的正极材料,电池的总反应为
 ,其工作时的正极电极反应式为
,其工作时的正极电极反应式为_______ 。
 、CuO、CaO、
、CuO、CaO、 等杂质)制备碱式氧化镍的流程如下:
等杂质)制备碱式氧化镍的流程如下: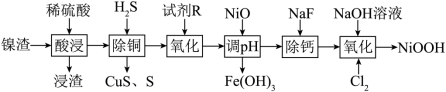
| A.研磨废料 | B.加入大量水 | C.搅拌 | D.适当升高温度 |
(3)“沉铜”过程中生成单质S的离子方程式为
(4)“氧化”中的目的是将
 氧化为
氧化为 ,若试剂R选用
,若试剂R选用 ,写出“氧化”时反应的离子方程式:
,写出“氧化”时反应的离子方程式:(5)碱式氧化镍(NiOOH)可用作镍氢电池的正极材料,电池的总反应为

 ,其工作时的正极电极反应式为
,其工作时的正极电极反应式为
更新时间:2024-05-11 14:10:48
|
相似题推荐
解答题-实验探究题
|
较易
(0.85)
名校
【推荐1】用图所示实验装置可以完成中学化学实验中的一些实验。
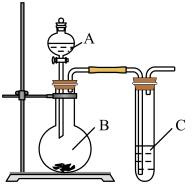
(1)现有稀硝酸、稀盐酸、稀硫酸、碳酸钠粉末、硅酸钠溶液五种试剂。选择三种试剂利用如图装置证明酸性强弱:H2SO4 > H2CO3 > H2SiO3
①仪器B的名称________ ,A中试剂________ ,B中试剂________
②C中发生反应的化学方程式:________________________________
(2)利用如图装置实验,证明二氧化硫气体具有漂白性。已知:Na2SO3 + H2SO4=Na2SO4 +SO2↑+H2O。 在装置A中加入 70%的硫酸溶液,B中加入Na2SO3粉末,
①C中应加入________ 溶液(填“品红”或“石蕊”)。打开分液漏斗活塞,一段时间后观察到C中现象是________________________________ ,反应完全后,将C试管加热一 段时间发生的现象是________________________
②如果仅用如图装置进行此实验,可能造成环境污染,此污染属于________ (选填“白色污染”或“酸雨污染"),因此应该在C装置后加一个盛有________ 溶液的洗气瓶。
③将二氧化硫气体通入FeCl3溶液中反应一.段时间后,滴加KSCN溶液,溶液未变红色,请写出所发生反应的离子方程式:________________________________

(1)现有稀硝酸、稀盐酸、稀硫酸、碳酸钠粉末、硅酸钠溶液五种试剂。选择三种试剂利用如图装置证明酸性强弱:H2SO4 > H2CO3 > H2SiO3
①仪器B的名称
②C中发生反应的化学方程式:
(2)利用如图装置实验,证明二氧化硫气体具有漂白性。已知:Na2SO3 + H2SO4=Na2SO4 +SO2↑+H2O。 在装置A中加入 70%的硫酸溶液,B中加入Na2SO3粉末,
①C中应加入
②如果仅用如图装置进行此实验,可能造成环境污染,此污染属于
③将二氧化硫气体通入FeCl3溶液中反应一.段时间后,滴加KSCN溶液,溶液未变红色,请写出所发生反应的离子方程式:
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐2】常温下,二甲基亚砜( )为无色无臭且能与水混溶的透明液体,熔点为18.4℃,沸点为189℃。实验室模拟“
)为无色无臭且能与水混溶的透明液体,熔点为18.4℃,沸点为189℃。实验室模拟“ 氧化法”制备二甲基亚砜的装置如图所示(部分夹持装置省略)。
氧化法”制备二甲基亚砜的装置如图所示(部分夹持装置省略)。

已知:①制备二甲基亚砜的反应原理为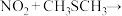

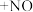 。
。
②二甲基硫醚(CH3SCH3)和二甲基亚砜的密度分别为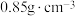 和
和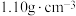 。
。
③ 遇微热易分解为
遇微热易分解为 和水。
和水。
实验过程:将A仪器中制得的气体通入 二甲基硫醚中,控制温度为60~80℃,反应一段时间得到二甲基亚砜粗品,粗品经减压蒸馏后共收集到
二甲基硫醚中,控制温度为60~80℃,反应一段时间得到二甲基亚砜粗品,粗品经减压蒸馏后共收集到 二甲基亚砜纯品。回答下列问题:
二甲基亚砜纯品。回答下列问题:
(1)A的名称为___________ ;仪器x的进水口为___________ (填“d”或“c”)口;B中盛放的试剂的目的是干燥 ,则B中盛放的试剂可能是
,则B中盛放的试剂可能是___________ (填名称)。
(2)通常采用水浴加热来控制温度为60~80℃,该方法的优点是___________ 。
(3)实验中 需过量的原因是
需过量的原因是___________ 。
(4) 溶液吸收尾气中
溶液吸收尾气中 和
和 的化学方程式为
的化学方程式为___________ 。
(5)本实验的产率是___________ (保留2位小数)%。
 )为无色无臭且能与水混溶的透明液体,熔点为18.4℃,沸点为189℃。实验室模拟“
)为无色无臭且能与水混溶的透明液体,熔点为18.4℃,沸点为189℃。实验室模拟“ 氧化法”制备二甲基亚砜的装置如图所示(部分夹持装置省略)。
氧化法”制备二甲基亚砜的装置如图所示(部分夹持装置省略)。
已知:①制备二甲基亚砜的反应原理为
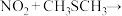

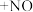 。
。②二甲基硫醚(CH3SCH3)和二甲基亚砜的密度分别为
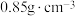 和
和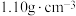 。
。③
 遇微热易分解为
遇微热易分解为 和水。
和水。实验过程:将A仪器中制得的气体通入
 二甲基硫醚中,控制温度为60~80℃,反应一段时间得到二甲基亚砜粗品,粗品经减压蒸馏后共收集到
二甲基硫醚中,控制温度为60~80℃,反应一段时间得到二甲基亚砜粗品,粗品经减压蒸馏后共收集到 二甲基亚砜纯品。回答下列问题:
二甲基亚砜纯品。回答下列问题:(1)A的名称为
 ,则B中盛放的试剂可能是
,则B中盛放的试剂可能是(2)通常采用水浴加热来控制温度为60~80℃,该方法的优点是
(3)实验中
 需过量的原因是
需过量的原因是(4)
 溶液吸收尾气中
溶液吸收尾气中 和
和 的化学方程式为
的化学方程式为(5)本实验的产率是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐3】以下是有关铝的实验探究,请回答相关问题:
(1)用铝粉和 做铝热反应实验,需要的试剂还有___________。
做铝热反应实验,需要的试剂还有___________。
(2)镁能发生和铝类似的“镁热反应”,写出镁在高温下和 反应的化学方程式
反应的化学方程式___________ 。
(3)向集满 的铝制易拉罐中加入过量
的铝制易拉罐中加入过量 浓溶液,立即封闭罐口,易拉罐渐渐凹瘪;再过一段时间,罐壁又重新凸起。写出罐壁又重新凸起发生的相关离子方程式:
浓溶液,立即封闭罐口,易拉罐渐渐凹瘪;再过一段时间,罐壁又重新凸起。写出罐壁又重新凸起发生的相关离子方程式:___________ 。
(4)用打磨过的铝片进行如下实验,下列分析不合理的是___________
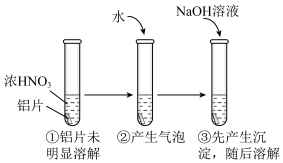
(5)某铝土矿的主要成分为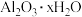 ,还含有
,还含有 和
和 杂质(已知
杂质(已知 难溶于水,且与稀硫酸及其它成分均不反应)。称取
难溶于水,且与稀硫酸及其它成分均不反应)。称取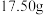 铝土矿样品,加入
铝土矿样品,加入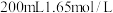 的稀硫酸,恰好完全反应,过滤得沉淀
的稀硫酸,恰好完全反应,过滤得沉淀 ,然后在滤液中加入足量的
,然后在滤液中加入足量的 溶液,得到沉淀
溶液,得到沉淀 。
。
①该试样中 的物质的量为
的物质的量为___________  。
。
②样品中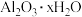 的
的
___________ 。
(1)用铝粉和
 做铝热反应实验,需要的试剂还有___________。
做铝热反应实验,需要的试剂还有___________。A. | B. | C. | D. |
(2)镁能发生和铝类似的“镁热反应”,写出镁在高温下和
 反应的化学方程式
反应的化学方程式(3)向集满
 的铝制易拉罐中加入过量
的铝制易拉罐中加入过量 浓溶液,立即封闭罐口,易拉罐渐渐凹瘪;再过一段时间,罐壁又重新凸起。写出罐壁又重新凸起发生的相关离子方程式:
浓溶液,立即封闭罐口,易拉罐渐渐凹瘪;再过一段时间,罐壁又重新凸起。写出罐壁又重新凸起发生的相关离子方程式:(4)用打磨过的铝片进行如下实验,下列分析不合理的是___________

| A.①中铝片发生了钝化 |
| B.②中产生的气泡是氮氧化合物,不是氢气 |
C.③中沉淀溶解的离子方程式是 |
| D.②中加水稀释过程中,仅发生了氧化还原反应 |
(5)某铝土矿的主要成分为
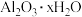 ,还含有
,还含有 和
和 杂质(已知
杂质(已知 难溶于水,且与稀硫酸及其它成分均不反应)。称取
难溶于水,且与稀硫酸及其它成分均不反应)。称取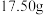 铝土矿样品,加入
铝土矿样品,加入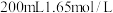 的稀硫酸,恰好完全反应,过滤得沉淀
的稀硫酸,恰好完全反应,过滤得沉淀 ,然后在滤液中加入足量的
,然后在滤液中加入足量的 溶液,得到沉淀
溶液,得到沉淀 。
。①该试样中
 的物质的量为
的物质的量为 。
。②样品中
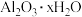 的
的
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
【推荐1】CO2相关转化的研究,对解决环境、能源问题意义重大。
(1)CO2催化加氢制取汽油,CO2转化过程示意图如图:
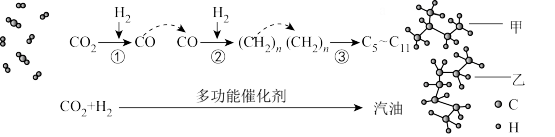
下列说法不正确的是____ 。
a.反应①的产物中含有水
b.图中甲与乙互为同系物
c.反应②中只有碳碳键形成
d.汽油主要是C5~C11的烃类混合物
(2)CO2与CH4经催化重整可制得合成气:
CH4(g)+CO2(g) 2CO(g)+2H2(g) ΔH
2CO(g)+2H2(g) ΔH
已知:C(s)+2H2(g)=CH4(g) ΔH1=−75 kJ∙mol−1
C(s)+O2(g)=CO2g) ΔH2=−394 kJ∙mol−1
2C(s)+O2(g)=2CO(g) ΔH3=−222 kJ∙mol−1
该催化重整反应的ΔH=____ kJ∙mol−1
(3)CO2与H2反应制取甲醇(CH3OH)。
已知1gH2与CO2反应生成CH3OH气体和水蒸气放出9.7kJ的热量。
①写出CO2(g)与H2(g)制取CH3OH(g)的热化学方程式____ 。
②已知:1mol液态甲醇完全气化需吸热37.4kJ,1mol液态水完全气化需吸热44.0kJ,由CO2合成1mol液态甲醇和1mol液态水放出____ kJ热量。
(4)制取化工原料草酸铝[Al2(C2O4)3]。
利用Al−CO2电池,能有效地将CO2转化成草酸铝,工作原理如图所示。
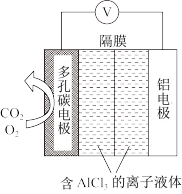
①电池的负极反应式是:____ 。
②电池的正极反应式:2CO2+2e-=C2O (草酸根)
(草酸根)
正极反应过程中,O2起催化作用,催化过程可表示为:
I.2O2+2e-=2O
II.……
写出II的离子方程式:____ 。
(1)CO2催化加氢制取汽油,CO2转化过程示意图如图:

下列说法不正确的是
a.反应①的产物中含有水
b.图中甲与乙互为同系物
c.反应②中只有碳碳键形成
d.汽油主要是C5~C11的烃类混合物
(2)CO2与CH4经催化重整可制得合成气:
CH4(g)+CO2(g)
 2CO(g)+2H2(g) ΔH
2CO(g)+2H2(g) ΔH已知:C(s)+2H2(g)=CH4(g) ΔH1=−75 kJ∙mol−1
C(s)+O2(g)=CO2g) ΔH2=−394 kJ∙mol−1
2C(s)+O2(g)=2CO(g) ΔH3=−222 kJ∙mol−1
该催化重整反应的ΔH=
(3)CO2与H2反应制取甲醇(CH3OH)。
已知1gH2与CO2反应生成CH3OH气体和水蒸气放出9.7kJ的热量。
①写出CO2(g)与H2(g)制取CH3OH(g)的热化学方程式
②已知:1mol液态甲醇完全气化需吸热37.4kJ,1mol液态水完全气化需吸热44.0kJ,由CO2合成1mol液态甲醇和1mol液态水放出
(4)制取化工原料草酸铝[Al2(C2O4)3]。
利用Al−CO2电池,能有效地将CO2转化成草酸铝,工作原理如图所示。

①电池的负极反应式是:
②电池的正极反应式:2CO2+2e-=C2O
 (草酸根)
(草酸根)正极反应过程中,O2起催化作用,催化过程可表示为:
I.2O2+2e-=2O

II.……
写出II的离子方程式:
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
解题方法
【推荐2】Ⅰ.某实验小组同学进行如图1实验,以检验化学反应中的能量变化。请回答下列问题:
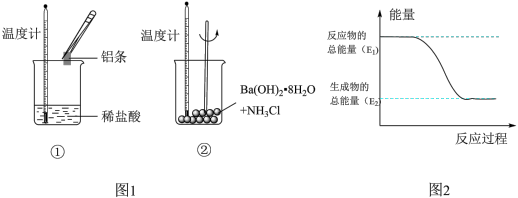
(1)实验中发现,反应后①中的温度升高;②中的温度降低。由此判断铝条与盐酸的反应是________ 热反应。反应过程________ (填“①”或“②”)的能量变化可用图2表示。
Ⅱ.A、B、C、D四种金属按下表中装置进行实验。
(2)根据实验现象回答下列问题:
①装置甲中溶液中的阴离子移向________ 极(填“A”或“B”)。
②装置乙中正极的电极反应式为________ 。
③装置丙中溶液的pH________ (填“变大”“变小”或“不变”)。
④四种金属活动性由强到弱的顺序是________ 。
⑤实验后同学们经过充分讨论,观察原电池反应特点,认真符合某些要求的化学反应都可以通过原电池来实现。下列化学反应在理论上可以设计成原电池的是________ 。
A. B.
B.
C. D.
D.

(1)实验中发现,反应后①中的温度升高;②中的温度降低。由此判断铝条与盐酸的反应是
Ⅱ.A、B、C、D四种金属按下表中装置进行实验。
| 装置 | 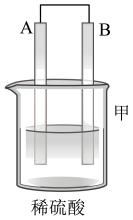 | 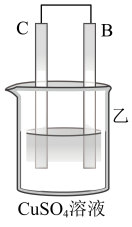 |  |
| 现象 | 二价金属A不断溶解 | C的质量增加 | A上有气体产生 |
①装置甲中溶液中的阴离子移向
②装置乙中正极的电极反应式为
③装置丙中溶液的pH
④四种金属活动性由强到弱的顺序是
⑤实验后同学们经过充分讨论,观察原电池反应特点,认真符合某些要求的化学反应都可以通过原电池来实现。下列化学反应在理论上可以设计成原电池的是
A.
 B.
B.
C.
 D.
D.
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
解题方法
【推荐3】研究化学反应的原理,对掌握物质的应用有重要的意义。
I.硅是太阳能电池的重要材料。“精炼硅”反应历程中的能量变化如图所示:_______ (选填“吸热”或“放热”)反应。
II.研究 、
、 、CO等气体的无害化处理对治理大气污染、建设生态文明有重要意义。
、CO等气体的无害化处理对治理大气污染、建设生态文明有重要意义。
(2)一定温度下,在恒容的密闭容器中充入1molCO和2mol ,发生
,发生 ,对于该反应,下列说法正确的是_______(填序号)。
,对于该反应,下列说法正确的是_______(填序号)。
(3)利用反应2NO(g)+2CO(g)⇌N2(g)+2CO2(g),可实现汽车尾气的无害化处理。一定温度下,在体积为2L的恒容密闭容器中加入等物质的量的NO和CO,测得部分物质的物质的量随时间的变化如图所示。_______ ;a点正反应速率_______ 逆反应速率(填“>”“<”或“=”)。
②从反应开始到达到平衡,
_______  ;该条件下,CO的平衡转化率为
;该条件下,CO的平衡转化率为_______ 。
(4)可用电化学原理处理 制备硫酸,装置图如图,电极为多孔材料。写出M极的电极方程式:
制备硫酸,装置图如图,电极为多孔材料。写出M极的电极方程式:_______ 。
I.硅是太阳能电池的重要材料。“精炼硅”反应历程中的能量变化如图所示:

II.研究
 、
、 、CO等气体的无害化处理对治理大气污染、建设生态文明有重要意义。
、CO等气体的无害化处理对治理大气污染、建设生态文明有重要意义。(2)一定温度下,在恒容的密闭容器中充入1molCO和2mol
 ,发生
,发生 ,对于该反应,下列说法正确的是_______(填序号)。
,对于该反应,下列说法正确的是_______(填序号)。A.反应过程中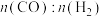 不变 不变 |
| B.升高温度,正反应速率减小 |
| C.往容器中充入He,压强增大,反应速率加快 |
| D.容器内混合气体的平均摩尔质量保持不变时说明反应已达平衡 |

②从反应开始到达到平衡,

 ;该条件下,CO的平衡转化率为
;该条件下,CO的平衡转化率为(4)可用电化学原理处理
 制备硫酸,装置图如图,电极为多孔材料。写出M极的电极方程式:
制备硫酸,装置图如图,电极为多孔材料。写出M极的电极方程式:
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐1】钼是一种过渡金属元素,通常用作合金及不锈钢的添加剂,这种元素可增强合金的强度、硬度、可焊接性及韧性,还可增强其耐高温及耐腐蚀性能。如图是化工生产中制备金属钼的主要流程图。

(1)反应①的尾气可以再利用,写出应用该尾气制得的两种重要化学试剂:___ 。
(2)如果在实验室模拟操作1和操作2,则需要使用的主要玻璃仪器有:___ 。
(3)钼在空气中灼烧生成三氧化钼,三氧化钼溶于氢氧化钠溶液生成钼酸钠;三氧化钼不溶于盐酸或稀硫酸。钼酸钠的化学式为___ 。
(4)工业上制备还原性气体CO和H2的反应原理为CO2+CH4 2CO+2H2,CH4+H2O
2CO+2H2,CH4+H2O CO+3H2。含甲烷体积分数为80%的a L(标准状况)天然气与足量二氧化碳和水蒸气的混合物在高温下反应,甲烷转化率为90%,用产生的还原性气体(CO和H2)还原MoO3制钼,理论上能生产钼的质量为
CO+3H2。含甲烷体积分数为80%的a L(标准状况)天然气与足量二氧化碳和水蒸气的混合物在高温下反应,甲烷转化率为90%,用产生的还原性气体(CO和H2)还原MoO3制钼,理论上能生产钼的质量为___ 。

(1)反应①的尾气可以再利用,写出应用该尾气制得的两种重要化学试剂:
(2)如果在实验室模拟操作1和操作2,则需要使用的主要玻璃仪器有:
(3)钼在空气中灼烧生成三氧化钼,三氧化钼溶于氢氧化钠溶液生成钼酸钠;三氧化钼不溶于盐酸或稀硫酸。钼酸钠的化学式为
(4)工业上制备还原性气体CO和H2的反应原理为CO2+CH4
 2CO+2H2,CH4+H2O
2CO+2H2,CH4+H2O CO+3H2。含甲烷体积分数为80%的a L(标准状况)天然气与足量二氧化碳和水蒸气的混合物在高温下反应,甲烷转化率为90%,用产生的还原性气体(CO和H2)还原MoO3制钼,理论上能生产钼的质量为
CO+3H2。含甲烷体积分数为80%的a L(标准状况)天然气与足量二氧化碳和水蒸气的混合物在高温下反应,甲烷转化率为90%,用产生的还原性气体(CO和H2)还原MoO3制钼,理论上能生产钼的质量为
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
解题方法
【推荐2】某硫酸厂以硫铁矿焙烧后的烧渣(主要成分为Fe2O3、SiO2、Al2O3)为原料制取铵明矾晶体[NH4A1(SO4)2·12H2O]的一种工艺流程如图。

已知:①SiO2是酸性氧化物,难溶于水,酸浸时不发生反应。
②AI(OH)3固体可溶于NaOH等强碱溶液。
请回答下列问题:
(1)写出Fe2O3的一种常见用途:_______ 。
(2)“试剂I”为_______ (填试剂名称),“滤渣b”为_______ (填化学式)。
(3)写出“滤液a”和NaOH溶液反应的离子方程式:_______ 、_______ 。
(4)“滤渣c”的化学式为_______ ,证明铁元素已沉淀完全的实验方法是_______ 。
(5)向NaAlO2溶液中通入足量CO2的离子方程式为_______ 。
(6)从铵明矾溶液中获得铵明矾晶体的实验操作依次为蒸发浓缩、冷却结晶、_______ (填操作名称)、洗涤、干燥。

已知:①SiO2是酸性氧化物,难溶于水,酸浸时不发生反应。
②AI(OH)3固体可溶于NaOH等强碱溶液。
请回答下列问题:
(1)写出Fe2O3的一种常见用途:
(2)“试剂I”为
(3)写出“滤液a”和NaOH溶液反应的离子方程式:
(4)“滤渣c”的化学式为
(5)向NaAlO2溶液中通入足量CO2的离子方程式为
(6)从铵明矾溶液中获得铵明矾晶体的实验操作依次为蒸发浓缩、冷却结晶、
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
【推荐3】一种利用含Co废渣(主要含金属Co,还含有Fe、Zn)制取CoCO3的流程如下图所示:

已知:部分金属离子开始生成氢氧化物沉淀和沉淀完全的pH如下表所示:
(1)酸浸时,不改变H2SO4的浓度和体积,任写出一种可以加快反应速率的方法:_______ 。
(2)酸浸后所得溶液中含Co2+、Fe2+、Zn2+,基态Co2+的电子排布式为_______ 。
(3)加入ZnO调pH的目的是促进Fe3+水解转化为Fe(OH)3沉淀,调pH的范围为_______ ,加入ZnO将Fe3+转化为Fe(OH)3沉淀的离子方程式为_______ 。
(4)写出沉钴反应的离子方程式:_______ 。

已知:部分金属离子开始生成氢氧化物沉淀和沉淀完全的pH如下表所示:
| Fe3+ | Zn2+ | Fe2+ | Co2+ | |
| 开始沉淀的pH | 1.5 | 5.4 | 5.8 | 6.6 |
| 沉淀完全的pH | 3.2 | 8.2 | 8.8 | 9.4 |
(2)酸浸后所得溶液中含Co2+、Fe2+、Zn2+,基态Co2+的电子排布式为
(3)加入ZnO调pH的目的是促进Fe3+水解转化为Fe(OH)3沉淀,调pH的范围为
(4)写出沉钴反应的离子方程式:
您最近一年使用:0次



