常温下,向 、
、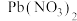 和
和 的混合液中滴加
的混合液中滴加 溶液,
溶液, 与
与 的关系如下图所示,已知:
的关系如下图所示,已知: ,
,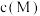 代表
代表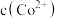 、
、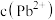 或
或 ;
; ;当被沉淀的离子的物质的量浓度小于
;当被沉淀的离子的物质的量浓度小于 时,认为该离子已沉淀完全。下列叙述正确的是
时,认为该离子已沉淀完全。下列叙述正确的是
 、
、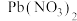 和
和 的混合液中滴加
的混合液中滴加 溶液,
溶液, 与
与 的关系如下图所示,已知:
的关系如下图所示,已知: ,
,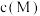 代表
代表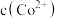 、
、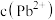 或
或 ;
; ;当被沉淀的离子的物质的量浓度小于
;当被沉淀的离子的物质的量浓度小于 时,认为该离子已沉淀完全。下列叙述正确的是
时,认为该离子已沉淀完全。下列叙述正确的是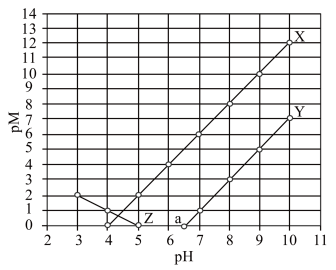
A.常温下,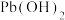 的 的 |
B. 、 、 分别代表 分别代表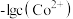 、 、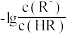 与 与 的关系 的关系 |
C.图中 点对应溶液的 点对应溶液的 为6.5,此时溶液中 为6.5,此时溶液中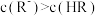 |
D.通过调节溶液 无法分离浓度均为 无法分离浓度均为 的 的 、 、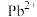 混合溶液 混合溶液 |
2024·福建龙岩·三模 查看更多[2]
更新时间:2024-05-17 22:34:42
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】25 ℃时,Ksp(FeS)=6.3×10-18,Ksp(CuS)=1.3×10-36,Ksp(ZnS)=1.3×10-24。下列有关说法中正确的是
| A.25 ℃时,CuS的溶解度小于ZnS的溶解度 |
| B.25 ℃时,饱和CuS溶液中Cu2+的浓度为1.3×10-36 mol·L-1 |
| C.向物质的量浓度相同的FeCl2、ZnCl2的混合液中加入少量Na2S,只有FeS沉淀生成 |
D.ZnS(s)+Cu2+(aq)  CuS(s)+Zn2+(aq)的平衡常数为1.0×10-12 CuS(s)+Zn2+(aq)的平衡常数为1.0×10-12 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列有关电解质溶液的说法正确的是
| A.10mL0.1mol·L-1Na2CO3溶液逐滴滴加到10mL0.1mol·L-1盐酸中,混合溶液中各离子浓度的大小关系:c(Na+)>c(Cl-)>c(HCO3-)>c(CO32-) |
| B.NH4HCO3溶液中存在:C(NH4+)=C(HCO3-)+C(CO32-)+C(H2CO3) |
| C.常温下,测得某纯CaSO3与水形成的浊液pH为9,已知Ka1(H2SO3)=1.8×10-2,Ka2(H2SO3)=6.0×10-9,忽略SO32-的第二步水解,则Ksp(CaSO3)=3.6×10-10 |
| D.若两种盐溶液的浓度相同且pH(NaX)>pH(NaY),则c(X-)+c(OH-)<c(Y-)+c(OH-) |
您最近一年使用:0次

 、
、 、
、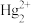 的溶液中滴加
的溶液中滴加 溶液,混合液中
溶液,混合液中 [
[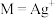 、
、 的关系如图所示。已知:
的关系如图所示。已知: 。下列叙述正确的是
。下列叙述正确的是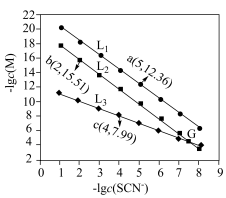
 直线代表
直线代表 与
与

 的平衡常数K大于100
的平衡常数K大于100

