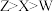下图为一种结构有趣的“糖葫芦”分子,其中 、
、 、
、 、
、 四种元素位于同一主族的相邻周期,
四种元素位于同一主族的相邻周期, 的电负性大于
的电负性大于 ,工业上利用沸点差异从空气中分离出
,工业上利用沸点差异从空气中分离出 的单质。
的单质。 是短周期元素,
是短周期元素, 与
与 的价电子数之和与
的价电子数之和与 的质子数相同,
的质子数相同,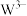 与
与 的电子结构相同。下列说法错误的是
的电子结构相同。下列说法错误的是

 、
、 、
、 、
、 四种元素位于同一主族的相邻周期,
四种元素位于同一主族的相邻周期, 的电负性大于
的电负性大于 ,工业上利用沸点差异从空气中分离出
,工业上利用沸点差异从空气中分离出 的单质。
的单质。 是短周期元素,
是短周期元素, 与
与 的价电子数之和与
的价电子数之和与 的质子数相同,
的质子数相同,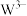 与
与 的电子结构相同。下列说法错误的是
的电子结构相同。下列说法错误的是
| A.分子中W、Y的杂化轨道类型不相同 |
B.第一电离能: |
C. 的氢化物 的氢化物 的VSEPR模型为四面体形 的VSEPR模型为四面体形 |
D.简单离子半径: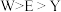 |
更新时间:2024-06-05 23:29:29
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】A、B、C、D是原子序数依次增大的前四周期的主族元素,A是宇宙中含量最多的元素;基态B原子核外 能级上的电子总数与
能级上的电子总数与 能级上的电子总数相等,但第一电离能低于同周期相邻元素;基态C原子核外
能级上的电子总数相等,但第一电离能低于同周期相邻元素;基态C原子核外 能级上的电子总数与
能级上的电子总数与 能级上的电子总数相等,但第一电离能高于同周期相邻元素;基态D原子的最外层只有一个电子,其次外层内的所有轨道的电子均成对。下列说法错误的是
能级上的电子总数相等,但第一电离能高于同周期相邻元素;基态D原子的最外层只有一个电子,其次外层内的所有轨道的电子均成对。下列说法错误的是
 能级上的电子总数与
能级上的电子总数与 能级上的电子总数相等,但第一电离能低于同周期相邻元素;基态C原子核外
能级上的电子总数相等,但第一电离能低于同周期相邻元素;基态C原子核外 能级上的电子总数与
能级上的电子总数与 能级上的电子总数相等,但第一电离能高于同周期相邻元素;基态D原子的最外层只有一个电子,其次外层内的所有轨道的电子均成对。下列说法错误的是
能级上的电子总数相等,但第一电离能高于同周期相邻元素;基态D原子的最外层只有一个电子,其次外层内的所有轨道的电子均成对。下列说法错误的是| A.A元素的单质常温下为气体 |
| B.离子半径:C>B>A |
| C.C元素的最高价氧化物的水化物碱性强于氢氧化铝 |
| D.D元素原子核外共有19种不同运动状态的电子 |
您最近一年使用:0次
【推荐2】现有四种元素基态原子的电子排布式如下。则下列有关比较中正确的是
①ls22s22p63s23p4 ②ls22s22p63s23p3 ③1s22s22p3 ④ls22s22p5
①ls22s22p63s23p4 ②ls22s22p63s23p3 ③1s22s22p3 ④ls22s22p5
| A.原子半径:①>②>③>④ | B.单电子数:④>①>③=② |
| C.电负性:④>③>①>② | D.第一电离能:④>③>①>② |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】下列说法不正确 的是
| A.非金属性P<O | B.热稳定性:NH3>PH3 |
| C.酸性:H2SO4>H3PO4 | D.原子半径大小:P<S |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】A、B、C、D为四种短周期主族元素,且原子序数依次增大。已知A的最外层电子数是其电子层数的2倍,B是第二周期第VIA元素,C原子最外层只有一个电子,D原子最外层电子数是C的3倍。下列说法正确的是
| A.最高价氧化物对应水化物的碱性:C<D | B.最低价的气态氢化物的稳定性:A>B |
| C.四种元素一定在同一周期 | D.原子半径:C>A |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】主族元素W、X、Y、Z位于三个不同短周期,且原子序数依次增大,W与Y同主族,X与Z原子的核外电子数之和是Y原子序数的2倍,X、Z两种元素形成的一种离子结构式为 下列说法正确的是
下列说法正确的是
 下列说法正确的是
下列说法正确的是| A.单质的熔点:Z>X>Y |
| B.X与Y形成的化合物不可能含有共价键 |
| C.X、Y、Z均能与W发生化合反应生成共价化合物 |
| D.Y的单质能与乙醇发生置换反应生成W的单质 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】W、X、Y、Z四种短周期主族元素在元素周期表中的相对位置如图所示,X的气态氢化物可与其最高价含氧酸反应生成离子化合物。下列说法正确的是( )
| W | X | ||
| Y | Z |
| A.4种元素氧化物中,只有W的氧化物能与Na2O2反应 |
| B.Y元素只能形成含氧酸H2YO3和H2YO4 |
| C.Z元素单质具有强氧化性、漂白性 |
| D.简单气态氢化物的稳定性:Y<Z |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列说法中不正确的是( )
| A.元素的第一电离能是元素的单质失去最外层1个电子所需要吸收的能量,同周期从左到右元素的电离能逐渐增大 |
| B.元素的电负性是衡量元素在化合物中吸引电子能力大小的一种标度,同主族从上到下元素的电负性逐渐减小 |
| C.元素的性质随着原子序数的增大而呈周期性变化 |
| D.鲍林的电负性是以氟的电负性为4.0和锂的电负性为1.0作为相对标准得出的 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列关于第三周期元素及相关物质的性质比较中,正确的是
A.酸性: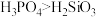 | B.熔点:红磷>单晶硅 |
| C.第一电离能:S>P | D.热稳定性: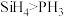 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列关于元素的“最”及其因果关系描述正确的是
| A.元素周期表的f区包括镧系、锕系元素,所以周期表中含元素种类最多的区为f区 |
| B.因为F元素的得电子能力最强,所以元素周期表中第一电离能最大的是F |
C.因为元素非金属性F>O,所以最简单氢化物的沸点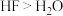 |
D.因为C原子易形成 杂化轨道,可以以四个价键进行不同方式的连接,所以形成化合物种类最多的元素在第ⅣA族 杂化轨道,可以以四个价键进行不同方式的连接,所以形成化合物种类最多的元素在第ⅣA族 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
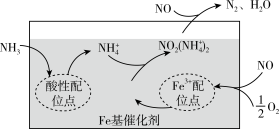
【推荐2】用氨水吸收硫酸工厂尾气中的SO2,发生的反应为:2NH3·H2O+SO2=(NH4)2SO3+H2O。下列说法不正确的是
| A.SO2是极性分子 |
| B.NH3中氮原子的杂化方式为sp3杂化 |
| C.(NH4)2SO3晶体中含离子键、共价键、配位键 |
| D.H2O分子间存在氢键所以较稳定 |
您最近一年使用:0次