为了从海带中提取碘,某研究性学习小组设计并进行了以下实验:______ (从下列仪器中选出所需的仪器,用标号字母填写在空白处)。
A.烧杯 B.坩埚 C.表面皿 D.泥三角 E.酒精灯 F.干燥器
(2)步骤⑤的实验操作名称是______ 。
(3)操作⑤选用苯做萃取剂,苯可以做萃取剂是因为______。
(4)④过程的离子方程式__________________
(5)从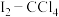 溶液中提取碘可用反萃取法,其流程如下:
溶液中提取碘可用反萃取法,其流程如下:
①操作1中向装有 的
的 溶液加入少量
溶液加入少量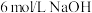 溶液,反应的离子方程式为
溶液,反应的离子方程式为______ ;
②振荡至溶液的______ 色消失,静置、分层,则______ (填“上”、“下”)层为 ;
;
③将含碘的碱溶液从仪器的______ (填“上”、“下”)口倒入烧杯中;
④边搅拌边加入几滴45% 溶液,溶液立即转为棕黄色,并析出碘晶体,若生成
溶液,溶液立即转为棕黄色,并析出碘晶体,若生成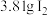 转移
转移______ mol电子。
(6) 溶液浓度越大吸光度越大。用色度计测得溶液的吸光度后,利用以溶液吸光度为纵坐标、碘浓度为横坐标的标准曲线图,可以得出被测溶液浓度其结果如图所示。海带灼热(灰化)时间超过40min,测得碘的含量逐渐降低,原因是
溶液浓度越大吸光度越大。用色度计测得溶液的吸光度后,利用以溶液吸光度为纵坐标、碘浓度为横坐标的标准曲线图,可以得出被测溶液浓度其结果如图所示。海带灼热(灰化)时间超过40min,测得碘的含量逐渐降低,原因是____________ 。
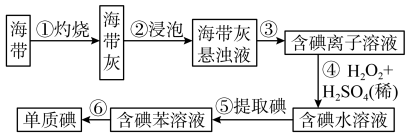
A.烧杯 B.坩埚 C.表面皿 D.泥三角 E.酒精灯 F.干燥器
(2)步骤⑤的实验操作名称是
(3)操作⑤选用苯做萃取剂,苯可以做萃取剂是因为______。
| A.苯不溶于水 | B.苯的密度比水小 |
| C.碘在苯中比在水中溶解度更大 | D.苯与碘水不反应 |
(4)④过程的离子方程式
(5)从
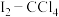 溶液中提取碘可用反萃取法,其流程如下:
溶液中提取碘可用反萃取法,其流程如下: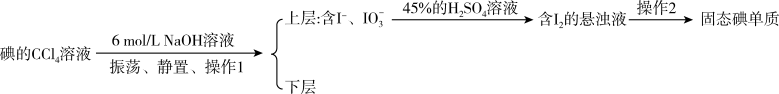
①操作1中向装有
 的
的 溶液加入少量
溶液加入少量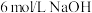 溶液,反应的离子方程式为
溶液,反应的离子方程式为②振荡至溶液的
 ;
;③将含碘的碱溶液从仪器的
④边搅拌边加入几滴45%
 溶液,溶液立即转为棕黄色,并析出碘晶体,若生成
溶液,溶液立即转为棕黄色,并析出碘晶体,若生成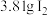 转移
转移(6)
 溶液浓度越大吸光度越大。用色度计测得溶液的吸光度后,利用以溶液吸光度为纵坐标、碘浓度为横坐标的标准曲线图,可以得出被测溶液浓度其结果如图所示。海带灼热(灰化)时间超过40min,测得碘的含量逐渐降低,原因是
溶液浓度越大吸光度越大。用色度计测得溶液的吸光度后,利用以溶液吸光度为纵坐标、碘浓度为横坐标的标准曲线图,可以得出被测溶液浓度其结果如图所示。海带灼热(灰化)时间超过40min,测得碘的含量逐渐降低,原因是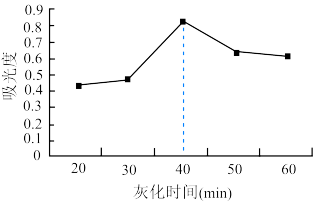
更新时间:2024-05-21 14:08:19
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】MnO2是一种两性氧化物,用软锰矿(主要成分为MnO2,含少量铁的氧化物)和BaS可制备高纯MnCO3。
(1)保持BaS投料量不变,随MnO2与BaS投料比增大,软锰矿还原率和氢氧化钡的产率的变化如图所示。当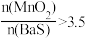 时,
时, 产率减小的原因是
产率减小的原因是_______ 。

(2)搅拌时间对 产率的影响如图2所示,延长搅拌时间,
产率的影响如图2所示,延长搅拌时间, 产率提高,原因为
产率提高,原因为_______ 。

(3)反应后的滤渣中还含有S和未反应的MnO2。以此滤渣为原料制备高纯度的MnCO3的流程如下图。
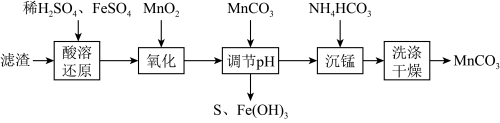
①酸溶还原时,MnO2发生反应的离子方程式_______ 。
② 溶液和
溶液和 固体混合后,反应生成MnCO3。反应的离子方程式为
固体混合后,反应生成MnCO3。反应的离子方程式为_______ 。
③实际制取MnCO3时,一般选择使用氨水— 混合溶液代替
混合溶液代替 固体,这样改进的优点是
固体,这样改进的优点是_______ 。
④常温下,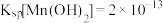 、
、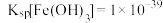 。当某离子浓度小于
。当某离子浓度小于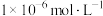 时,认为该离子已除净。氧化后所得溶液中
时,认为该离子已除净。氧化后所得溶液中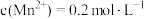 ,为使溶液中
,为使溶液中 除净,调节pH的范围应为
除净,调节pH的范围应为_______ 。
(1)保持BaS投料量不变,随MnO2与BaS投料比增大,软锰矿还原率和氢氧化钡的产率的变化如图所示。当
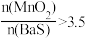 时,
时, 产率减小的原因是
产率减小的原因是
(2)搅拌时间对
 产率的影响如图2所示,延长搅拌时间,
产率的影响如图2所示,延长搅拌时间, 产率提高,原因为
产率提高,原因为
(3)反应后的滤渣中还含有S和未反应的MnO2。以此滤渣为原料制备高纯度的MnCO3的流程如下图。

①酸溶还原时,MnO2发生反应的离子方程式
②
 溶液和
溶液和 固体混合后,反应生成MnCO3。反应的离子方程式为
固体混合后,反应生成MnCO3。反应的离子方程式为③实际制取MnCO3时,一般选择使用氨水—
 混合溶液代替
混合溶液代替 固体,这样改进的优点是
固体,这样改进的优点是④常温下,
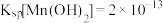 、
、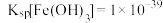 。当某离子浓度小于
。当某离子浓度小于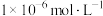 时,认为该离子已除净。氧化后所得溶液中
时,认为该离子已除净。氧化后所得溶液中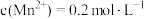 ,为使溶液中
,为使溶液中 除净,调节pH的范围应为
除净,调节pH的范围应为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】某小组设计实验探究 的性质,装置如图所示。
的性质,装置如图所示。
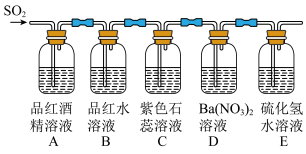
观察到的实验现象如下:
已知:NO能被酸性 氧化成
氧化成 ,与碱石灰不反应。
,与碱石灰不反应。
回答下列问题:
(1)实验室制 宜选择下列试剂中的__________(填标号)。
宜选择下列试剂中的__________(填标号)。
(2)依据实验现象判断 在
在___________ (填化学式)存在下表现漂白性,预测C中现象是___________ 。
(3)D中产生的白色沉淀是_______ (填化学式),D中发生反应的离子方程式为________ 。
(4)E中现象表明 具有的性质是
具有的性质是___________ (填标号)。
a.漂白性 b.酸性 c.氧化性 d.还原性
(5)为了证明 的漂白性是暂时性的,请设计一个补充实验:
的漂白性是暂时性的,请设计一个补充实验:___________ 。
(6)为处理上述实验尾气,下列装置中可供选择的是___________ (填标号)。

 的性质,装置如图所示。
的性质,装置如图所示。
观察到的实验现象如下:
| 装置标号 | A | B | C | D | E |
| 现象 | 溶液不褪色 | 溶液变无色 | ? | 产生白色沉淀 | 产生黄色浑浊 |
 氧化成
氧化成 ,与碱石灰不反应。
,与碱石灰不反应。回答下列问题:
(1)实验室制
 宜选择下列试剂中的__________(填标号)。
宜选择下列试剂中的__________(填标号)。A. 粉末和浓硝酸 粉末和浓硝酸 | B. 粉末和70%浓硫酸 粉末和70%浓硫酸 |
C. 粉末和30%稀硝酸 粉末和30%稀硝酸 | D. 粉末和10%盐酸 粉末和10%盐酸 |
(2)依据实验现象判断
 在
在(3)D中产生的白色沉淀是
(4)E中现象表明
 具有的性质是
具有的性质是a.漂白性 b.酸性 c.氧化性 d.还原性
(5)为了证明
 的漂白性是暂时性的,请设计一个补充实验:
的漂白性是暂时性的,请设计一个补充实验:(6)为处理上述实验尾气,下列装置中可供选择的是

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】一种利用电化学方法同时脱除NO/SO2的工艺如图所示:
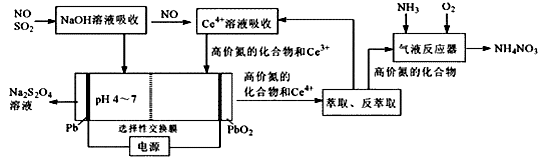
已知SO2水溶液中含硫微粒分布分数(Xi)与pH关系如图所示
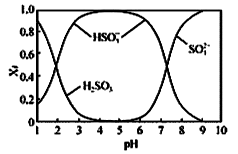
(1)NaOH溶液吸收SO2时,溶液的pH由9→6时,主要发生反应的离子方程式为________ 。
(2)含Ce4+的溶液吸收NO,若高价氮中的NO2、N2O3、NO2-、NO3-各1mol,则消耗0.5mol·L-1的含Ce4+溶液的体积为________ L;其中NO转化NO3-的离子方程式为________ 。
(3)电解槽中,阴极电极反应式主要为________ ,阳极电极反应式为________ 。
(4)在“气液反应器”中高价氮中的N2O3化合为NH4NO3的化学方程式为________ 。

已知SO2水溶液中含硫微粒分布分数(Xi)与pH关系如图所示

(1)NaOH溶液吸收SO2时,溶液的pH由9→6时,主要发生反应的离子方程式为
(2)含Ce4+的溶液吸收NO,若高价氮中的NO2、N2O3、NO2-、NO3-各1mol,则消耗0.5mol·L-1的含Ce4+溶液的体积为
(3)电解槽中,阴极电极反应式主要为
(4)在“气液反应器”中高价氮中的N2O3化合为NH4NO3的化学方程式为
您最近一年使用:0次
【推荐1】“雾霾”成为人们越来越关心的环境问题。雾霾中含有二氧化硫、氮氧化物和可吸入颗粒物等污染性物质。请回答下列问题:
(1)汽车尾气是雾霾形成的原因之一。尾气治理可用汽油中挥发出来的烃类物质(CxHy)催化还原尾气中的NO气体,该过程的化学方程式为___ 。
(2)冬季燃煤供暖产生的废气也是雾霾的主要来源之一。发现将煤炭在O2/CO2的气氛下燃烧,能够降低燃煤时NO的排放,主要反应为:2NO(g)+2CO(g) N2(g)+2CO2(g) ΔH
N2(g)+2CO2(g) ΔH
已知:①N2(g)+O2(g) 2NO(g) ΔH1=+180.5kJ·mol-1
2NO(g) ΔH1=+180.5kJ·mol-1
②2CO(g) 2C(s)+O2(g) ΔH2=+221kJ·mol-1
2C(s)+O2(g) ΔH2=+221kJ·mol-1
③C(s)+O2(g) CO2(g) ΔH3=-393.5kJ·mol-1
CO2(g) ΔH3=-393.5kJ·mol-1
则ΔH=___ 。
(3)某研究小组用NaOH溶液吸收尾气中的二氧化硫,将得到的Na2SO3溶液进行电解,其中阴阳膜组合电解装置如图所示,电极材料为石墨。
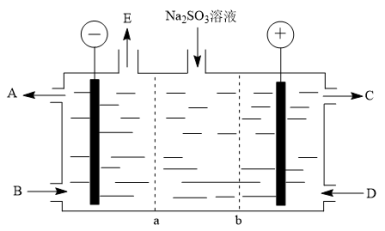
①a表示___ 离子交换膜(填“阴”或“阳”)。A~E分别代表生产中的原料或产品,其中C为硫酸,则A表示___ ,E表示___ 。
②生成C时,阳极的电极反应式为___ 。
(1)汽车尾气是雾霾形成的原因之一。尾气治理可用汽油中挥发出来的烃类物质(CxHy)催化还原尾气中的NO气体,该过程的化学方程式为
(2)冬季燃煤供暖产生的废气也是雾霾的主要来源之一。发现将煤炭在O2/CO2的气氛下燃烧,能够降低燃煤时NO的排放,主要反应为:2NO(g)+2CO(g)
 N2(g)+2CO2(g) ΔH
N2(g)+2CO2(g) ΔH已知:①N2(g)+O2(g)
 2NO(g) ΔH1=+180.5kJ·mol-1
2NO(g) ΔH1=+180.5kJ·mol-1②2CO(g)
 2C(s)+O2(g) ΔH2=+221kJ·mol-1
2C(s)+O2(g) ΔH2=+221kJ·mol-1③C(s)+O2(g)
 CO2(g) ΔH3=-393.5kJ·mol-1
CO2(g) ΔH3=-393.5kJ·mol-1则ΔH=
(3)某研究小组用NaOH溶液吸收尾气中的二氧化硫,将得到的Na2SO3溶液进行电解,其中阴阳膜组合电解装置如图所示,电极材料为石墨。

①a表示
②生成C时,阳极的电极反应式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】以黄铁矿为原料制硫酸产生的硫酸渣中含Fe2O3、SiO2、Al2O3、MgO等,用硫酸渣制备铁红(Fe2O3)的过程如图所示:
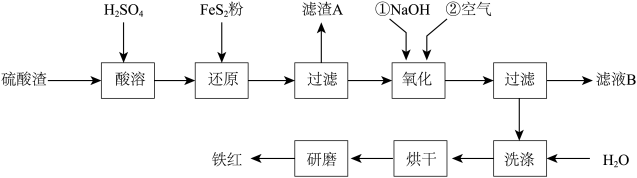
回答下列问题:
(1)酸溶时,粉碎硫酸渣的目的是__________
(2)还原过程中加入FeS2粉增大溶液中Fe2+的含量,同时有H2SO4生成,完成该反应的离子方程式:FeS2+14Fe3++______H2O═15Fe2++______SO42-+______.______________
(3)滤渣A的主要成分为__________
(4)生产过程中,为了确保铁红的纯度,氧化过程需要调节溶液的pH的范围是_____ ;(部分阳离子以氢氧化物形式沉淀时溶液的pH见表)
为得到纯净的Fe(OH)3固体,需要对沉淀进行洗涤,判断沉淀Fe(OH)3是否洗净的方法是__________ 。

回答下列问题:
(1)酸溶时,粉碎硫酸渣的目的是
(2)还原过程中加入FeS2粉增大溶液中Fe2+的含量,同时有H2SO4生成,完成该反应的离子方程式:FeS2+14Fe3++______H2O═15Fe2++______SO42-+______.
(3)滤渣A的主要成分为
(4)生产过程中,为了确保铁红的纯度,氧化过程需要调节溶液的pH的范围是
| 沉淀物 | Fe(OH)3 | Al(OH)3 | Fe(OH)2 | Mg(OH)2 |
| 开始沉淀pH | 2.7 | 3.8 | 7.5 | 9.4 |
| 完全沉淀pH | 3.2 | 5.2 | 9.7 | 12.4 |
为得到纯净的Fe(OH)3固体,需要对沉淀进行洗涤,判断沉淀Fe(OH)3是否洗净的方法是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】硅在地壳中的含量较高,在自然界中硅主要以硅的氧化物和硅酸盐的形式存在。高纯硅是现代信息、半导体和光伏发电等产业都需要的基础材料。下图为一种工业上提纯硅的路线:

相关信息如下:
a.硼、铁、磷在高温下均能与氯气直接反应生成相应的氯化物;
b.有关物质的物理常数见下表:
请回答下列问题:
(1)SiCl4的电子式:________________ ;
(2)写出①的化学方程式________________________________________ ;
(3)①SiO2是硅酸盐玻璃的主要成分,盛放NaOH溶液的试剂瓶若用玻璃瓶塞容易形成粘性的硅酸盐而无法打开,写出发生反应的离子方程式______________________________________________________________
②硅能与NaOH溶液反应,但同主族元素金属锗(Ge)不易溶于NaOH溶液,但有H2O2存在时,锗能与NaOH溶液反应生成锗酸盐,请写出化学反应方程式______________________________________________________________
(4)用强还原剂LiAlH4在乙醚介质中还原SiCl4,制得高纯度的甲硅烷SiH4,SiH4极易水解生成SiO2·nH2O和另一种气体。写出SiH4水解的化学反应方程式__________________________________________________________________
(5)下列有关含硅材料说法正确的是_______________ (填字母)
A. 沸点:SiCl4 > SiH4
B. 金刚砂的有效成分是氮化硅,硬度大、熔点高,可用于制作高温陶瓷和轴承
C. 玻璃、陶瓷、水泥是广泛使用的三大新型硅酸盐材料
D. 人工制造的分子筛(一种具有均匀微孔结构的铝硅酸盐),主要用作吸附剂和催化剂等。
E. 锗、锡、铅的+4价氢氧化物的碱性强弱顺序:Ge(OH)4 < Sn(OH)4 < Pb(OH)4
(6)粗硅中常含有铁、硼、磷等杂质,步骤②需在无氧无水环境下,控制温度在460℃左右得到SiCl4粗品,欲提纯SiCl4,步骤③采用的工艺方法依次是沉降、冷凝和_____________ ,需收集温度在_________ ℃左右的馏分。

相关信息如下:
a.硼、铁、磷在高温下均能与氯气直接反应生成相应的氯化物;
b.有关物质的物理常数见下表:
| 物质 | SiCl4 | BCl3 | FeCl3 | PCl5 | Si | SiH4 |
| 沸点/℃ | 57.7 | 12.8 | 315 | — | 2355 | -111.9 |
| 熔点/℃ | -70.0 | -107.2 | — | — | 1410 | — |
| 升华温度/℃ | — | — | 300 | 162 | — | — |
(1)SiCl4的电子式:
(2)写出①的化学方程式
(3)①SiO2是硅酸盐玻璃的主要成分,盛放NaOH溶液的试剂瓶若用玻璃瓶塞容易形成粘性的硅酸盐而无法打开,写出发生反应的离子方程式
②硅能与NaOH溶液反应,但同主族元素金属锗(Ge)不易溶于NaOH溶液,但有H2O2存在时,锗能与NaOH溶液反应生成锗酸盐,请写出化学反应方程式
(4)用强还原剂LiAlH4在乙醚介质中还原SiCl4,制得高纯度的甲硅烷SiH4,SiH4极易水解生成SiO2·nH2O和另一种气体。写出SiH4水解的化学反应方程式
(5)下列有关含硅材料说法正确的是
A. 沸点:SiCl4 > SiH4
B. 金刚砂的有效成分是氮化硅,硬度大、熔点高,可用于制作高温陶瓷和轴承
C. 玻璃、陶瓷、水泥是广泛使用的三大新型硅酸盐材料
D. 人工制造的分子筛(一种具有均匀微孔结构的铝硅酸盐),主要用作吸附剂和催化剂等。
E. 锗、锡、铅的+4价氢氧化物的碱性强弱顺序:Ge(OH)4 < Sn(OH)4 < Pb(OH)4
(6)粗硅中常含有铁、硼、磷等杂质,步骤②需在无氧无水环境下,控制温度在460℃左右得到SiCl4粗品,欲提纯SiCl4,步骤③采用的工艺方法依次是沉降、冷凝和
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】已知:乙二酸晶体熔点101.5℃;乙二酸晶体加热分解的方程式为:H2C2O4•2H2O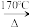 3H2O + CO2↑+ CO↑。现利用下列装置验证反应产物中含有CO2和CO(装置不能重复使用)。请回答下列问题:
3H2O + CO2↑+ CO↑。现利用下列装置验证反应产物中含有CO2和CO(装置不能重复使用)。请回答下列问题:
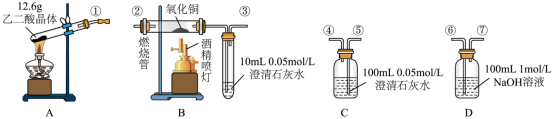
(1)检验装置A气密性的方法是________________________________________________
(2)A装置是否有误_____________ (填“是”或“否”),原因为_______________________
(3)按气流方向连接各仪器,用数字表示接口的连接顺序:①→_________________________ ;
(4)该套装置有明显缺陷,请予以更正________________
(5)证明CO存在的实验现象是________________ ;
(6)根据题给的数据,假设反应产生的气体全部排出,并与吸收液充分反应(提示:B、C中澄清石灰水均先变浑浊,后又变澄清),最终D中生成了两种物质,则这两种生成物的化学式及对应的物质的量分别是①_______________ ,②_______________ 。
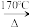 3H2O + CO2↑+ CO↑。现利用下列装置验证反应产物中含有CO2和CO(装置不能重复使用)。请回答下列问题:
3H2O + CO2↑+ CO↑。现利用下列装置验证反应产物中含有CO2和CO(装置不能重复使用)。请回答下列问题:
(1)检验装置A气密性的方法是
(2)A装置是否有误
(3)按气流方向连接各仪器,用数字表示接口的连接顺序:①→
(4)该套装置有明显缺陷,请予以更正
(5)证明CO存在的实验现象是
(6)根据题给的数据,假设反应产生的气体全部排出,并与吸收液充分反应(提示:B、C中澄清石灰水均先变浑浊,后又变澄清),最终D中生成了两种物质,则这两种生成物的化学式及对应的物质的量分别是①
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】某课题组采用活性炭回收海带化工提碘废水中残留的低浓度碘(主要以I-形式存在,杂质不参与反应),实验过程如下:
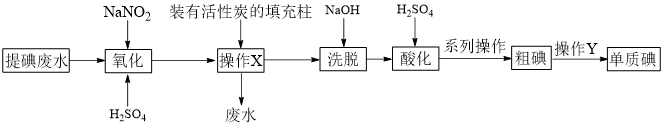
已知:3I2+6NaOH=5NaI+NaIO3+3H2O;
I2+2S2O32-=2I-+S4O62-。
请回答:
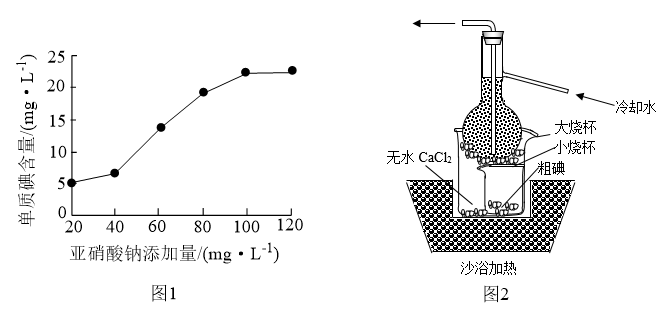
(1)结合图1可知,NaNO2最适宜的添加量为_____ mg•L-1。
(2)操作X的目的是_____ 。
(3)系列操作中涉及抽滤操作,下列有关抽滤的说法中不正确的是_____ 。
A.选择抽滤主要是为了加快过滤速度,得到较干燥的沉淀
B.当溶液具有强酸性、强氧化性时,可用玻璃砂漏斗代替布氏漏斗
C.抽滤不宜过滤胶状沉淀,否则易在滤纸上形成一层密实的沉淀
D.洗涤沉淀时,应开大水龙头,使洗涤剂快速通过沉淀物
(4)进行操作Y时所用装置如图2所示(省去了夹持装置),则操作Y的名称为_____ ;该装置中有两处不合理,请指出其中的一处_____ 。
(5)称取0.5080g粗碘试样于250mL碘量瓶中,加入足量的KI溶液,加盖摇匀至碘完全溶解.迅速用0.1200mol•L-1Na2S2O3标准溶液滴定至浅黄色,再加入淀粉指示剂,继续滴定至蓝色褪去即为终点,共消耗Na2S2O3标准溶液24.00mL。则粗碘试样中碘单质的纯度为_____ 。

已知:3I2+6NaOH=5NaI+NaIO3+3H2O;
I2+2S2O32-=2I-+S4O62-。
请回答:
(1)结合图1可知,NaNO2最适宜的添加量为
(2)操作X的目的是
(3)系列操作中涉及抽滤操作,下列有关抽滤的说法中不正确的是
A.选择抽滤主要是为了加快过滤速度,得到较干燥的沉淀
B.当溶液具有强酸性、强氧化性时,可用玻璃砂漏斗代替布氏漏斗
C.抽滤不宜过滤胶状沉淀,否则易在滤纸上形成一层密实的沉淀
D.洗涤沉淀时,应开大水龙头,使洗涤剂快速通过沉淀物
(4)进行操作Y时所用装置如图2所示(省去了夹持装置),则操作Y的名称为
(5)称取0.5080g粗碘试样于250mL碘量瓶中,加入足量的KI溶液,加盖摇匀至碘完全溶解.迅速用0.1200mol•L-1Na2S2O3标准溶液滴定至浅黄色,再加入淀粉指示剂,继续滴定至蓝色褪去即为终点,共消耗Na2S2O3标准溶液24.00mL。则粗碘试样中碘单质的纯度为

您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】钼酸钠晶体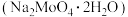 是无公害型冷却水系统的金属腐蚀抑制剂,工业上利用钼精矿(主要成分是不溶于水的
是无公害型冷却水系统的金属腐蚀抑制剂,工业上利用钼精矿(主要成分是不溶于水的 ,含少量
,含少量 等)制备钼酸钠的工艺如图所示。
等)制备钼酸钠的工艺如图所示。
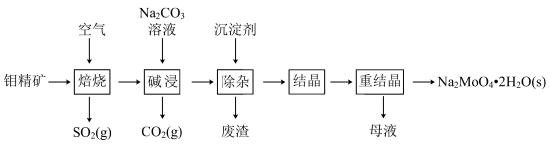
回答下列问题:
(1)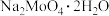 中钼元素的化合价是
中钼元素的化合价是_______ 。
(2)“焙烧”时空气从炉底进入,矿石经粉碎后从炉顶进入,这样处理的目的是_______ ,“焙烧”时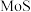 ,转化为
,转化为 ,反应的化学方程式为
,反应的化学方程式为_______ 。
(3)碱浸”所得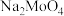 溶液中含
溶液中含 杂质,其中
杂质,其中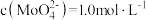 ,
,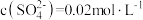 ,在结晶前需加入
,在结晶前需加入 固体以除去溶液中的
固体以除去溶液中的 。当
。当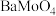 开始沉淀时,
开始沉淀时, 的去除率是
的去除率是_______ 。[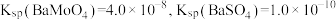 ,溶液体积变化忽略]。
,溶液体积变化忽略]。
(4)“重结晶”的具体操作为_______ 。
(5)另一种利用钼精矿制备钼酸钠的工艺流程中,直接向粉碎后的钼精矿中加入 溶液和
溶液和 溶液来得到钼酸钠,反应的离子方程式为
溶液来得到钼酸钠,反应的离子方程式为_______ ,该工艺的优点是_______ 。(任写一条)
(6)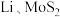 可充电电池的工作原理为:
可充电电池的工作原理为: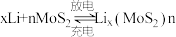 ,则电池充电时阳极的电极反应式为
,则电池充电时阳极的电极反应式为_______ 。
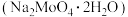 是无公害型冷却水系统的金属腐蚀抑制剂,工业上利用钼精矿(主要成分是不溶于水的
是无公害型冷却水系统的金属腐蚀抑制剂,工业上利用钼精矿(主要成分是不溶于水的 ,含少量
,含少量 等)制备钼酸钠的工艺如图所示。
等)制备钼酸钠的工艺如图所示。
回答下列问题:
(1)
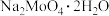 中钼元素的化合价是
中钼元素的化合价是(2)“焙烧”时空气从炉底进入,矿石经粉碎后从炉顶进入,这样处理的目的是
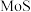 ,转化为
,转化为 ,反应的化学方程式为
,反应的化学方程式为(3)碱浸”所得
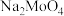 溶液中含
溶液中含 杂质,其中
杂质,其中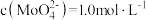 ,
,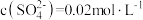 ,在结晶前需加入
,在结晶前需加入 固体以除去溶液中的
固体以除去溶液中的 。当
。当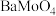 开始沉淀时,
开始沉淀时, 的去除率是
的去除率是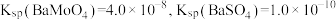 ,溶液体积变化忽略]。
,溶液体积变化忽略]。(4)“重结晶”的具体操作为
(5)另一种利用钼精矿制备钼酸钠的工艺流程中,直接向粉碎后的钼精矿中加入
 溶液和
溶液和 溶液来得到钼酸钠,反应的离子方程式为
溶液来得到钼酸钠,反应的离子方程式为(6)
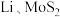 可充电电池的工作原理为:
可充电电池的工作原理为: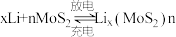 ,则电池充电时阳极的电极反应式为
,则电池充电时阳极的电极反应式为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐1】I.镁燃料电池在可移动电子设备电源和备用电源等方面应用前景广阔。如图为“镁-次氯酸盐”燃料电池原理示意图,电极为镁合金和铂合金。
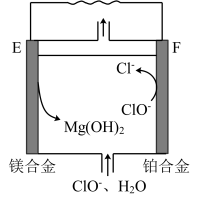
(1)E 为该燃料电池的_____ (填“正”或“负”)极。F 电极上的电极反应为_____ 。
(2)镁燃料电池负极容易发生自腐蚀产生氢气,使负极利用率降低,用化学用语解释其原因:___ 。
II、以干海带为原料提取碘单质和氯化钾的过程要分三步,完成下列填空。
(1)步骤一、灼烧干海带,使其灰化后用热水浸泡过滤,制得原料液,含有氯化钾等物质。实验室灼烧海带应放在__ (填仪器名称)中。选用热水而不是冷水浸泡海带灰的目的是__ 。
(2)步骤二:原料液经结晶过滤分离出氯化钾后,向滤液中通适量氯气氧化 I−,制得富碘溶液。通适量氯气发生反应的离子方程式为__ 。
(3)步骤三:取步骤二中富碘溶液 100 mL,按如下流程分离碘单质。
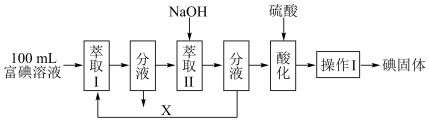
酸化过程发生的反应是:5I−+ +6H+=3I2 +3H2O,则萃取Ⅱ发生的反应离子方程式为
+6H+=3I2 +3H2O,则萃取Ⅱ发生的反应离子方程式为_____ 。萃取剂 X 应选择____ (填字母),萃取操作的仪器是_____ 。
a.100 mL 苯 b.10 mL 乙醇 c.10 mL CCl4
(4)请设计一种检验提取碘后的水溶液中是否还有单质碘的简单方法:___ 。

(1)E 为该燃料电池的
(2)镁燃料电池负极容易发生自腐蚀产生氢气,使负极利用率降低,用化学用语解释其原因:
II、以干海带为原料提取碘单质和氯化钾的过程要分三步,完成下列填空。
(1)步骤一、灼烧干海带,使其灰化后用热水浸泡过滤,制得原料液,含有氯化钾等物质。实验室灼烧海带应放在
(2)步骤二:原料液经结晶过滤分离出氯化钾后,向滤液中通适量氯气氧化 I−,制得富碘溶液。通适量氯气发生反应的离子方程式为
(3)步骤三:取步骤二中富碘溶液 100 mL,按如下流程分离碘单质。

酸化过程发生的反应是:5I−+
 +6H+=3I2 +3H2O,则萃取Ⅱ发生的反应离子方程式为
+6H+=3I2 +3H2O,则萃取Ⅱ发生的反应离子方程式为a.100 mL 苯 b.10 mL 乙醇 c.10 mL CCl4
(4)请设计一种检验提取碘后的水溶液中是否还有单质碘的简单方法:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】海带中含有丰富的碘。为了从海带中提取碘,某研究性学习小组设计并进行了以下实验:

(1)步骤③的实验操作名称是______ 。
(2)为检验提取碘后的水溶液中是否还含有单质碘,可选择的试剂是:_____ 。
(3)步骤④反应中能生成可溶性的Mn2+,写出该反应的离子方程式:_____ 。

(1)步骤③的实验操作名称是
(2)为检验提取碘后的水溶液中是否还含有单质碘,可选择的试剂是:
(3)步骤④反应中能生成可溶性的Mn2+,写出该反应的离子方程式:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】海带中含有丰富的碘元素,某化学兴趣小组设计如下流程图提取碘:

请回答下列问题:
(1)操作a的名称是___________ (填“过滤”或“蒸发”);
(2)溶液A中通入足量Cl2的目的是将I-氧化为I2,也能达到该目的的物质是___________ (填“双氧水”或“稀盐酸”);
(3)在萃取时,可选用的萃取剂为___________ (填“酒精”或“四氯化碳”);
(4)已知I2与H2发生反应:I2(g)+H2(g) 2HI(g)。一定条件下,将1molI2和1molH2充入1L的密闭容器中,5min后测得I2的物质的量为0.4mol。
2HI(g)。一定条件下,将1molI2和1molH2充入1L的密闭容器中,5min后测得I2的物质的量为0.4mol。
①用I2表示该反应的化学反应速率是___________ mol·L-1·min-1;
②当其他条件不变时,升高温度,该反应速率将___________ (填“增大”或“减小”)。

请回答下列问题:
(1)操作a的名称是
(2)溶液A中通入足量Cl2的目的是将I-氧化为I2,也能达到该目的的物质是
(3)在萃取时,可选用的萃取剂为
(4)已知I2与H2发生反应:I2(g)+H2(g)
 2HI(g)。一定条件下,将1molI2和1molH2充入1L的密闭容器中,5min后测得I2的物质的量为0.4mol。
2HI(g)。一定条件下,将1molI2和1molH2充入1L的密闭容器中,5min后测得I2的物质的量为0.4mol。①用I2表示该反应的化学反应速率是
②当其他条件不变时,升高温度,该反应速率将
您最近一年使用:0次



