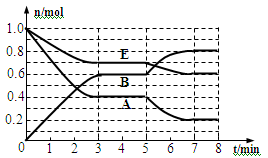
在一体积为2L的密闭容器中,气态物质A、B、E的物质的量n随时间t的变化如图所示。已知达到平衡后,降低温度A的转化率增大。
29、写出此反应的化学方程式_________________________________ ;此反应是___________ 热反应。
30、根据图数据,从反应开始到第一次达到平衡时平均速率v (E)为________________ 。
31、在5~7 min内曲线变化的原因可能是____ (填编号)
A. 降低了温度 B. 使用了催化剂
C. 减小了容器的体积 D. 减少了A的物质的量
32、设该反应达到平衡时的平衡常数为K1,保持温度不变,将容器体积减少一半,达到新的平衡后,测得B的平衡浓度为原来的2.2倍,平衡常数为K2,则_______ (填编号)
A. 平衡向正反应方向移动,且K2 > K1
B. 平衡移动过程中,正反应速率大于逆反应速率
C. 达到新平衡时,A的浓度增大,且K1 > K2
D. 达到新平衡时,E的浓度是原来的2倍多,且K1 = K2
已知在25℃时,亚硝酸、次氯酸和氢硫酸的电离常数分别为:
亚硝酸 Ki= 4.6×10-4
次氯酸 Ki = 3.0×10-8
氢硫酸 Ki 1= 9.1×10-8 Ki 2 = 1.1×10-12
33、写出氢硫酸的第一级电离平衡常数表达式:Ki1 =_________________ 。
34、在相同条件下,试比较H2S、HS-、HClO和HNO2的酸性强弱:______ >______ >_____ >_______ 。
35、保持温度不变,在氢硫酸溶液中加入少量盐酸,下列量会变小的是_____ (填序号)
A.c(S2-)
B.c(H+)
C.Kw
D.氢硫酸电离平衡常数
E.氢硫酸的电离度

29、写出此反应的化学方程式
30、根据图数据,从反应开始到第一次达到平衡时平均速率v (E)为
31、在5~7 min内曲线变化的原因可能是
A. 降低了温度 B. 使用了催化剂
C. 减小了容器的体积 D. 减少了A的物质的量
32、设该反应达到平衡时的平衡常数为K1,保持温度不变,将容器体积减少一半,达到新的平衡后,测得B的平衡浓度为原来的2.2倍,平衡常数为K2,则
A. 平衡向正反应方向移动,且K2 > K1
B. 平衡移动过程中,正反应速率大于逆反应速率
C. 达到新平衡时,A的浓度增大,且K1 > K2
D. 达到新平衡时,E的浓度是原来的2倍多,且K1 = K2
已知在25℃时,亚硝酸、次氯酸和氢硫酸的电离常数分别为:
亚硝酸 Ki= 4.6×10-4
次氯酸 Ki = 3.0×10-8
氢硫酸 Ki 1= 9.1×10-8 Ki 2 = 1.1×10-12
33、写出氢硫酸的第一级电离平衡常数表达式:Ki1 =
34、在相同条件下,试比较H2S、HS-、HClO和HNO2的酸性强弱:
35、保持温度不变,在氢硫酸溶液中加入少量盐酸,下列量会变小的是
A.c(S2-)
B.c(H+)
C.Kw
D.氢硫酸电离平衡常数
E.氢硫酸的电离度
更新时间:2016-12-09 07:13:05
|
相似题推荐
填空题
|
适中
(0.65)
名校
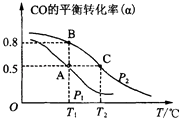
【推荐1】利用CO和H2合成甲醇,其反应的化学方程式为CO(g)+2H2(g)⇌CH3OH(g).今在一容积可变的密闭容器中,充有10mol CO和20mol H2用于合成甲醇.CO的平衡转化率(α)与温度(T)、压强(P)的关系如图所示:
(1)写出该反应的平衡常数表达式为__________________ .
(2)上述合成甲醇的反应为________ 反应(填“放热”或“吸热”). A、B、C三点的平衡常数KA、KB、KC的大小关系为____________ .A、B两点对应的压强大小关系是PA________ PB(填“大于”、“小于”或“等于”).
(3)若反应达到平衡状态A时,保持容器体积及体系温度不变,再向容器中充入2mol CO(g)、4molH2(g)、 2molCH3OH(g)则平衡向______ 方向移动(填“正”或“逆”)
(4)通常状况下取一定量的甲醇充分完全燃烧生成27克的水,放出热量544.35KJ,请写出表示甲醇燃烧热的热化学反应方程式_______________________________________ 。

(1)写出该反应的平衡常数表达式为
(2)上述合成甲醇的反应为
(3)若反应达到平衡状态A时,保持容器体积及体系温度不变,再向容器中充入2mol CO(g)、4molH2(g)、 2molCH3OH(g)则平衡向
(4)通常状况下取一定量的甲醇充分完全燃烧生成27克的水,放出热量544.35KJ,请写出表示甲醇燃烧热的热化学反应方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】对于密闭容器中的反应: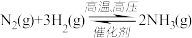 (正反应是放热反应),在673K,30MPa下
(正反应是放热反应),在673K,30MPa下 和
和 随时间变化的关系如图所示。
随时间变化的关系如图所示。
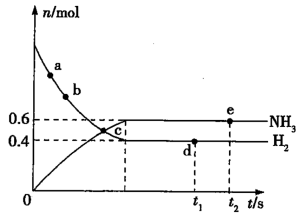
请回答下列问题:
(1)a点时正反应速率______ 逆反应速率;c点时正反应速率______ 逆反应速率。(填“ ”“
”“ ”或“
”或“ ”)
”)
(2)d点处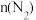
______ (填“ ”“
”“ ”或“
”或“ ”)e点处
”)e点处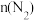 ,原因是
,原因是________________________ 。
(3)起始时加入氢气的物质的量为______ mol。
(4)若温度、压强不变,反应在加入催化剂条件下进行,在上图的基础上画出 和
和 随时间变化的关系图
随时间变化的关系图______ 。
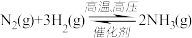 (正反应是放热反应),在673K,30MPa下
(正反应是放热反应),在673K,30MPa下 和
和 随时间变化的关系如图所示。
随时间变化的关系如图所示。
请回答下列问题:
(1)a点时正反应速率
 ”“
”“ ”或“
”或“ ”)
”)(2)d点处
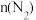
 ”“
”“ ”或“
”或“ ”)e点处
”)e点处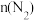 ,原因是
,原因是(3)起始时加入氢气的物质的量为
(4)若温度、压强不变,反应在加入催化剂条件下进行,在上图的基础上画出
 和
和 随时间变化的关系图
随时间变化的关系图
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】向一容积不变的密闭容器中充入一定量A和B,发生如下反应: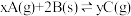 ;
; 。在一定条件下,容器中A、C的物质的量浓度随时间变化的曲线如下图。请回答下列问题:
。在一定条件下,容器中A、C的物质的量浓度随时间变化的曲线如下图。请回答下列问题:
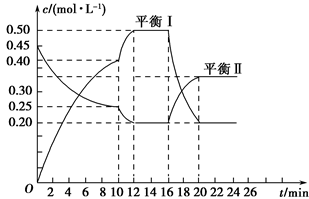
(1)用A的浓度变化表示该反应0~10 min内的平均反应速率v(A)=_____ ;达到平衡状态Ⅰ时A的转化率为_______ ;
(2)根据图示可确定x:y=___________ ;
(3)0~10 min容器内压强___________ (填“变大”,“不变”或“变小”)
(4)推测第10 min引起曲线变化的反应条件可能是_______ (填序号);第16 min引起曲线变化的反应条件可能是_____ (填序号);
①减压;②增大A的浓度;③增大C的量;④升温;⑤降温;⑥加催化剂
(5)能说明该反应达到化学平衡状态的是___________(填序号)
(6)能使该反应的反应速率增大,且平衡向正反应方向移动的是___________。
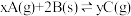 ;
; 。在一定条件下,容器中A、C的物质的量浓度随时间变化的曲线如下图。请回答下列问题:
。在一定条件下,容器中A、C的物质的量浓度随时间变化的曲线如下图。请回答下列问题:
(1)用A的浓度变化表示该反应0~10 min内的平均反应速率v(A)=
(2)根据图示可确定x:y=
(3)0~10 min容器内压强
(4)推测第10 min引起曲线变化的反应条件可能是
①减压;②增大A的浓度;③增大C的量;④升温;⑤降温;⑥加催化剂
(5)能说明该反应达到化学平衡状态的是___________(填序号)
| A.容器内压强不再改变 | B.c(A):c(C)=1:2 |
| C.气体密度不再改变 | D.v正(A)=2v逆(C) |
| A.及时分离出C气体 | B.适当升高温度 |
| C.增大A的浓度 | D.选择高效催化剂 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】反应A(g)+B(g)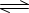 C(g)+D(g)过程中的能量变化如下图所示,回答下列问题。
C(g)+D(g)过程中的能量变化如下图所示,回答下列问题。
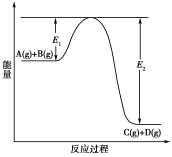
(1)该反应是________ 反应(填“吸热”或“放热”)。
(2)当反应达到平衡时,升高温度,A的转化率________ (填“增大”、“减小”或“不变”)
(3)反应体系中加入催化剂对反应热是否有影响?___________________________________ (填“有”、或“无”)
(4)在反应体系中加入催化剂,反应速率增大,E1和E2的变化是:E1________ ,E2________ (填“增大”、“减小”或“不变”)。
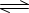 C(g)+D(g)过程中的能量变化如下图所示,回答下列问题。
C(g)+D(g)过程中的能量变化如下图所示,回答下列问题。
(1)该反应是
(2)当反应达到平衡时,升高温度,A的转化率
(3)反应体系中加入催化剂对反应热是否有影响?
(4)在反应体系中加入催化剂,反应速率增大,E1和E2的变化是:E1
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】工业合成氨,N2(g)+3H2(g)  2NH3(g)反应过程中的能量变化如图所示,据图回答问题:
2NH3(g)反应过程中的能量变化如图所示,据图回答问题:
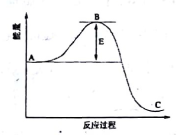
(1)该反应通常用活性铁作催化剂,加活性铁会使图中B点升高还是降低______ (填“升高”或“降低”或“不变”)理由是________________ 。
(2)该反应在恒温恒容条件下进行,下列选项一定能判断反应达到平衡状态的是________ 。
A.3v (N2)=v(H2)
B.单位时间内每消耗a mol N2的同时消耗3a molH2
C.单位时间内每断裂amol氮氮三键的同时生成3a mol氢氢单键
D.c(N2):c(H2):c(NH3)=1:3:2
E.气体总密度不变
F.气体平均摩尔质量不变
(3)该反应平衡常数表达式为:K=_______ ,当浓度商Q______ K(填“<”、 “>”或“=”)时,反应向右进行。
(4)450℃时该反应的平衡常数_______ 500℃时的平衡常数(填“<”、 “>”或“=”)。
(5)一定条件下的密闭容器中,该反应达到平衡,要提高H2的转化率,可以采取的合理措施有_____ (填字母代号)。
a.高温高压 b.加入催化剂 c.增加N2的浓度 d.增加H2的浓度 e.分离出NH3
 2NH3(g)反应过程中的能量变化如图所示,据图回答问题:
2NH3(g)反应过程中的能量变化如图所示,据图回答问题:
(1)该反应通常用活性铁作催化剂,加活性铁会使图中B点升高还是降低
(2)该反应在恒温恒容条件下进行,下列选项一定能判断反应达到平衡状态的是
A.3v (N2)=v(H2)
B.单位时间内每消耗a mol N2的同时消耗3a molH2
C.单位时间内每断裂amol氮氮三键的同时生成3a mol氢氢单键
D.c(N2):c(H2):c(NH3)=1:3:2
E.气体总密度不变
F.气体平均摩尔质量不变
(3)该反应平衡常数表达式为:K=
(4)450℃时该反应的平衡常数
(5)一定条件下的密闭容器中,该反应达到平衡,要提高H2的转化率,可以采取的合理措施有
a.高温高压 b.加入催化剂 c.增加N2的浓度 d.增加H2的浓度 e.分离出NH3
您最近一年使用:0次



