25. 用海水可同时生产氯化钠和金属镁或镁的化合物,其流程如下图所示:

36、在实验室中由粗盐“重结晶”制精盐的操作包括溶解、过滤、蒸发、
_________、洗涤等步骤;有关其中“蒸发”步骤的叙述错误的是
____________。
a. 蒸发的目的是得到热饱和溶液
b. 蒸发的目的是析出晶体
c. 应用余热蒸干溶液
d. 应蒸发至有较多晶体析出时为止
37、由MgCl
2溶液得到MgCl
2·6H
2O也需要蒸发,根据溶解度曲线,蒸发的目的是
_________。
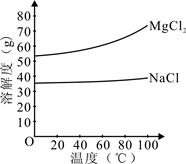
a. 得到热饱和溶液
b. 析出晶体
38、若在空气中加热MgCl
2·6H
2O,生成的是Mg(OH)Cl,写出反应的化学方程式:
___________________;用电解法制取金属镁时,需要无水氯化镁。在干燥的HCl气流中加热MgCl
2·6H
2O时,能得到无水MgCl
2,其原因是
_______________________________________________________________。
39、该流程产生的物质中,除Ca
2+能被海洋生物利用外,还需综合利用的物质是
_________。
40、MgCl
2可电解制Mg,MgO则是重要的耐火材料。在550℃时,MgCl
2·6H
2O会分解生成MgO、MgCl
2、HCl和水,若不补充其它原料,使一定量的MgCl
2·6H
2O全部生成a mol MgO、b mol MgCl
2和36.5%的盐酸,则a:b≈
______________(取整数值)。