19. 电子工业常用FeCl
3溶液腐蚀印刷电路板上不需要的铜箔,最后得到含FeCl
3、FeCl
2杂质的CuCl
2溶液。某化学兴趣小组设计下列方案,从该废液中 除去FeCl
3、FeCl
2杂质,制取纯净的CuCl
2。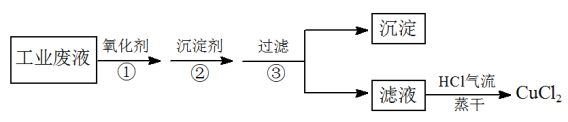
请回答下列问题:
(1)在①步操作中使用了氧化剂,下列氧化剂中一定不能使用的是
_______。
A.Cl
2 B.NaClO C.H
2O
2 D.KMnO
4 E.O
3(2)②步操作中的“沉淀剂”可以是下列中的
_______。
A.NaOH B.NH
3·H
2O C.CuO D.Cu
2(OH)
2CO
3 E.Fe
2O
3用一种你选择的沉淀剂,分步写出除去杂质的离子方程式:
_______。
(3)最后将滤液在HCl气流中蒸干,其目的是
_______,如果将滤液直接加热蒸干,最后得到的固体可能是
_______。
(4)设常温下各沉淀的溶度积近似为:K
sp[Cu(OH)
2]=10
-20、K
sp[Fe(OH)
3]=10
-38、K
sp[Fe(OH)
2]=10
-16;通常,人们把浓度小于10
-5mol/L的离子视为“不存在”。根据所给条件,完成下列问题:
①如果该废液中CuCl
2的浓度为1 mol/L,在加沉淀剂时应调节溶液的pH值范围为:
_______。
②如果对废液不先用氧化剂,而是直接加入沉淀剂,带来的后果是:
_______。