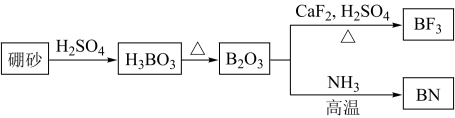
氮化硼(BN)是一种重要的功能陶瓷材料。以天然硼砂为起始物,经过一系列反应可以得到BF3和BN,如下图所示:
请回答下列问题:
(1)由B2O3制备BN的化学方程式是_____________________________________ ;
(2)B和N相比,电负性较大的是__________ ,BN中B元素的化合价为__________ ;
(3)在BF3分子中,F—B—F的键角是________ , B原子的杂化轨道类型为________ ;
(4)BF3和过量NaF作用可生成NaBF4,BF 的立体构型为
的立体构型为________ ;
(5)六方氮化硼与石墨相似,层内B原子与N原子之间的化学键为_________ ,N原子L层的P电子比S电子多_________ 个。
(6)写出CaF2的电子式:________ 。

请回答下列问题:
(1)由B2O3制备BN的化学方程式是
(2)B和N相比,电负性较大的是
(3)在BF3分子中,F—B—F的键角是
(4)BF3和过量NaF作用可生成NaBF4,BF
 的立体构型为
的立体构型为(5)六方氮化硼与石墨相似,层内B原子与N原子之间的化学键为
(6)写出CaF2的电子式:
更新时间:2016-12-09 07:50:36
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】我国科研工作者发现并制备了一系列主要由N、O、P、Se等元素组成的导电材料。回答下列问题:
(1) 三种元素中,电负性最小的元素名称是
三种元素中,电负性最小的元素名称是___________ ;键角:
___________  (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
(2)肼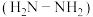 分子中孤电子对与
分子中孤电子对与 键的数目之比为
键的数目之比为___________ ,肼的相对分子质量与乙烯接近,但沸点远高于乙烯的原因是___________ 。
(3)正硝酸钠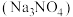 是一种重要的化工原料。
是一种重要的化工原料。 阴离子的空间结构为
阴离子的空间结构为___________ 形,其中心原子杂化方式为___________ 杂化。
(4)基态硒原子的价层电子排布式为___________ ; 晶体的熔点为
晶体的熔点为 ,加热易升华,固态
,加热易升华,固态 属于
属于___________ 晶体。
(1)
 三种元素中,电负性最小的元素名称是
三种元素中,电负性最小的元素名称是
 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。(2)肼
 分子中孤电子对与
分子中孤电子对与 键的数目之比为
键的数目之比为(3)正硝酸钠
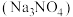 是一种重要的化工原料。
是一种重要的化工原料。 阴离子的空间结构为
阴离子的空间结构为(4)基态硒原子的价层电子排布式为
 晶体的熔点为
晶体的熔点为 ,加热易升华,固态
,加热易升华,固态 属于
属于
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐2】前四周期元素X、Y、Z、M、N、O、P,原子序数逐渐增大,其中X、Y、Z、M、N为短周期元素,而X、Y、Z、M处于同周期的P区,且未成对电子数之比为1:2:3:2;N与Z同族。O、P分别位于周期表第2、4列,P的单质被称为“未来金属”,具有质量轻、强度大、耐腐蚀性好的优点。
(1)Y、Z、M三种元素的电负性由大到小的顺序:________ (用元素符号表示)。
(2)M的常见氢化物的氢键的键能小于HF的氢键的键能,但Z的常见氢化物常温下为液态而HF常温下为气态的原因是:__________ 。
(3)XN一种耐磨涂料,可用于金属表面保护层,该化合物可由X的三溴化物和N的三溴化物于高温下在氢气的氛围中合成。
①写出合成XN的化学方程式:_________ 。(各物质用化学式表示)
②XN的晶体的晶胞如图所示:
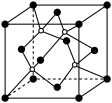
其中实心球为N,在一个晶胞中N原子空间堆积方式为______ ,N原子的配位数为______ ;该结构中有一个配位键,提供空轨道的原子是________ (写元素符号)。

(4)O和硫形成的某种晶体的晶胞如图a所示:该晶胞原子的坐标参数A为(0,0,0);B为(1,0,0)。则C原子的坐标参数为_______ 。
(5)图b为P的一种面心立方晶胞结构,若晶胞的边长为anm,则P的密度为_____ g·cm-3(用含a和NA的代数式表示)
(1)Y、Z、M三种元素的电负性由大到小的顺序:
(2)M的常见氢化物的氢键的键能小于HF的氢键的键能,但Z的常见氢化物常温下为液态而HF常温下为气态的原因是:
(3)XN一种耐磨涂料,可用于金属表面保护层,该化合物可由X的三溴化物和N的三溴化物于高温下在氢气的氛围中合成。
①写出合成XN的化学方程式:
②XN的晶体的晶胞如图所示:

其中实心球为N,在一个晶胞中N原子空间堆积方式为

(4)O和硫形成的某种晶体的晶胞如图a所示:该晶胞原子的坐标参数A为(0,0,0);B为(1,0,0)。则C原子的坐标参数为
(5)图b为P的一种面心立方晶胞结构,若晶胞的边长为anm,则P的密度为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】已知A、B、C、D、E、F、G都是元素周期表中短周期主族元素,它们的原子序数依次增大。A是周期表中原子半径最小的元素,D3B中阴、阳离子具有相同的电子层结构,B、C均可分别与A形成10个电子分子,B、C属同一周期,两者可以形成许多种共价化合物,C、F属同一主族,B原子最外电子层的p能级上的电子处于半满状态,C的最外层电子数是内层电子数的3倍,E最外层电子数比最内层多1。请用具体的元素回答下列问题:
(1)E元素原子基态电子排布式____________ 。
(2)用电子排布图表示F元素原子的价电子排布图________________ 。
(3)F、G元素对应的最高价含氧酸中酸性较强的分子式为_____________________ 。
(4)离子半径D+______ B3-,第一电离能B______ C,电负性C______ F(填“<”、“>”或“=”)。
(5)A、C形成的两种常见分子电子式_____________ ;_____________ (其中一种为绿色氧化剂)常见阴离子电子式为______________________ 。
(6)写出E与D的最高价氧化物对应的水化物反应的化学方程式______________ 。
(1)E元素原子基态电子排布式
(2)用电子排布图表示F元素原子的价电子排布图
(3)F、G元素对应的最高价含氧酸中酸性较强的分子式为
(4)离子半径D+
(5)A、C形成的两种常见分子电子式
(6)写出E与D的最高价氧化物对应的水化物反应的化学方程式
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】(物质结构与性质)CuCl和CuCl2都是重要的化工原料,常用作催化剂、颜料、防腐剂和消毒剂等。已知:
①CuCl可以由CuCl2用适当的还原剂如SO2、SnCl2等还原制得:
2Cu2++2Cl-+SO2+2H2O 2CuCl↓+4H++SO
2CuCl↓+4H++SO
2CuCl2+SnCl2=2CuCl↓+SnCl4
②CuCl2溶液与乙二胺(H2N-CH2-CH2-NH2)可形成配离子:
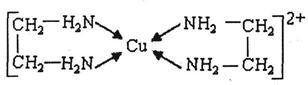
请回答下列问题:
(1)基态Cu原子的核外电子排布式为______ 。H、N、O三种元素的电负性由大到小的顺序是______ 。
(2)SO2分子的空间构型为______ 。与SnCl4互为等电子体的一种离子的化学式为______ 。
(3)乙二胺分子中氮原子轨道的杂化类型为______ 。乙二胺和三甲胺[N(CH3)3]均属于胺,但乙二胺比三甲胺的沸点高的多,原因是______ 。
(4)②中所形成的配离子中含有的化学键类型有______ 。(填字母)
a.配位键 b.极性键 c.离子键 d.非极性键
(5)CuCl的晶胞结构如图所示,其中Cl原子的配位数为______ 。
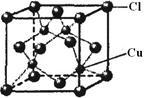
①CuCl可以由CuCl2用适当的还原剂如SO2、SnCl2等还原制得:
2Cu2++2Cl-+SO2+2H2O
 2CuCl↓+4H++SO
2CuCl↓+4H++SO
2CuCl2+SnCl2=2CuCl↓+SnCl4
②CuCl2溶液与乙二胺(H2N-CH2-CH2-NH2)可形成配离子:

请回答下列问题:
(1)基态Cu原子的核外电子排布式为
(2)SO2分子的空间构型为
(3)乙二胺分子中氮原子轨道的杂化类型为
(4)②中所形成的配离子中含有的化学键类型有
a.配位键 b.极性键 c.离子键 d.非极性键
(5)CuCl的晶胞结构如图所示,其中Cl原子的配位数为

您最近一年使用:0次
【推荐2】Fe3+与CN-、F-、有机分子等形成的化合物具有广泛的应用。
(1)Fe3+基态核外电子排布式为________ 。
(2)乙酰基二茂铁是常用汽油抗震剂,其结构如图甲所示。此物质中碳原子的杂化方式是__________ 。
(3)C、N、O原子的第一电离能由大到小的顺序是___________________________ 。
(4)配合物K3Fe(CN)6可用于电子传感器的制作。与配体互为等电子体的一种分子的化学式为________________ 。已知(CN)2是直线形分子,并具有对称性,则(CN)2中π键和σ键的个数比为__________________ 。
(5)F-不仅可与Fe3+形成3-,还可以与Mg2+、K+形成一种立方晶系的离子晶体,此晶体应用于激光领域,其结构如图乙所示,则该晶体的化学式为__________________________ 。

(1)Fe3+基态核外电子排布式为
(2)乙酰基二茂铁是常用汽油抗震剂,其结构如图甲所示。此物质中碳原子的杂化方式是
(3)C、N、O原子的第一电离能由大到小的顺序是
(4)配合物K3Fe(CN)6可用于电子传感器的制作。与配体互为等电子体的一种分子的化学式为
(5)F-不仅可与Fe3+形成3-,还可以与Mg2+、K+形成一种立方晶系的离子晶体,此晶体应用于激光领域,其结构如图乙所示,则该晶体的化学式为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐3】氮元素可形成氢化物、卤化物、氮化物、叠氮化物和配合物等多种化合物。
(1)肼(N2H4)可用作火箭燃料,其原理是N2O4(l)+2N2H4(l)=3N2(g)+4H2O(g),若反应中有4 mol N—H键断裂,则形成的π键有___________ mol。
(2)F2和过量NH3在铜催化作用下反应生成NF3,NF3分子的空间几何构型为___________ ,相比NH3,NF3分子作配体的能力___________ (选填“相当”、“更强”或“更弱”)。
(3)某FexNy的晶胞如图1所示,Cu可以完全替代该晶体中a位置Fe或者b位置Fe,形成Cu替代型产物Fe(x-n)CunNy。FexNy转化为两种Cu替代型产物的能量变化如图2 所示,其中更稳定的Cu替代型产物的化学式为___________

(4)叠氮化钠(NaN3)分解反应为2NaN3(s)=2Na(l)+3N2(g),写出与N 等电子体的一种化合物的分子式
等电子体的一种化合物的分子式___________ 。
(5)与N同主族的P、As有多种含氧酸,亚磷酸 、亚砷酸
、亚砷酸 ,酸性强弱比较:H3PO3
,酸性强弱比较:H3PO3___________ H3AsO3(选填“>”或“<”)
(1)肼(N2H4)可用作火箭燃料,其原理是N2O4(l)+2N2H4(l)=3N2(g)+4H2O(g),若反应中有4 mol N—H键断裂,则形成的π键有
(2)F2和过量NH3在铜催化作用下反应生成NF3,NF3分子的空间几何构型为
(3)某FexNy的晶胞如图1所示,Cu可以完全替代该晶体中a位置Fe或者b位置Fe,形成Cu替代型产物Fe(x-n)CunNy。FexNy转化为两种Cu替代型产物的能量变化如图2 所示,其中更稳定的Cu替代型产物的化学式为

(4)叠氮化钠(NaN3)分解反应为2NaN3(s)=2Na(l)+3N2(g),写出与N
 等电子体的一种化合物的分子式
等电子体的一种化合物的分子式(5)与N同主族的P、As有多种含氧酸,亚磷酸
 、亚砷酸
、亚砷酸 ,酸性强弱比较:H3PO3
,酸性强弱比较:H3PO3
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】氢氧化镍在乙醇的悬浊液中可发生反应生成单质镍的配合物:Ni(OH)2+5CH3NC=(CH3NC)4Ni+CH3NCO+H2O。
(1)基态镍原子的未成对电子数为__ ,钯(Pd)与镍位于同一族,且Pd是Ni的下一周期元素,基态钯原子的未成对电子数为0,基态钯原子的外围电子排布式为___ 。
(2)CH3NCO中四种元素的第一电离能由大到小的顺序为___ 。CH3NC(结构简式为CH3—N≡C)分子中甲基碳原子的杂化轨道类型是___ 。
(3)用光气(COCl2)与甲胺(CH3NH2)可以制取CH3NCO。与COCl2互为等电子体的一种阴离子为___ 。
(4)如图,在镍的催化作用下,甲基呋哺与氨在高温下反应得到甲基吡咯。甲基吡咯的熔、沸点高于甲基呋喃的原因是_____________ 。

(5)(CH3NC)4Ni可作为储氢材料,某种镁铝合金也可作为储氢材料,该合金晶胞结构如图所示,晶胞棱长为anm,该合金的化学式为___ ,该晶体的密度为__ g·cm-3(阿伏加 德罗常数的数值用NA表示)。

(1)基态镍原子的未成对电子数为
(2)CH3NCO中四种元素的第一电离能由大到小的顺序为
(3)用光气(COCl2)与甲胺(CH3NH2)可以制取CH3NCO。与COCl2互为等电子体的一种阴离子为
(4)如图,在镍的催化作用下,甲基呋哺与氨在高温下反应得到甲基吡咯。甲基吡咯的熔、沸点高于甲基呋喃的原因是

(5)(CH3NC)4Ni可作为储氢材料,某种镁铝合金也可作为储氢材料,该合金晶胞结构如图所示,晶胞棱长为anm,该合金的化学式为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】[化学——选修3:物质结构与性质]
具有自主知识产权、中国制造的C919,是一款与波音737MAX同等体量的民用飞机。制造C919需要大量的合金材料,其中包括钢,钢是现代社会的物质基础,钢中除含有铁外还含有碳和少量不可避免的硅、锰、磷、硫等元素。请回答下列有关问题:
(1)基态Mn原子的价电子排布式为___________ 。
(2)NO3-的立体构型名称为___________ ,其中心原子的杂化方式为___________ 。
(3)C、O、Si三种元素第一电离能由大到小的顺序是___________ 。
(4)写出和CN-互为等电子体的一种离子的电子式___________ 。
(5)铵盐大多易分解,NH4F和NH4Br两种盐中较易分解的是___________ (填化学式);理由是___________ 。
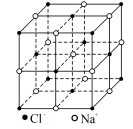
(6)氧化亚铁晶胞与NaCl的相似,NaCl的晶胞如图所示。由于晶体缺陷,某氧化亚铁晶体的实际组成为Fe0.9O,其中包含有Fe2+和Fe3+,晶胞边长为apm,该晶体的密度为ρg·cm-3,则a=___________ (列出计算式即可,用NA表示阿伏伽德罗常数的值)。
具有自主知识产权、中国制造的C919,是一款与波音737MAX同等体量的民用飞机。制造C919需要大量的合金材料,其中包括钢,钢是现代社会的物质基础,钢中除含有铁外还含有碳和少量不可避免的硅、锰、磷、硫等元素。请回答下列有关问题:
(1)基态Mn原子的价电子排布式为
(2)NO3-的立体构型名称为
(3)C、O、Si三种元素第一电离能由大到小的顺序是
(4)写出和CN-互为等电子体的一种离子的电子式
(5)铵盐大多易分解,NH4F和NH4Br两种盐中较易分解的是
(6)氧化亚铁晶胞与NaCl的相似,NaCl的晶胞如图所示。由于晶体缺陷,某氧化亚铁晶体的实际组成为Fe0.9O,其中包含有Fe2+和Fe3+,晶胞边长为apm,该晶体的密度为ρg·cm-3,则a=

您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
【推荐3】丙烯酸乙酯(D)是一种食品用合成香料,可用以下方法合成:

请回答:
(1)工业生产乙烯和丙烯主要来自于石油的______。
(2)乙烯的碳原子之间存在______ 、______ 键(从原子轨道重叠方式分析),乙烯中碳原子杂化方式为______ 。(填“sp”、“sp2”或“sp3”)
(3)反应①的类型____________ ,反应④的反应类型____________ 。
(4)医用口罩中的过滤层所用的材料是熔喷聚丙烯,请写出写出聚丙烯的结构简式____________ 。
(5)A+C→D的化学方程式为____________ 。
(6)B中的官能团名称______ 、______ ,并简述检验B中含氧官能团的化学方法:__________________ 。
(7)X是B的同分异构体,X能与Na反应且能使溴水褪色,写出一种X的结构简式为______ 。(已知羟基接在不饱和碳上的结构不稳定。)
(8)利用学过的知识,写出由乙烯(CH2=CH2)为原料制备 的合成路线(无机试剂任用)
的合成路线(无机试剂任用)
(合成路线常用的表示方式为:甲 乙 ∙∙∙∙∙∙
乙 ∙∙∙∙∙∙ 目标产物)
目标产物)____________ 。

请回答:
(1)工业生产乙烯和丙烯主要来自于石油的______。
| A.干馏 | B.分馏 | C.裂化 | D.裂解 |
(2)乙烯的碳原子之间存在
(3)反应①的类型
(4)医用口罩中的过滤层所用的材料是熔喷聚丙烯,请写出写出聚丙烯的结构简式
(5)A+C→D的化学方程式为
(6)B中的官能团名称
(7)X是B的同分异构体,X能与Na反应且能使溴水褪色,写出一种X的结构简式为
(8)利用学过的知识,写出由乙烯(CH2=CH2)为原料制备
 的合成路线(无机试剂任用)
的合成路线(无机试剂任用)(合成路线常用的表示方式为:甲
 乙 ∙∙∙∙∙∙
乙 ∙∙∙∙∙∙ 目标产物)
目标产物)
您最近一年使用:0次



