有关晶体的结构如图所示,下列说法中不正确的是 ( )
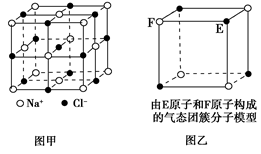
| A.在NaCl晶体(图甲)中,距Na+最近的Cl-形成正八面体 |
| B.该气态团簇分子(图乙)的分子式为EF或FE |
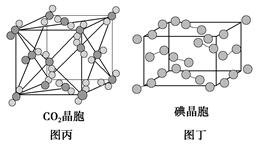
| C.在CO2晶体(图丙)中,一个CO2分子周围有12个CO2分子紧邻 |
| D.在碘晶体(图丁)中,碘分子的排列有两种不同的方向 |
14-15高二下·福建福州·阶段练习 查看更多[8]
更新时间:2016-12-09 07:57:47
|
相似题推荐
【推荐1】钛酸钙是典型的钙钛矿型化合物,该类化合物具有特殊的理化性质,比如吸光性、电催化性等,其晶体结构如图所示。下列说法正确的是

| A.基态钛原子价电子排布式为4s23d2 |
| B.钛酸钙的化学式为CaTiO2 |
| C.每个晶胞中含有8个Ca2+ |
| D.每个Ca2+周围距离最近且等距的O2-有12个 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列说法中不正确的是


| A.水合铜离子为如图1所示的平面结构,可知Cu发生的不是sp3杂化 |
| B.CaF2晶体的晶胞如图2所示,每个晶胞平均占有4个Ca2+ |
| C.H原子的电子云图如图3所示,H原子核外电子在原子核外做圆周运动 |
| D.某气态团簇分子结构如图4所示,该气态团簇分子的分子式是E4F4或F4E4 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐1】晶体的叙述中,正确的是
| A.原子晶体中,共价键的键能越大,熔、沸点越高 |
| B.分子晶体中,分子间的作用力越大,该分子越稳定 |
| C.分子晶体中,共价键的键能越大,熔、沸点越高 |
| D.离子晶体不一定能溶于水,但一定不含非极性共价键 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐2】有关晶体的下列说法正确的是
| A.晶体中分子间作用力越大,分子越稳定 |
| B.分子中共价键越强,该物质熔点越高 |
| C.铁熔化时金属键被破坏 |
| D.氯化钠溶于水时离子键未被破坏 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】根据表给出的几种物质的熔沸点数据,判断下列说法中错误的是
| 晶体 | NaCl | MgCl2 | AlCl3 | SiCl4 | 单质R |
熔点/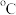 | 801 | 714 | 190 | -70 | 2300 |
沸点/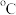 | 1465 | 1418 | 177.8 | 57 | 2500 |
| A.SiCl4和A1Cl3都是分子晶体 ,熔融状态下不导电 |
| B.MgCl2和NaCl都是离子晶体,熔融状态能导电且易溶于水 |
| C.若单质R是原子晶体,其熔沸点的高低是由共价键的键能决定的 |
| D.固态时可导电的一定是金属晶体 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列物质的熔点高低顺序,正确的是
| A.金刚石>晶体硅>碳化硅 | B.K>Na>Li |
| C.NaF<NaCl<NaBr | D.CI4>CBr4>CCl4>CH4 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】物质的性质决定用途,下列两者对应关系不正确的是
| A.二氧化硫具有漂白性,食品中添加适量的SO2有防腐和抗氧化作用 |
| B.氯化铁溶液有氧化性,可用于蚀刻不锈钢广告牌上的图形 |
| C.生铁硬度大,抗压性强,可用于铸造机器底座 |
| D.新型陶瓷碳化硅(SiC)硬度很大,可用作砂纸和砂轮的磨料 |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】工业上常用反应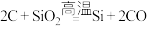 制备粗硅,若碳过量还会生成SiC,下列说法不正确的是
制备粗硅,若碳过量还会生成SiC,下列说法不正确的是
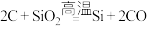 制备粗硅,若碳过量还会生成SiC,下列说法不正确的是
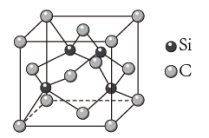
制备粗硅,若碳过量还会生成SiC,下列说法不正确的是| A.相对分子质量:C60>SiO2>SiC,因此熔沸点:C60>SiO2>SiC |
B. 中 中 的化合价为 的化合价为 价, 价, 中C的化合价为 中C的化合价为 价,因此 价,因此 还原性强于 还原性强于 |
C.Si原子间难形成双键而C原子间可以,是因为 的原子半径大于C,难形成 的原子半径大于C,难形成 键 键 |
| D.键能:Si-H<C-H,Si-Si<C-C,因此硅烷的种类和数量远不如烷烃的多 |
您最近半年使用:0次

 的熔沸点比
的熔沸点比 高
高 溶液中滴加盐酸产生白色凝胶
溶液中滴加盐酸产生白色凝胶 平衡正移
平衡正移 和
和 混合气体体积,红棕色变深
混合气体体积,红棕色变深

