选考[化学与技术]根据废水中所含有害物质的不同,工业上有多种废水的处理方法。
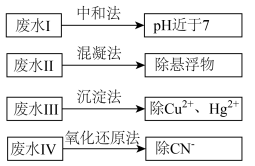
(1)废水I若采用CO2处理,离子方程式是___________ 。
(2)废水Ⅱ常用明矾处理。实践中发现废水中的c(HCO )越大,净水效果越好,这是因为
)越大,净水效果越好,这是因为___________ 。
(3)③废水Ⅲ中的汞元素存在如下转化(在空格上填相应的化学式):Hg2++___________ ═CH3Hg++___________ ;我国规定,Hg2+的排放标准不能超过0.05mg/L。对于含Hg2+的污水,可加入沉淀剂___________ (填写化学式),使Hg2+除去,降低污染。
(4)④废水Ⅳ常用Cl2氧化CN-成CO2和N2,若参加反应的Cl2与CN-的物质的量之比为5:2,则该反应的离子方程式为___________ 。
化学需氧量(COD)可量度水体受有机物污染的程度,它是指在一定条件下,用强氧化剂处理水样时所消耗的氧化剂的量,换算成氧的含量(以mg/L计)。某研究性学习小组测定某水样的化学需氧量(COD),过程如下:
Ⅰ.取V1 mL水样于锥形瓶,加入10.00mL 0.2500mol/L K2Cr2O7溶液。
Ⅱ.加碎瓷片少许,然后慢慢加入硫酸酸化,混合均匀,加热。
Ⅲ.反应完毕后,冷却,加指示剂,用c mol/L的硫酸亚铁铵[(NH4)2Fe(SO4)2]溶液滴定。终点时消耗硫酸亚铁铵溶液V2 mL。
(5)I中,量取K2Cr2O7,溶液的仪器是___________ 。
(6)Ⅲ中,发生的反应为:Cr2O +6Fe2++14H+═2Cr3++6Fe3+7H2O由此可知,该水样的化学需氧量COD=
+6Fe2++14H+═2Cr3++6Fe3+7H2O由此可知,该水样的化学需氧量COD=___________ (用含c、V1、V2的表达式表示)。

(1)废水I若采用CO2处理,离子方程式是
(2)废水Ⅱ常用明矾处理。实践中发现废水中的c(HCO
 )越大,净水效果越好,这是因为
)越大,净水效果越好,这是因为(3)③废水Ⅲ中的汞元素存在如下转化(在空格上填相应的化学式):Hg2++
(4)④废水Ⅳ常用Cl2氧化CN-成CO2和N2,若参加反应的Cl2与CN-的物质的量之比为5:2,则该反应的离子方程式为
化学需氧量(COD)可量度水体受有机物污染的程度,它是指在一定条件下,用强氧化剂处理水样时所消耗的氧化剂的量,换算成氧的含量(以mg/L计)。某研究性学习小组测定某水样的化学需氧量(COD),过程如下:
Ⅰ.取V1 mL水样于锥形瓶,加入10.00mL 0.2500mol/L K2Cr2O7溶液。
Ⅱ.加碎瓷片少许,然后慢慢加入硫酸酸化,混合均匀,加热。
Ⅲ.反应完毕后,冷却,加指示剂,用c mol/L的硫酸亚铁铵[(NH4)2Fe(SO4)2]溶液滴定。终点时消耗硫酸亚铁铵溶液V2 mL。
(5)I中,量取K2Cr2O7,溶液的仪器是
(6)Ⅲ中,发生的反应为:Cr2O
 +6Fe2++14H+═2Cr3++6Fe3+7H2O由此可知,该水样的化学需氧量COD=
+6Fe2++14H+═2Cr3++6Fe3+7H2O由此可知,该水样的化学需氧量COD=
更新时间:2016-12-09 08:08:41
|
相似题推荐
【推荐1】碘元素是人体必需的微量元素,某研究小组为了检测加碘盐中是否含有KIO3,进行如下实验:取少量加碘盐溶于水中,然后加入稀硫酸和KI 溶液,最后加入一定量的CCl4,振荡后静置,观察到溶液分成两层,上层呈无色,下层呈紫红色。据此回答下列问题:
(1)KIO3中钾元素位于元素周期表第_______ 周期__________ 族。
(2)实验中发生反应的离子方程式为______________________________ ,其中还原产物与氧化产物的质量之比为______________ 。
(3)某学生在一次分液操作中发现上下层液体都是无色的,请用简单的方法帮他鉴别哪一层是有机层,哪一层是水层:___________________________________________________ (写出有关步骤及判断)。
(1)KIO3中钾元素位于元素周期表第
(2)实验中发生反应的离子方程式为
(3)某学生在一次分液操作中发现上下层液体都是无色的,请用简单的方法帮他鉴别哪一层是有机层,哪一层是水层:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】Ⅰ、已知Mg与HNO3反应的化学方程式如下(未配平):
___________Mg+___________HNO3(稀)=___________Mg(NO3)2+___________NO↑+___________H2O
(1)请配平上述化学方程式,并用双线桥法表示电子转移的方向和数目___________ 。
(2)把上述化学方程式改写成离子方程式___________ 。
(3)该反应中,氧化剂是___________ ,还原产物是___________ ,n(氧化剂)︰n(还原剂)=___________ 。
(4)HNO3在上述反应中显示出来的性质是___________。
(5)当转移1.806×1023个电子时,生成的NO气体的体积(标准状况下)为___________ 。
Ⅱ、Mn2+、Bi3+、BiO 、MnO
、MnO 、H+、H2O组成的一个氧化还原反应体系中,发生BiO
、H+、H2O组成的一个氧化还原反应体系中,发生BiO →Bi3+的反应过程。
→Bi3+的反应过程。
(6)该反应中,被氧化的元素是___________ ,氧化剂是___________ 。
(7)将以上物质分别填入下面对应的横线上,组成一个未配平的化学方程式:___________ 。·
___________+___________+___________→___________+___________+H2O
___________Mg+___________HNO3(稀)=___________Mg(NO3)2+___________NO↑+___________H2O
(1)请配平上述化学方程式,并用双线桥法表示电子转移的方向和数目
(2)把上述化学方程式改写成离子方程式
(3)该反应中,氧化剂是
(4)HNO3在上述反应中显示出来的性质是___________。
| A.氧化性 | B.还原性 | C.酸性 | D.碱性 |
Ⅱ、Mn2+、Bi3+、BiO
 、MnO
、MnO 、H+、H2O组成的一个氧化还原反应体系中,发生BiO
、H+、H2O组成的一个氧化还原反应体系中,发生BiO →Bi3+的反应过程。
→Bi3+的反应过程。(6)该反应中,被氧化的元素是
(7)将以上物质分别填入下面对应的横线上,组成一个未配平的化学方程式:
___________+___________+___________→___________+___________+H2O
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】溶液常 用作氧化还原反应滴定的标准液,利用
用作氧化还原反应滴定的标准液,利用 氧化
氧化 制备
制备 的装置如图所示(加热、夹持装置略):
的装置如图所示(加热、夹持装置略):
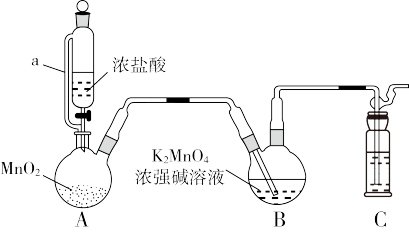
已知: 在浓强碱溶液中可稳定存在,碱性减弱时易发生反应:
在浓强碱溶液中可稳定存在,碱性减弱时易发生反应:
回答下列问题:
(1) 的化学名称为
的化学名称为_______ 。
(2)装置A中所发生反应的化学方程式为_______ ;其中a的作用是_______ 。
(3)装置C中盛装的试剂是_______ 。
(4)分析发现该装置有不足之处,改进的方法是_______ 。
(5)为测定某 固体的纯度,现用
固体的纯度,现用 的酸性
的酸性 溶液进行滴定。(已知:
溶液进行滴定。(已知: )称取
)称取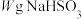 固体溶于水配成500mL溶液,取
固体溶于水配成500mL溶液,取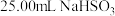 溶液置于锥形瓶中,用
溶液置于锥形瓶中,用 溶液滴定至终点,消耗
溶液滴定至终点,消耗 溶液V mL。滴定终点的现象为
溶液V mL。滴定终点的现象为_______ , 固体的纯度为
固体的纯度为_______ 。
 用作氧化还原反应滴定的标准液,利用
用作氧化还原反应滴定的标准液,利用 氧化
氧化 制备
制备 的装置如图所示(加热、夹持装置略):
的装置如图所示(加热、夹持装置略):
已知:
 在浓强碱溶液中可稳定存在,碱性减弱时易发生反应:
在浓强碱溶液中可稳定存在,碱性减弱时易发生反应:
回答下列问题:
(1)
 的化学名称为
的化学名称为(2)装置A中所发生反应的化学方程式为
(3)装置C中盛装的试剂是
(4)分析发现该装置有不足之处,改进的方法是
(5)为测定某
 固体的纯度,现用
固体的纯度,现用 的酸性
的酸性 溶液进行滴定。(已知:
溶液进行滴定。(已知: )称取
)称取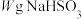 固体溶于水配成500mL溶液,取
固体溶于水配成500mL溶液,取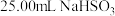 溶液置于锥形瓶中,用
溶液置于锥形瓶中,用 溶液滴定至终点,消耗
溶液滴定至终点,消耗 溶液V mL。滴定终点的现象为
溶液V mL。滴定终点的现象为 固体的纯度为
固体的纯度为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】配平下列方程式:
(1) ____P+____Br2+____H2O=____H3PO4+____HBr________
(2) ___KMnO4+___HCl(浓)=___KCl+___MnCl2+___Cl2↑+___H2O r________
(3)___FeSO4 + ___H2O + ___O2 = ___Fe2(SO4)3 + ___Fe(OH)3 r________
(1) ____P+____Br2+____H2O=____H3PO4+____HBr
(2) ___KMnO4+___HCl(浓)=___KCl+___MnCl2+___Cl2↑+___H2O r
(3)___FeSO4 + ___H2O + ___O2 = ___Fe2(SO4)3 + ___Fe(OH)3 r
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】钴(Co)合金广泛应用于机械制造等领域。
(1)在 表面促进
表面促进 还原
还原 的反应历程如图所示:
的反应历程如图所示:

①该反应中 的作用是
的作用是___________ 。
②写出整个历程中发生的总反应式:___________ ;该反应中氧化剂与还原剂的物质的量之比为___________ 。
(2)燃料电池具有安全、高效的特点。一种以固体氧化物作为电解质的 燃料电池的工作原理示意图如图所示。
燃料电池的工作原理示意图如图所示。

①放电时,电池的负极是___________ (填“电极a”或“电极b”);外电路中电子的流动向为___________ (填“电极a到电极b”或“电极b到电极a”)。
(1)在
 表面促进
表面促进 还原
还原 的反应历程如图所示:
的反应历程如图所示:
①该反应中
 的作用是
的作用是②写出整个历程中发生的总反应式:
(2)燃料电池具有安全、高效的特点。一种以固体氧化物作为电解质的
 燃料电池的工作原理示意图如图所示。
燃料电池的工作原理示意图如图所示。
①放电时,电池的负极是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】向ZnSO4溶液中滴加饱和H2S溶液,没有沉淀生成,继续滴加一定量的氨水后,生成ZnS沉淀。用电离平衡原理解释上述现象_____ 。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】表为几种弱电解质的电离平衡常数、难溶电解质的溶度积Ksp (25℃)。
回答下列问题:
(1)由表分析,若①CH3COOH ②HCO ③C6H5OH ④H2PO
③C6H5OH ④H2PO 均可看作酸,则它们酸性由强到弱的顺序为
均可看作酸,则它们酸性由强到弱的顺序为_______ (须填编号);
(2)写出C6H5OH与Na3PO4反应的离子方程式:_______ ;
(3)25℃时,将等体积等浓度的醋酸和氨水混合,混合液中:c(CH3COO-)_______ c(NH );(填“>”、“=”或“<”)
);(填“>”、“=”或“<”)
(4)25℃时,向10ml 0.01mol/L苯酚溶液中滴加Vml 0.01mol/L氨水,混合溶液中粒子浓度关系正确的是_______ ;
A.若混合液pH>7,则V≥10
B.若混合液pH<7,则c((NH ) >c (C6H5O-) >c (H+)>c (OH-)
) >c (C6H5O-) >c (H+)>c (OH-)
C.V=10时,混合液中水的电离程度小于10ml 0.01mol/L苯酚溶液中水的电离程度
D.V=5时,2c(NH3·H2O)+ 2c(NH )= c (C6H5O-)+ c(C6H5OH)
)= c (C6H5O-)+ c(C6H5OH)
(5)水解反应是典型的可逆反应.水解反应的化学平衡常数称为水解常数(用Kh表示),类比化学平衡常数的定义,请写出Na2CO3第一步水解反应的水解常数的表达式_______ 。
(6)Ⅰ.如图所示,有T1、T2两种温度下两条BaSO4在水中的沉淀溶解平衡曲线,回答下列问题:

① T1_______ T2(填>、=、<),T2温度时Ksp(BaSO4)=_______ ;
②讨论T1温度时BaSO4的沉淀溶解平衡曲线,下列说法正确的是_______
A.加入Na2SO4可使溶液由a点变为b点
B.在T1曲线上方区域(不含曲线)任意一点时,均有BaSO4沉淀生成
C.蒸发溶剂可能使溶液由d点变为曲线上a、b之间的某一点(不含a、b)
D.升温可使溶液由b点变为d点
Ⅱ.现有0.2mol的BaSO4沉淀,每次用1L饱和Na2CO3溶液(浓度为1.7mol/L)处理。若使BaSO4中的SO 全部转化到溶液中,需要反复处理
全部转化到溶液中,需要反复处理_______ 次。[提示: BaSO4(s)+ CO (aq)⇌BaCO3(s)+ SO
(aq)⇌BaCO3(s)+ SO (aq)]
(aq)]
| 电解质 | 平衡方程式 | 平衡常数K | Ksp |
| CH3COOH | CH3COOH⇌CH3COO-+H+ | 1.76×10-5 | |
| H2CO3 | H2CO3⇌H++HCO HCO  ⇌H++CO ⇌H++CO | K1=4.31×10-7 K2=5.61×10-11 | |
| C6H5OH | C6H5OH⇌C6H5O-+H+ | 1.1×10-10 | |
| H3PO4 | H3PO4⇌H++H2PO H2PO  ⇌H++HPO ⇌H++HPO HPO  ⇌H++PO ⇌H++PO | K1=7.52×10-3 K2=6.23×10-8 K3=2.20×10-13 | |
NH3 H2O H2O | NH3 H2O⇌NH H2O⇌NH +OH- +OH- | 1.76×10-5 | |
| BaSO4 | BaSO4⇌Ba2++SO | 1.07×10-10 | |
| BaCO3 | BaCO3⇌ Ba2++CO | 2.58×10-9 |
回答下列问题:
(1)由表分析,若①CH3COOH ②HCO
 ③C6H5OH ④H2PO
③C6H5OH ④H2PO 均可看作酸,则它们酸性由强到弱的顺序为
均可看作酸,则它们酸性由强到弱的顺序为(2)写出C6H5OH与Na3PO4反应的离子方程式:
(3)25℃时,将等体积等浓度的醋酸和氨水混合,混合液中:c(CH3COO-)
 );(填“>”、“=”或“<”)
);(填“>”、“=”或“<”)(4)25℃时,向10ml 0.01mol/L苯酚溶液中滴加Vml 0.01mol/L氨水,混合溶液中粒子浓度关系正确的是
A.若混合液pH>7,则V≥10
B.若混合液pH<7,则c((NH
 ) >c (C6H5O-) >c (H+)>c (OH-)
) >c (C6H5O-) >c (H+)>c (OH-)C.V=10时,混合液中水的电离程度小于10ml 0.01mol/L苯酚溶液中水的电离程度
D.V=5时,2c(NH3·H2O)+ 2c(NH
 )= c (C6H5O-)+ c(C6H5OH)
)= c (C6H5O-)+ c(C6H5OH)(5)水解反应是典型的可逆反应.水解反应的化学平衡常数称为水解常数(用Kh表示),类比化学平衡常数的定义,请写出Na2CO3第一步水解反应的水解常数的表达式
(6)Ⅰ.如图所示,有T1、T2两种温度下两条BaSO4在水中的沉淀溶解平衡曲线,回答下列问题:

① T1
②讨论T1温度时BaSO4的沉淀溶解平衡曲线,下列说法正确的是
A.加入Na2SO4可使溶液由a点变为b点
B.在T1曲线上方区域(不含曲线)任意一点时,均有BaSO4沉淀生成
C.蒸发溶剂可能使溶液由d点变为曲线上a、b之间的某一点(不含a、b)
D.升温可使溶液由b点变为d点
Ⅱ.现有0.2mol的BaSO4沉淀,每次用1L饱和Na2CO3溶液(浓度为1.7mol/L)处理。若使BaSO4中的SO
 全部转化到溶液中,需要反复处理
全部转化到溶液中,需要反复处理 (aq)⇌BaCO3(s)+ SO
(aq)⇌BaCO3(s)+ SO (aq)]
(aq)]
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】FeS2、FeS在空气中易被氧化,将FeS2在空气中氧化,测得氧化过程中剩余固体的质量与起始FeS2的质量的比值随温度变化的曲线如图所示。800℃时,FeS2氧化成含有两种元素的固体产物为_______ (填化学式)。


您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】化学科学在药物的开发、合成和使用中起着至关重要的作用。如小苏打、氢氧化铝、三硅酸镁等可治疗胃酸过多,硫酸亚铁可补铁、防治贫血。试回答下列问题:
(1)写出小苏打与胃酸(主要成分为稀盐酸)作用的离子方程式:_________ 。
(2)现有一瓶胃舒平药片(复方氢氧化铝),请设计实验验证其主要成分。(写出实验步骤和实验现象):将药片碾碎,_______ 则说明其主要成分为氢氧化铝。
(3)自选合适的氧化剂,将补铁剂中的Fe2+氧化成Fe3+,写出相关的离子反应方程式:_______ 检验Fe3+常用的试剂除碱外,还可以用_______ (填化学式),现象是_______ 。
(1)写出小苏打与胃酸(主要成分为稀盐酸)作用的离子方程式:
(2)现有一瓶胃舒平药片(复方氢氧化铝),请设计实验验证其主要成分。(写出实验步骤和实验现象):将药片碾碎,
(3)自选合适的氧化剂,将补铁剂中的Fe2+氧化成Fe3+,写出相关的离子反应方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】水中溶解氧是水生生物生存不可缺少的条件。某课外小组采用碘量法测定学校周边河水中的溶解氧。实验步骤及测定原理如下:
Ⅰ.取样、氧的固定
用溶解氧瓶采集水样。记录大气压及水体温度。将水样与Mn(OH)2碱性悬浊液(含有KI)混合,反应生成MnO(OH)2,实现氧的固定。
Ⅱ.酸化,滴定
将固氧后的水样酸化,MnO(OH)2被I−还原为Mn2+,在暗处静置5 min,然后用标准Na2S2O3溶液滴定生成的I2(2 S2O32−+I2=2I−+ S4O62−)。
回答下列问题:
(1)“氧的固定”中发生反应的化学方程式为__________________________________ 。
(2)Na2S2O3溶液不稳定,使用前需标定。配制该溶液时需要的玻璃仪器有烧杯、玻璃棒、试剂瓶、胶头滴管和______________ ;蒸馏水必须经过煮沸、冷却后才能使用,其目的是杀菌、除_______ 及二氧化碳。
(3)取100.00 mL水样经固氧、酸化后,用a mol·L−1Na2S2O3溶液滴定,以淀粉溶液作指示剂,终点现象为__________________________________ ;若消耗Na2S2O3溶液的体积为b mL,则水样中溶解氧的含量为___________________ mg·L−1。
Ⅰ.取样、氧的固定
用溶解氧瓶采集水样。记录大气压及水体温度。将水样与Mn(OH)2碱性悬浊液(含有KI)混合,反应生成MnO(OH)2,实现氧的固定。
Ⅱ.酸化,滴定
将固氧后的水样酸化,MnO(OH)2被I−还原为Mn2+,在暗处静置5 min,然后用标准Na2S2O3溶液滴定生成的I2(2 S2O32−+I2=2I−+ S4O62−)。
回答下列问题:
(1)“氧的固定”中发生反应的化学方程式为
(2)Na2S2O3溶液不稳定,使用前需标定。配制该溶液时需要的玻璃仪器有烧杯、玻璃棒、试剂瓶、胶头滴管和
(3)取100.00 mL水样经固氧、酸化后,用a mol·L−1Na2S2O3溶液滴定,以淀粉溶液作指示剂,终点现象为
您最近一年使用:0次

 的目的是生成
的目的是生成 沉淀除去
沉淀除去 。若溶液酸度过高,
。若溶液酸度过高,

