物质A—J间的转化关系如下图所示,A、C为金属氧化物,其中A为红棕色粉末,B、D是生活中常见金属单质,F、J是难溶于水的白色化合物,G、J受热后容易分解。
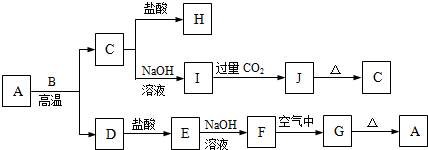
(1)A的化学式是________ ,A与B反应的反应类型是_________ (填基本反应类型)。
(2)C→I反应的离子方程式是___________________ 。
(3)J→C反应的化学方程式是___________________ 。
(4)F转化为G的过程中观察到的现象是________________ ,反应的化学方程式是_______________ 。

(1)A的化学式是
(2)C→I反应的离子方程式是
(3)J→C反应的化学方程式是
(4)F转化为G的过程中观察到的现象是
更新时间:2016/12/09 11:15:59
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】下列A—L 11种物质是中学化学常见物质,其中C、D、E、F为气体,C、D、H为单质。E、F含有两种相同的元素,G为红棕色粉末。它们有如下图所示的转化关系(部分反应中的生成物已略去)
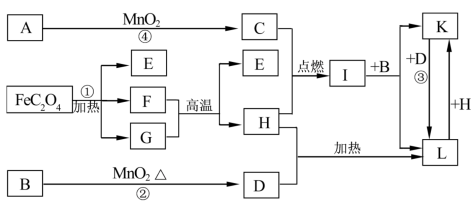
(1)写出有关物质的化学式:G___________ 。
(2)写出反应③中的离子方程式___________ 。
(3)写出检验L中阳离子的最合适试剂是___________ 。(填化学式)
(4)MnO2在反应②和④中的作用分别是___________ 、___________ 。
(5)写出向K的溶液中滴加NaOH溶液的现象为___________ ,此过程中发生的氧化还原反应为___________ 。(用化学方程式表达)

(1)写出有关物质的化学式:G
(2)写出反应③中的离子方程式
(3)写出检验L中阳离子的最合适试剂是
(4)MnO2在反应②和④中的作用分别是
(5)写出向K的溶液中滴加NaOH溶液的现象为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】如图是有关物质相互转化的关系图,其中A俗称铁红,甲为强酸,乙为还原性气体,丙为强碱溶液,G为红褐色沉淀,I的颜色呈浅绿色。
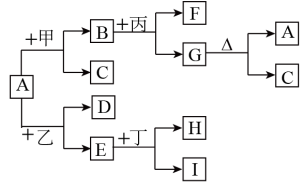
(1)若F是由Na+和SO42﹣组成的溶液,则甲的化学式是_______ ,列举A物质的一种用途_______ 。
(2)若D是能使澄清石灰水变浑浊的气体,则乙的化学式为_______ ,丁属于单质、酸、碱中的_______ ;在I溶液中加入氢氧化钠溶液,可以观察到的现象是_______ ,对应的离子方程式和化学方程式依次是_______ 。
(3)写出G→A+C的化学方程式:_______ 。
(4)写出E和C反应的方程式并用单线桥法标明电子的转移方向和数目:_______ 。
(5)若A中混有杂质Al2O3,除去杂质的方法是加入过量的_______ ,该反应的离子方程式为_______ 。
(6)由E和A组成的混合物与稀H2SO4作用,固体恰好溶解,所得溶液中不含Fe3+,且生成的Fe2+与H2的物质的量之比为4:1。则反应物中A、E、H2SO4的物质的量之比为_______ 。

(1)若F是由Na+和SO42﹣组成的溶液,则甲的化学式是
(2)若D是能使澄清石灰水变浑浊的气体,则乙的化学式为
(3)写出G→A+C的化学方程式:
(4)写出E和C反应的方程式并用单线桥法标明电子的转移方向和数目:
(5)若A中混有杂质Al2O3,除去杂质的方法是加入过量的
(6)由E和A组成的混合物与稀H2SO4作用,固体恰好溶解,所得溶液中不含Fe3+,且生成的Fe2+与H2的物质的量之比为4:1。则反应物中A、E、H2SO4的物质的量之比为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】A、B、C为中学常见单质,其中一种为金属;通常情况下A为固体、B为黄绿色气体、C为无色气体。D、E、F、G、H、X均为化合物,其中X常温下是无色气体,其水溶液是一种无氧强酸溶液,E为黑色固体,H在常温下为液体。它们之间的转化如图所示(某些反应条件和部分反应产物已略去)。

(1)写出下列物质的化学式:D____________ X_______________ 。
(2)反应⑥的离子方程式为:___________________________ 。
(3)往G溶液中加入NaOH溶液观察到的现象是__________________ 。
(4)反应⑦的化学方程式为_____________________________________ ;
反应③的化学方程式为_____________________________________ ;
(5)除去G溶液中混有的少量D的方法是:_______________________________ 。

(1)写出下列物质的化学式:D
(2)反应⑥的离子方程式为:
(3)往G溶液中加入NaOH溶液观察到的现象是
(4)反应⑦的化学方程式为
反应③的化学方程式为
(5)除去G溶液中混有的少量D的方法是:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】氢氧化铝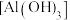 是重要的化工原料,也是用量最大和应用最广的无机阻燃添加剂,钼酸钠
是重要的化工原料,也是用量最大和应用最广的无机阻燃添加剂,钼酸钠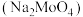 具有广泛的用途,可作新型阻燃剂、水处理剂和无公害型冷却水系统的金属抑制剂等。现从某废钼催化剂
具有广泛的用途,可作新型阻燃剂、水处理剂和无公害型冷却水系统的金属抑制剂等。现从某废钼催化剂 主要成分
主要成分 、
、 、
、 等
等 中回收
中回收 和
和 ,其工艺流程如图:
,其工艺流程如图:
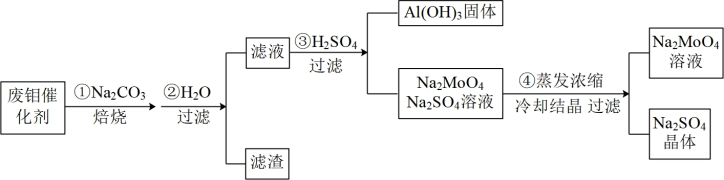
回答下列问题:
(1)已知 、
、 与
与 相似,均能在高温下跟
相似,均能在高温下跟 发生类似的反应,试写出①焙烧时
发生类似的反应,试写出①焙烧时 跟
跟 反应的化学方程式:
反应的化学方程式:___________ 。
(2)检验②操作后所得的滤渣中含有 的方法是:
的方法是:___________
(3)第③步操作中加入 需要适量,可以通过测定溶液
需要适量,可以通过测定溶液___________ 来控制 的用量。该步操作中制备
的用量。该步操作中制备 的离子方程式为
的离子方程式为___________
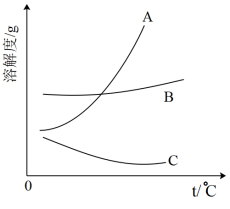
(4)从题目信息可知,下图曲线___________  填序号
填序号 为
为 的溶解度曲线。
的溶解度曲线。
(5)利用铝热反应可以回收金属钼。将所得钼酸钠溶液用酸处理得到沉淀,再加热可得 。写出
。写出 发生铝热反应的化学方程式:
发生铝热反应的化学方程式:___________
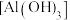 是重要的化工原料,也是用量最大和应用最广的无机阻燃添加剂,钼酸钠
是重要的化工原料,也是用量最大和应用最广的无机阻燃添加剂,钼酸钠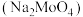 具有广泛的用途,可作新型阻燃剂、水处理剂和无公害型冷却水系统的金属抑制剂等。现从某废钼催化剂
具有广泛的用途,可作新型阻燃剂、水处理剂和无公害型冷却水系统的金属抑制剂等。现从某废钼催化剂 主要成分
主要成分 、
、 、
、 等
等 中回收
中回收 和
和 ,其工艺流程如图:
,其工艺流程如图:
回答下列问题:
(1)已知
 、
、 与
与 相似,均能在高温下跟
相似,均能在高温下跟 发生类似的反应,试写出①焙烧时
发生类似的反应,试写出①焙烧时 跟
跟 反应的化学方程式:
反应的化学方程式:(2)检验②操作后所得的滤渣中含有
 的方法是:
的方法是:(3)第③步操作中加入
 需要适量,可以通过测定溶液
需要适量,可以通过测定溶液 的用量。该步操作中制备
的用量。该步操作中制备 的离子方程式为
的离子方程式为(4)从题目信息可知,下图曲线
 填序号
填序号 为
为 的溶解度曲线。
的溶解度曲线。
(5)利用铝热反应可以回收金属钼。将所得钼酸钠溶液用酸处理得到沉淀,再加热可得
 。写出
。写出 发生铝热反应的化学方程式:
发生铝热反应的化学方程式:
您最近一年使用:0次
【推荐2】软锰矿(主要成分为MnO2)可用于制备锰及其化合物。
(1)早期冶炼金属锰的一种方法是先煅烧软锰矿生成Mn3O4,再利用铝热反应原理制得锰,该铝热反应的化学方程式为__ 。
(2)现代冶炼金属锰的一种工艺流程如图所示:
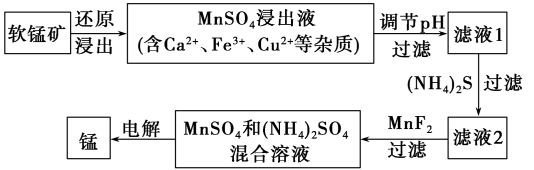
如表为常温下有关物质的pKsp(注:pKsp=-lgKsp)。
软锰矿还原浸出的反应为:12MnO2+C6H12O6+12H2SO4=12MnSO4+6CO2↑+18H2O
①该反应中,还原剂为___ ,写出一种能提高还原浸出速率的措施__ 。
②滤液1的pH__ (填“大于”、“小于”或“等于”)MnSO4浸出液的pH。
③加入MnF2的主要目的是除去__ (填Ca2+、Fe3+或Cu2+)。
(3)由MnSO4制取MnCO3:往MnSO4溶液中加入过量NH4HCO3溶液,该反应的离子方程式为___ ;若向MnSO4溶液中加入(NH4)2CO3溶液,还会产生Mn(OH)2,可能的原因是:MnCO3(s)+2OH-(aq) Mn(OH)2(s)+CO
Mn(OH)2(s)+CO (aq),常温下,计算该反应的平衡常数K=
(aq),常温下,计算该反应的平衡常数K=__ (填数值)。
(4)通常认为常温下残留在溶液中的离子浓度小于1×10-5mol·L-1时就认为沉淀完全,Fe3+完全沉淀时溶液的pH至少为___ 。
(1)早期冶炼金属锰的一种方法是先煅烧软锰矿生成Mn3O4,再利用铝热反应原理制得锰,该铝热反应的化学方程式为
(2)现代冶炼金属锰的一种工艺流程如图所示:

如表为常温下有关物质的pKsp(注:pKsp=-lgKsp)。
| 物质 | Fe(OH)3 | Cu(OH)2 | Ca(OH)2 | Mn(OH)2 | CuS | CaS | MnS | MnCO3 |
| pKsp | 37.4 | 19.32 | 5.26 | 12.7 | 35.2 | 5.86 | 12.6 | 10.7 |
软锰矿还原浸出的反应为:12MnO2+C6H12O6+12H2SO4=12MnSO4+6CO2↑+18H2O
①该反应中,还原剂为
②滤液1的pH
③加入MnF2的主要目的是除去
(3)由MnSO4制取MnCO3:往MnSO4溶液中加入过量NH4HCO3溶液,该反应的离子方程式为
 Mn(OH)2(s)+CO
Mn(OH)2(s)+CO (aq),常温下,计算该反应的平衡常数K=
(aq),常温下,计算该反应的平衡常数K=(4)通常认为常温下残留在溶液中的离子浓度小于1×10-5mol·L-1时就认为沉淀完全,Fe3+完全沉淀时溶液的pH至少为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】如图所涉及的物质均为中学化学中的常见物质,其中D为黄绿色的气体,E为Fe单质,它们存在如下转化关系,反应中生成的水及次要产物均已略去.
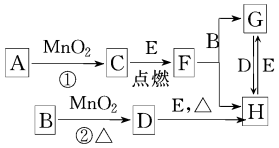
(1)写出有关物质的名称:B__________ ,F______________
(2)写出F与金属铝在高温下的反应化学方程式____________________________
(3)若反应①是在加热条件下进行的,则A是____________ (填化学式);
(4)指出MnO2在相关反应中的作用:反应②中是________ 剂.
(5)写出B与MnO2共热获得D的化学方程式:__________________________ .
(6)实验室检验H中的阳离子的方法是______________________________

(1)写出有关物质的名称:B
(2)写出F与金属铝在高温下的反应化学方程式
(3)若反应①是在加热条件下进行的,则A是
(4)指出MnO2在相关反应中的作用:反应②中是
(5)写出B与MnO2共热获得D的化学方程式:
(6)实验室检验H中的阳离子的方法是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】已知A为淡黄色固体,T、R为两种常见的用途很广的金属单质,D是具有磁性的黑色晶体,C是无色无味的气体,H是白色沉淀,W溶液中加入KSCN出现红色.
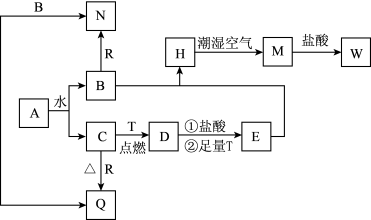
(1)写出下列物质的化学式:
A:______ D:____ E:______ N:______ .
(2)B与E混和得到H并在潮湿空气中变成M的过程中,可能观察到的现象:______ ;
(3)按要求写方程式:B和R反应生成N的离子方程式:______ ;M→W的离子方程式:____

(1)写出下列物质的化学式:
A:
(2)B与E混和得到H并在潮湿空气中变成M的过程中,可能观察到的现象:
(3)按要求写方程式:B和R反应生成N的离子方程式:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】铁及其化合物在日常生活中很常见
(1)氧化铁是重要工业颜料,用废铁屑制备它的流程如下:
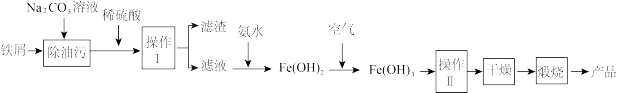
回答下列问题:
①操作II所包含的两项主要基本操作是____________ 。上述流程中,Fe(OH)2转化成Fe(OH)3时的化学方程式为__________________________________ 。
②将FeCl2溶液高温水解、氧化也可直接制得氧化铁,请写出反应的化学方程式:_______________ 。
(2)有些同学认为用KMnO4溶液能进行绿矾(FeSO4·7H2O)产品中铁元素含量的测定,反应的离子方程式为:___________ ,该滴定过程中_____ (填“是”或“否”)还需要指示剂。
实验步骤如下:
a.考虑绿矾产品可能因为保存不当被空气中氧气所氧化,所以事先取少量绿矾产品溶于水,滴加_____ 溶液进行验证。
b.称取2.850g绿矾产品,溶解,在250mL容量瓶中定容;
c.量取25.00mL待测溶液于锥形瓶中;
d.用硫酸酸化的0.01000 mol·L-1KMnO4溶液滴定至终点,消耗KMnO4溶液体积的平均值为20.00mL。
请完成下列问题:
①实验前,首先要精确配制一定物质的量浓度的KMnO4溶液250 mL,配制时需要的仪器除天平、玻璃棒、烧杯、胶头滴管外,还需__________________________ 。
②某同学设计的下列滴定方式,最合理的是________ (夹持部分略去)(填字母序号)。
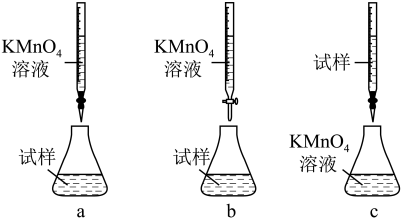
③计算上述样品中FeSO4·7H2O的质量分数为_____________ 。
(1)氧化铁是重要工业颜料,用废铁屑制备它的流程如下:
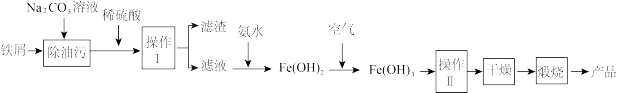
回答下列问题:
①操作II所包含的两项主要基本操作是
②将FeCl2溶液高温水解、氧化也可直接制得氧化铁,请写出反应的化学方程式:
(2)有些同学认为用KMnO4溶液能进行绿矾(FeSO4·7H2O)产品中铁元素含量的测定,反应的离子方程式为:
实验步骤如下:
a.考虑绿矾产品可能因为保存不当被空气中氧气所氧化,所以事先取少量绿矾产品溶于水,滴加
b.称取2.850g绿矾产品,溶解,在250mL容量瓶中定容;
c.量取25.00mL待测溶液于锥形瓶中;
d.用硫酸酸化的0.01000 mol·L-1KMnO4溶液滴定至终点,消耗KMnO4溶液体积的平均值为20.00mL。
请完成下列问题:
①实验前,首先要精确配制一定物质的量浓度的KMnO4溶液250 mL,配制时需要的仪器除天平、玻璃棒、烧杯、胶头滴管外,还需
②某同学设计的下列滴定方式,最合理的是

③计算上述样品中FeSO4·7H2O的质量分数为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】电子工业中常用覆铜板为基材制作印刷电路板,原理是利用 溶液作为“腐蚀液”将覆铜板上不需要的铜腐蚀,使用后的“腐蚀液”可回收利用。回答下列问题。
溶液作为“腐蚀液”将覆铜板上不需要的铜腐蚀,使用后的“腐蚀液”可回收利用。回答下列问题。
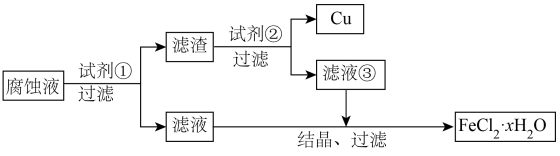
(1) 溶液腐蚀电路板的化学方程式为
溶液腐蚀电路板的化学方程式为___________ 。
(2)过量试剂①为___________ ;过量试剂②为___________ 。
(3)鉴别滤液③中的金属阳离子,应滴加的试剂依次是___________ ,现象是___________ 。 长时间暴露在空气中会变质,主要原因是
长时间暴露在空气中会变质,主要原因是___________ 。
(4)取 滤液③加入试管中,逐滴加入
滤液③加入试管中,逐滴加入 溶液。填写下列表格:
溶液。填写下列表格:
 溶液作为“腐蚀液”将覆铜板上不需要的铜腐蚀,使用后的“腐蚀液”可回收利用。回答下列问题。
溶液作为“腐蚀液”将覆铜板上不需要的铜腐蚀,使用后的“腐蚀液”可回收利用。回答下列问题。
(1)
 溶液腐蚀电路板的化学方程式为
溶液腐蚀电路板的化学方程式为(2)过量试剂①为
(3)鉴别滤液③中的金属阳离子,应滴加的试剂依次是
 长时间暴露在空气中会变质,主要原因是
长时间暴露在空气中会变质,主要原因是(4)取
 滤液③加入试管中,逐滴加入
滤液③加入试管中,逐滴加入 溶液。填写下列表格:
溶液。填写下列表格:| 序号 | 现象 | 用方程式解释现象 |
| ① | 开始无明显现象 | |
| ② | 稍后出现白色沉淀 |  |
| ③ | 空气中放置一段时间后,出现红褐色沉淀 |
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】已知A、E为金属单质,B为淡黄色粉末且常用于防毒面具中,回答下列问题。

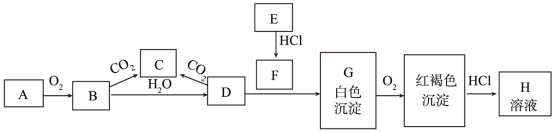
(1)实验室中A常常保存在盛有_______ 的广口瓶中,A的焰色反应为________ 色。
(2)写出B转变为C的化学方程式_______ 。该反应中氧化剂是________ ,0.1molB参与该反应,转移电子的数目为________ 。
(3)写出B转变为D的离子方程式_______ 。该反应中还原剂是________ ,该反应生成0.1molD,转移电子的数目为______ 。
(4)描述G露置在空气中的变化现象______ ,写出该过程的化学方程式________ 。
(5)写出E与水蒸气反应的化学方程式________ 。


(1)实验室中A常常保存在盛有
(2)写出B转变为C的化学方程式
(3)写出B转变为D的离子方程式
(4)描述G露置在空气中的变化现象
(5)写出E与水蒸气反应的化学方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】已知A为淡黄色固体,R是地壳中含量最多的金属元素的单质,T为生活中使用最广泛的金属单质,D是具有磁性的黑色晶体 ,C、F是无色无味的气体,H是白色沉淀,W溶液中滴加KSCN溶液出现红色。
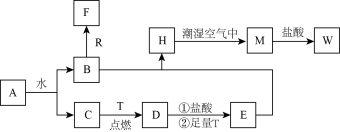
(1)物质D的化学式为___________ ,H的名称___________ 。
(2) 在潮湿空气中变成M的实验现象是
在潮湿空气中变成M的实验现象是______________ ,化学方程式为___________ 。
(3) 与W溶液也能发生反应,其反应的类型为
与W溶液也能发生反应,其反应的类型为______ (填序号)。
 化合反应
化合反应  置换反应
置换反应  复分解反应
复分解反应 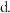 氧化还原反应
氧化还原反应
(4) 和R在溶液中反应生成F的离子方程式为
和R在溶液中反应生成F的离子方程式为____________________ 。
(5)将 投入到E溶液中,可以观察到的现象是:
投入到E溶液中,可以观察到的现象是:___________________ 。

(1)物质D的化学式为
(2)
 在潮湿空气中变成M的实验现象是
在潮湿空气中变成M的实验现象是(3)
 与W溶液也能发生反应,其反应的类型为
与W溶液也能发生反应,其反应的类型为 化合反应
化合反应  置换反应
置换反应  复分解反应
复分解反应 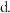 氧化还原反应
氧化还原反应(4)
 和R在溶液中反应生成F的离子方程式为
和R在溶液中反应生成F的离子方程式为(5)将
 投入到E溶液中,可以观察到的现象是:
投入到E溶液中,可以观察到的现象是:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】下列转化关系中,X、Y是生活中用途广泛的两种金属单质,A、B是氧化物,A为红棕色固体,C、D、E是中学常见的三种化合物。请根据转化关系回答下列问题。
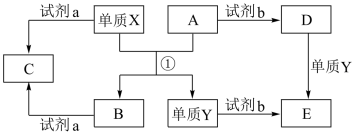
(1)请写出反应①的化学方程式:_______
(2)由D到E的离子方程式:_______ 。
(3)若试剂a是NaOH溶液,写出单质X与NaOH溶液反应的离子方程式:_______
(4)0.3molY在高温下与足量的水蒸气充分反应,转移的电子的物质的量为_______ mol。
(5)在D和E的混合溶液中,检验其中E的金属阳离子的试剂为_______ ,对应现象_______ 。
(6)向E溶液中加入NaOH溶液的现象为:_______
(7)若试剂b是 ,工业上用E、
,工业上用E、 和
和 为原料制取高效净水剂
为原料制取高效净水剂 ,产物还有NO和一种正盐,则该反应的化学方程式是
,产物还有NO和一种正盐,则该反应的化学方程式是_______ 。

(1)请写出反应①的化学方程式:
(2)由D到E的离子方程式:
(3)若试剂a是NaOH溶液,写出单质X与NaOH溶液反应的离子方程式:
(4)0.3molY在高温下与足量的水蒸气充分反应,转移的电子的物质的量为
(5)在D和E的混合溶液中,检验其中E的金属阳离子的试剂为
(6)向E溶液中加入NaOH溶液的现象为:
(7)若试剂b是
 ,工业上用E、
,工业上用E、 和
和 为原料制取高效净水剂
为原料制取高效净水剂 ,产物还有NO和一种正盐,则该反应的化学方程式是
,产物还有NO和一种正盐,则该反应的化学方程式是
您最近一年使用:0次



