下列各组排列顺序中正确的是:
| A.微粒半径: K+>Cl->S2->Na+ | B.稳定性:HI> HBr>HCl>HF |
| C.酸性: HClO4>H2SO4>H3PO4>H4SiO4 | D.熔点:金刚石>NaCl>SiO2>Na |
9-10高一下·浙江宁波·期中 查看更多[2]
更新时间:2016-12-09 00:27:36
|
相似题推荐
单选题
|
较易
(0.85)
名校
【推荐1】短周期主族元素X、Y、Z、W的原子序数依次增大,最外层电子数之和为16。Y的原子半径在同周期元素中最大(除稀有气体外),Z所在周期与族序数相同,W与X属于同一主族。下列说法正确的是
A.原子半径: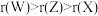 |
| B.由X、Y组成的化合物中均不含共价键 |
| C.Y的最高价氧化物的水化物的碱性比Z的弱 |
| D.X的简单气态氢化物的热稳定性比W的强 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】W、X、Y、Z是原子序数依次增大的四种短周期主族元素,X与Y位于同一主族,X与W能够形成多种化合物,其中一种为红棕色气体,Y与Z形成的一种化合物Y2Z2的分子结构模型为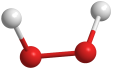 。下列叙述正确的是
。下列叙述正确的是
 。下列叙述正确的是
。下列叙述正确的是| A.X与W、Y及Z均能组合成多种化合物 | B.简单离子半径:Y>Z>X>W |
| C.W的氧化物的水化物一定为强酸 | D.化合物Y2Z2中Y不满足8电子稳定结构 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】已知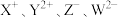 四种离子均具有相同的电子层结构,则下列关于
四种离子均具有相同的电子层结构,则下列关于 四种元素的描述中,正确的是
四种元素的描述中,正确的是
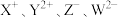 四种离子均具有相同的电子层结构,则下列关于
四种离子均具有相同的电子层结构,则下列关于 四种元素的描述中,正确的是
四种元素的描述中,正确的是A.原子序数: | B.原子最外层电子数: |
C.原子半径: | D.金属性: ,还原性: ,还原性: |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】已知X、Y、Z、W、R是原子序数依次增大的短周期主族元素,X是周期表中原子半径最小的元素,Y元素的最高正价与最低负价的绝对值相等,Z的核电荷数是Y的2倍,W的最外层电子数是其最内层电子数的3倍。下列说法正确的是
| A.原子半径:Z>W>R>X |
| B.对应气态氢化物的热稳定性:W>R>Y |
| C.W与Y、Z与R形成的化合物微粒组成比相同 |
| D.W与R的氧化物对应的水化物是强酸 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】下列说法正确的是
A.一氯甲烷的电子式: | B.CH4分子球棍模型: |
| C.晶体类型相同:SiO2和SO3 | D.第一电离能:S>P |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】下列物质的晶体属于离子晶体的是
| A.苛性钾 | B.碘化氢 | C.硫酸 | D.醋酸 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】下列关于微粒间的作用力说法正确的是
①所有金属与所有非金属之间都能形成离子键
②金属的导电性、延展性均与金属键有关
③金属晶体的熔沸点不一定高于分子晶体
④晶体的熔沸点:金刚石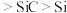
⑤ 中的
中的 键成键原理完全相同
键成键原理完全相同
⑥分子晶体中共价键的键能越大,晶体的熔点和沸点越高
⑦离子键的强弱:
⑧ 比
比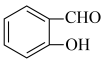 熔沸点低
熔沸点低
①所有金属与所有非金属之间都能形成离子键
②金属的导电性、延展性均与金属键有关
③金属晶体的熔沸点不一定高于分子晶体
④晶体的熔沸点:金刚石
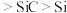
⑤
 中的
中的 键成键原理完全相同
键成键原理完全相同⑥分子晶体中共价键的键能越大,晶体的熔点和沸点越高
⑦离子键的强弱:

⑧
 比
比 熔沸点低
熔沸点低| A.①③④⑦ | B.②③④⑥ | C.②④⑦⑧ | D.②③④⑦ |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】胍(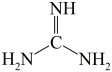 )是一元强碱,为平面形分子,其盐酸盐(
)是一元强碱,为平面形分子,其盐酸盐(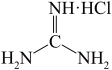 )是核酸检测液的主要成分。下列说法错误的是
)是核酸检测液的主要成分。下列说法错误的是
 )是一元强碱,为平面形分子,其盐酸盐(
)是一元强碱,为平面形分子,其盐酸盐( )是核酸检测液的主要成分。下列说法错误的是
)是核酸检测液的主要成分。下列说法错误的是| A.胍分子中最多7个原子共面 |
| B.胍易溶于水 |
| C.胍的熔点低于胍盐 |
| D.胍盐中的氯元素以氯化氢分子形式存在 |
您最近一年使用:0次