(Ⅰ)混合物的分离与提纯在化学实验中占有重要的位置。下图表示从固体混合物中分离X的方案,请回答有关问题。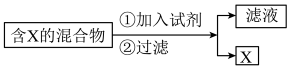
(1)若按照以上图示从某金属粉末(含有Au、Ag和Cu)中分离Au,加入的试剂是_______ ,有关反应的化学方程式为______________ ;
(2)为提纯某Fe2O3样品(主要杂质有SiO2、A12O3),请设计一种以框图形式表示的实验方案(注明物质和操作)__________________________ 。
(Ⅱ)工业上以黄铜矿为原料,采用火法熔炼工艺生产铜。
(3)该工艺的中间过程会发生反应: ,反应的氧化剂是
,反应的氧化剂是______________ ,氧化产物为__________
(4)在精炼铜的过程中,电解液中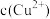 逐渐下降,
逐渐下降,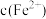 、
、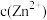 会逐渐增加,所以需定时除去其中的
会逐渐增加,所以需定时除去其中的 、
、 。下表为几种物质的溶度积。
。下表为几种物质的溶度积。
甲同学设计了如下除杂方案:
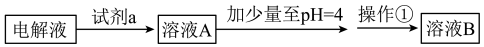
①试剂a是__________ ,其目的是____________________________________ ;根据溶度积该方案能够除去的杂质金属阳离子是____________ 。写出检验该杂质金属阳离子的操作方法:_______________________________________________ .
②乙同学在查阅资料时发现,“工业原料氯化铵中含杂质氯化铁,使其溶入水,再加入氨水
调节pH至7~8,可使 生成
生成 沉淀而除去”,乙同学认为甲同学的方案中也
沉淀而除去”,乙同学认为甲同学的方案中也
应该将溶液pH调至7~8。你认为乙同学的建议是否正确?________ (填“是”或“否”),理由是_________________________________________________ 。

(1)若按照以上图示从某金属粉末(含有Au、Ag和Cu)中分离Au,加入的试剂是
(2)为提纯某Fe2O3样品(主要杂质有SiO2、A12O3),请设计一种以框图形式表示的实验方案(注明物质和操作)
(Ⅱ)工业上以黄铜矿为原料,采用火法熔炼工艺生产铜。
(3)该工艺的中间过程会发生反应:
 ,反应的氧化剂是
,反应的氧化剂是(4)在精炼铜的过程中,电解液中
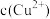 逐渐下降,
逐渐下降,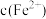 、
、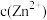 会逐渐增加,所以需定时除去其中的
会逐渐增加,所以需定时除去其中的 、
、 。下表为几种物质的溶度积。
。下表为几种物质的溶度积。| 物质 |  |  |  |  |
溶度积 |  | 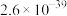 | 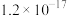 | 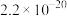 |
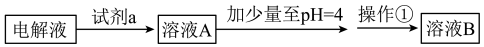
①试剂a是
②乙同学在查阅资料时发现,“工业原料氯化铵中含杂质氯化铁,使其溶入水,再加入氨水
调节pH至7~8,可使
 生成
生成 沉淀而除去”,乙同学认为甲同学的方案中也
沉淀而除去”,乙同学认为甲同学的方案中也应该将溶液pH调至7~8。你认为乙同学的建议是否正确?
2010·四川绵阳·一模 查看更多[1]
(已下线)2010年四川绵阳高考预测(综合题)化学卷
更新时间:2016-12-09 00:41:50
|
相似题推荐
解答题-实验探究题
|
容易
(0.94)
【推荐1】下图是CO还原CuO的装置图:
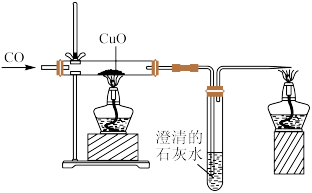
(1)需要先通一会一氧化碳,为了先_______ ,防止一氧化碳纯度不够而爆炸,通一会一氧化碳之后再加热。结束时,先撤掉_______ ,继续通一会一氧化碳,直到玻璃管冷却,防止生成的铜又被氧化,一氧化碳_______ (填“有”或“没有”)毒,加强通风换气,这里通入的气体必须处理掉,用点燃或者小气球收集;
(2)如果用点燃的方法处理多余的CO,化学方程式是_______ ,产物_______ (填“是”或“不是”)温室效应的气体之一,其固体俗称_______ ;
(3)生活中冶炼金属(还原金属氧化物)除常用CO外,还有H2和C等,从经济型和实用型考虑:
①首饰加工店你建议用_______ ,(选填“CO”、“H2或” 或“C”);
②农村打铁铺你建议用_______ ,(选填“CO”、“H2或” 或“C”);
(4)CO还原CuO反应的化学方程式CO+CuO Cu+CO2中,氧化剂是:
Cu+CO2中,氧化剂是:_______ ,还原剂是:_______ ,氧化产物是:_______ ,还原产物是:_______ 。

(1)需要先通一会一氧化碳,为了先
(2)如果用点燃的方法处理多余的CO,化学方程式是
(3)生活中冶炼金属(还原金属氧化物)除常用CO外,还有H2和C等,从经济型和实用型考虑:
①首饰加工店你建议用
②农村打铁铺你建议用
(4)CO还原CuO反应的化学方程式CO+CuO
 Cu+CO2中,氧化剂是:
Cu+CO2中,氧化剂是:
您最近一年使用:0次
解答题-实验探究题
|
容易
(0.94)
【推荐2】用脱脂棉包住约0.2g过氧化钠粉末,置于石棉网上,向脱脂棉上滴水,观察到脱脂棉剧烈燃烧起来。

(1)Na2O2跟水反应的离子反应方程式为___________ 。此反应中Na2O2的O元素化合价为___________ ,___________ 是氧化剂(写化学式),___________ 是还原剂(写化学式)。
(2)由上述实验现象所得到的过氧化钠跟水反应的结论是:
①有氧气生成;②反应过程中有___________ 。
(3)某研究性学习小组拟用如图所示装置(气密性良好)进行实验,以证明上述实验结论。验证第①条结论的实验操作及现象是:向试管中滴入水,___________ 。
(4)向试管中加水至固体完全溶解且不再有气泡生成后,取出试管,向试管中滴入酚酞试液并振荡,现象为___________ 。

(1)Na2O2跟水反应的离子反应方程式为
(2)由上述实验现象所得到的过氧化钠跟水反应的结论是:
①有氧气生成;②反应过程中有
(3)某研究性学习小组拟用如图所示装置(气密性良好)进行实验,以证明上述实验结论。验证第①条结论的实验操作及现象是:向试管中滴入水,
(4)向试管中加水至固体完全溶解且不再有气泡生成后,取出试管,向试管中滴入酚酞试液并振荡,现象为
您最近一年使用:0次
解答题-原理综合题
|
容易
(0.94)
解题方法
【推荐1】温度升高,难溶电解质的溶解度都增大吗_______ 。
您最近一年使用:0次
解答题-工业流程题
|
容易
(0.94)
【推荐1】侯氏制碱法的工艺流程如图所示:
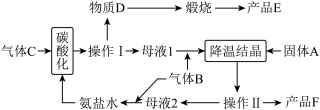
完成下列各题。
(1)写出碳酸化反应的化学方程式:__________ 。
(2)气体B的化学式为__________ 。
(3)操作Ⅰ的名称是________ 。在实验室里进行煅烧所用的仪器有__________ 。

完成下列各题。
(1)写出碳酸化反应的化学方程式:
(2)气体B的化学式为
(3)操作Ⅰ的名称是
您最近一年使用:0次
解答题-实验探究题
|
容易
(0.94)
解题方法
【推荐2】现有如图仪器,
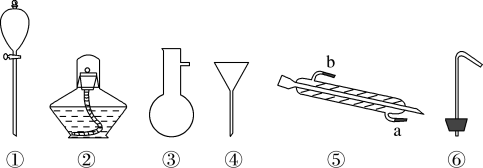
(1)海水蒸馏是由海水获得淡水的常用方法之一,在实验室里组成一套蒸馏装置肯定需要上述仪器中的________ (填序号);实验时③中除加入适量海水外,还需加入________ ,其作用是__________________________________________ 。
(2)海带等藻类物质经过处理后,可以得到碘水,欲从碘水中提取碘,需要上述中的仪器,该仪器名称为____________ 。为了使该仪器中液体可以顺利流下,应进行的具体操作是____________________________________________ 。向该碘水中加入四氯化碳以提取碘单质的实验操作为____________ 。

(1)海水蒸馏是由海水获得淡水的常用方法之一,在实验室里组成一套蒸馏装置肯定需要上述仪器中的
(2)海带等藻类物质经过处理后,可以得到碘水,欲从碘水中提取碘,需要上述中的仪器,该仪器名称为
您最近一年使用:0次
解答题-工业流程题
|
容易
(0.94)
名校
【推荐3】已知某工业废水中含有大量CuSO4,少量的Ag+、Hg2+以及部分污泥,通过下述过程可从该废水中回收硫酸铜晶体及其它物质。

(1)步骤1的主要操作是___________ ,需用到的玻璃仪器除烧杯外有___________ 和___________ 。
(2)步骤2中需加入某种试剂后再将混合物分离,该试剂是(填化学式)___________ ,固体残渣的成分是(填化学式) ___________ 。
(3)步骤3中涉及的操作是:蒸发浓缩、___________ 、过滤、烘干。

(1)步骤1的主要操作是
(2)步骤2中需加入某种试剂后再将混合物分离,该试剂是(填化学式)
(3)步骤3中涉及的操作是:蒸发浓缩、
您最近一年使用:0次
解答题-实验探究题
|
容易
(0.94)
【推荐1】按如图所示装置进行 制备实验,填写有关现象及化学方程式。
制备实验,填写有关现象及化学方程式。
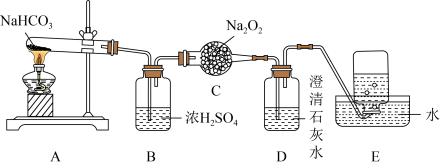
(1)A中发生反应的化学方程式为_______ 。
(2)C中发生反应的化学方程式为_______ 。
(3)石灰水作用_______ 。
 制备实验,填写有关现象及化学方程式。
制备实验,填写有关现象及化学方程式。
(1)A中发生反应的化学方程式为
(2)C中发生反应的化学方程式为
(3)石灰水作用
您最近一年使用:0次
解答题-实验探究题
|
容易
(0.94)
解题方法
【推荐2】浓硫酸是中学中常见的一种化学试剂,某学校实验小组为探究浓硫酸与金属的反应并检验生成的气体设计了相关实验。
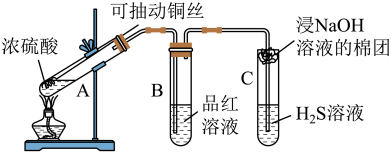
(1)常温下,将铝片插入浓H2SO4中未发现有明显的变化,其原因为__________ 。
(2)在加热的条件下,浓H2SO4可将铜氧化,写出该反应的化学方程式:_________ 。
(3)实验中使用可抽动的铜丝,其优点是_________ 。
(4)实验中可观察到B中品红溶液的现象为__________ 。
(5)C中的实验现象为_____ ,通过对该实验现象的分析,说明SO2有______ (填“还原性”或“氧化性”)。
(6)浸有NaOH溶液的棉团的作用为:_________ 。

(1)常温下,将铝片插入浓H2SO4中未发现有明显的变化,其原因为
(2)在加热的条件下,浓H2SO4可将铜氧化,写出该反应的化学方程式:
(3)实验中使用可抽动的铜丝,其优点是
(4)实验中可观察到B中品红溶液的现象为
(5)C中的实验现象为
(6)浸有NaOH溶液的棉团的作用为:
您最近一年使用:0次
解答题-实验探究题
|
容易
(0.94)
名校
【推荐3】FeCl3为黑棕色固体,无水氯化铁在300℃以上升华,遇潮湿空气极易潮解。
(1)甲组同学拟用下列装置制取纯净干燥的氯气。
①装置B的作用是_________
②装置A中发生反应时消耗的氧化剂和还原剂的物质的量之比为__________
(2)乙组同学选用甲组实验中的装置ABC和下列装置制取FeCl3

①乙组同学的实验装置中,依次连接的合理顺序为:a→_____ →_____ →_____ →_____ →_____ →_____
②连好装置,检查装置的气密性,先打开装置A中___________ (填仪器的名称)的活塞,直到______ 再点燃装置F处的酒精灯,目的是_______
③装置D的作用有_______
(3)实验结束后,取少量F中的固体加水溶解,欲对所得产物FeCl3中是否含有FeCl2进行检测,所需试剂是_______
a.KSCN b.H2O2 c.K3[Fe(CN)6] d. .K4[Fe(CN)6]
经检测发现溶液中含有Fe2+,丙同学认为所得产物FeCl3中一定含有FeCl2,丁同学认为不一定,理由是_____
(1)甲组同学拟用下列装置制取纯净干燥的氯气。
①装置B的作用是
②装置A中发生反应时消耗的氧化剂和还原剂的物质的量之比为
(2)乙组同学选用甲组实验中的装置ABC和下列装置制取FeCl3

①乙组同学的实验装置中,依次连接的合理顺序为:a→
②连好装置,检查装置的气密性,先打开装置A中
③装置D的作用有
(3)实验结束后,取少量F中的固体加水溶解,欲对所得产物FeCl3中是否含有FeCl2进行检测,所需试剂是
a.KSCN b.H2O2 c.K3[Fe(CN)6] d. .K4[Fe(CN)6]
经检测发现溶液中含有Fe2+,丙同学认为所得产物FeCl3中一定含有FeCl2,丁同学认为不一定,理由是
您最近一年使用:0次




