[化学—选修3]碳是地球上组成生命的最基本元素之一,可以sp3、sp2和sp杂化轨道成共价键,具有很强的结合能力,与其它元素结合成不计其数的无机物和有机化合物,构成了丰富多彩的世界。碳及其化合物在研究和生产中有许多重要用途。请回答下列问题:
(1)基态碳原子核外有__________ 种空间运动状态的电子,其价电子排布图为 ____________________ 。
(2)光气的分子式为 COCl2,又称碳酰氯,是一种重要的含碳化合物,判断其分子立体构型为_________ ,其碳原子杂化轨道类型为_______ 杂化。
(3)碳酸盐在一定温度下会发生分解,实验证明碳酸盐的阳离子不同,分解温度不同,如下表所示:
试解释为什么随着阳离子半径的增大,碳酸盐的分解温度逐步升高?__________________________ 。
(4)碳的一种同素异形体——C60,又名足球烯,是一种高度对称的球碳分子。立方烷(分子式:C8H8,结构是立方体: )是比 C60 约早20年合成出的一种对称型烃类分子,而现如今已合成出一种立方烷与 C60 的复合型分子晶体,该晶体的晶胞结构如图乙所示,立方烷分子填充在原 C60 晶体的分子间空隙中。则该复合型分子晶体的组成用二者的分子式可表示为
)是比 C60 约早20年合成出的一种对称型烃类分子,而现如今已合成出一种立方烷与 C60 的复合型分子晶体,该晶体的晶胞结构如图乙所示,立方烷分子填充在原 C60 晶体的分子间空隙中。则该复合型分子晶体的组成用二者的分子式可表示为___________ 。

(5)碳的另一种同素异形体——石墨,其晶体结构如图丙所示,虚线勾勒出的是其晶胞。则石墨晶胞含碳原子个数为______ 个。已知石墨的密度为ρ g.cm-3,C-C键长为 r cm,阿伏伽德罗常数的值为 NA,计算石墨晶体的层间距为_______ cm。
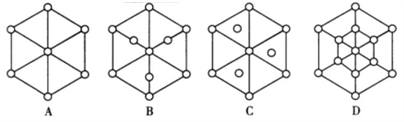
(6)碳的第三种同素异形体——金刚石,其晶胞如图丁所示。已知金属钠的晶胞(体心立方堆积)沿其体对角线垂直在纸平面上的投影图如图A,则金刚石晶胞沿其体对角线垂直在纸平面的投影图应该是图_________ 。
(1)基态碳原子核外有
(2)光气的分子式为 COCl2,又称碳酰氯,是一种重要的含碳化合物,判断其分子立体构型为
(3)碳酸盐在一定温度下会发生分解,实验证明碳酸盐的阳离子不同,分解温度不同,如下表所示:
| 碳酸盐 | MgCO3 | CaCO3 | BaCO3 | SrCO3 |
| 热分解温度/℃ | 402 | 900 | 1172 | 1360 |
| 阳离子半径/pm | 66 | 99 | 112 | 135 |
试解释为什么随着阳离子半径的增大,碳酸盐的分解温度逐步升高?
(4)碳的一种同素异形体——C60,又名足球烯,是一种高度对称的球碳分子。立方烷(分子式:C8H8,结构是立方体:
 )是比 C60 约早20年合成出的一种对称型烃类分子,而现如今已合成出一种立方烷与 C60 的复合型分子晶体,该晶体的晶胞结构如图乙所示,立方烷分子填充在原 C60 晶体的分子间空隙中。则该复合型分子晶体的组成用二者的分子式可表示为
)是比 C60 约早20年合成出的一种对称型烃类分子,而现如今已合成出一种立方烷与 C60 的复合型分子晶体,该晶体的晶胞结构如图乙所示,立方烷分子填充在原 C60 晶体的分子间空隙中。则该复合型分子晶体的组成用二者的分子式可表示为
(5)碳的另一种同素异形体——石墨,其晶体结构如图丙所示,虚线勾勒出的是其晶胞。则石墨晶胞含碳原子个数为
(6)碳的第三种同素异形体——金刚石,其晶胞如图丁所示。已知金属钠的晶胞(体心立方堆积)沿其体对角线垂直在纸平面上的投影图如图A,则金刚石晶胞沿其体对角线垂直在纸平面的投影图应该是图

更新时间:2017-05-09 21:51:58
|
相似题推荐
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐1】A、B、D、E、F为原子序数依次增大的前四周期元素,其中A的最外层电子数是其内层电子数的2倍,B、D、E为同周期元素,B原子的核外电子总数是其未成对电子数的5倍,E原子最外层有1个未成对电子,F原子核外有22种运动状态的电子。请回答下列问题:
(1)F元素位于周期表___________ 区,其价电子排布图为:___________ 。
(2)B、D、E三种元素中,第一电离能最小的是_______________________ (填元素符号);写出AD2的等电子体___________ (分子和阴离子各写一种)。
(3)AO2和DO2熔点高的是___________ ,原因是___________ 。
(4)B的单质和E的单质反应可形成原子个数比为1∶3的化合物M,M的立体构型为___________ ,中心原子的杂化轨道类型为___________ 。
(5)元素F有两种同素异形体,常温下是六方堆积,高温下是体心立方堆积。如图所示是F晶体的一种晶胞,晶胞参数a=0.295nm,c=0.469nm,则该F晶体的密度为___________ g·cm-3(用NA表示阿伏伽德罗常数的值,列出计算式即可)。

(1)F元素位于周期表
(2)B、D、E三种元素中,第一电离能最小的是
(3)AO2和DO2熔点高的是
(4)B的单质和E的单质反应可形成原子个数比为1∶3的化合物M,M的立体构型为
(5)元素F有两种同素异形体,常温下是六方堆积,高温下是体心立方堆积。如图所示是F晶体的一种晶胞,晶胞参数a=0.295nm,c=0.469nm,则该F晶体的密度为

您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐2】新型高温铁基超导材料主要由 、P、
、P、 、
、 等元素组成。回答下列问题:
等元素组成。回答下列问题:
(1)基态 原子的价层电子排布式为
原子的价层电子排布式为___________ ,基态 与基态
与基态 中的未成对电子数之比为
中的未成对电子数之比为___________ 。
(2)向 中嵌入吡啶(
中嵌入吡啶(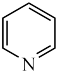 )能得到具有优异性能的超导材料,吡啶能与水以任意比例互溶,是因为吡啶是极性分子且
)能得到具有优异性能的超导材料,吡啶能与水以任意比例互溶,是因为吡啶是极性分子且___________ 。
(3)氧、硫、硒为同主族元素, 、
、 和
和 的沸点由高到低的顺序为
的沸点由高到低的顺序为___________ (填化学式,下同),键角由大到小的顺序为___________ 。
(4) 晶体的配离子结构如图1所示,其配体
晶体的配离子结构如图1所示,其配体 中的C的杂化方式为
中的C的杂化方式为___________ 杂化,中心离子的配位数为___________ 。

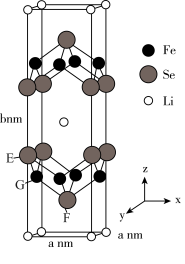
图1 图2
(5) 、
、 、
、 可形成新型超导材料,晶胞棱边夹角均为90°,晶胞结构及晶胞参数如图2所示,以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标,E原子的坐标为
可形成新型超导材料,晶胞棱边夹角均为90°,晶胞结构及晶胞参数如图2所示,以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标,E原子的坐标为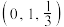 ,F原子的坐标为
,F原子的坐标为 ,G原子的坐标为
,G原子的坐标为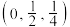 。
。
则距离 原子最近的
原子最近的 原子的个数为
原子的个数为___________ , 原子和
原子和 原子间的最短距离为
原子间的最短距离为___________ (填含a、b的代数式) 。
。
 、P、
、P、 、
、 等元素组成。回答下列问题:
等元素组成。回答下列问题:(1)基态
 原子的价层电子排布式为
原子的价层电子排布式为 与基态
与基态 中的未成对电子数之比为
中的未成对电子数之比为(2)向
 中嵌入吡啶(
中嵌入吡啶( )能得到具有优异性能的超导材料,吡啶能与水以任意比例互溶,是因为吡啶是极性分子且
)能得到具有优异性能的超导材料,吡啶能与水以任意比例互溶,是因为吡啶是极性分子且(3)氧、硫、硒为同主族元素,
 、
、 和
和 的沸点由高到低的顺序为
的沸点由高到低的顺序为(4)
 晶体的配离子结构如图1所示,其配体
晶体的配离子结构如图1所示,其配体 中的C的杂化方式为
中的C的杂化方式为

图1 图2
(5)
 、
、 、
、 可形成新型超导材料,晶胞棱边夹角均为90°,晶胞结构及晶胞参数如图2所示,以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标,E原子的坐标为
可形成新型超导材料,晶胞棱边夹角均为90°,晶胞结构及晶胞参数如图2所示,以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标,E原子的坐标为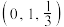 ,F原子的坐标为
,F原子的坐标为 ,G原子的坐标为
,G原子的坐标为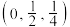 。
。则距离
 原子最近的
原子最近的 原子的个数为
原子的个数为 原子和
原子和 原子间的最短距离为
原子间的最短距离为 。
。
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐3】铝酸铋[Bi(AlO2)3]主要用作抗酸药及抗溃疡药,具有中和胃酸和收敛作用。以辉铋矿(主要成分为 Bi2S3,含有: 等杂质)为原料制备铝酸铋的一种工艺流程如图所示:
等杂质)为原料制备铝酸铋的一种工艺流程如图所示:

已知:“沉淀”步骤中,不能出现Fe3+,否则后续Bi(OH)3沉淀中会混有Fe(OH)3杂质。请回答下列问题:
(1)铋位于第六周期,且与氮同主族,则铋元素在元素周期表中属于___________ 区,铋的价层电子排布式为___________ 。
(2)“浸取”过程中,提高浸出率的措施有___________ 。(写一条即可)
(3) “还原”时, 加入铋的目的是___________ 。
(4)已知进入“碱溶”步骤的物质为经过充分洗涤的Cu(OH)2和 Bi(OH)3固体混合物,为检验是否洗涤干净,可选择的试剂为___________ 。
A.KSCN溶液 B.K3[Fe(CN)6]溶液 C.BaCl2溶液
 等杂质)为原料制备铝酸铋的一种工艺流程如图所示:
等杂质)为原料制备铝酸铋的一种工艺流程如图所示:
已知:“沉淀”步骤中,不能出现Fe3+,否则后续Bi(OH)3沉淀中会混有Fe(OH)3杂质。请回答下列问题:
(1)铋位于第六周期,且与氮同主族,则铋元素在元素周期表中属于
(2)“浸取”过程中,提高浸出率的措施有
(3) “还原”时, 加入铋的目的是
(4)已知进入“碱溶”步骤的物质为经过充分洗涤的Cu(OH)2和 Bi(OH)3固体混合物,为检验是否洗涤干净,可选择的试剂为
A.KSCN溶液 B.K3[Fe(CN)6]溶液 C.BaCl2溶液
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐1】Ⅰ.X、Y、Z、W、R、Q为前30号元素,且原子序数依次增大。X是元素周期表中原子半径最小的元素;Y元素基态原子有三个能级上有电子,且每个能级上的电子数相等;Z元素基态原子的单电子数在同周期元素基态原子中最多;W与Z同周期,第一电离能比Z的低;R与Y同主族;Q的最外层只有一个电子,其他电子层均有 个电子(n表示电子层序数)。请回答下列问题:
个电子(n表示电子层序数)。请回答下列问题:
(1)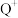 的核外电子排布式为
的核外电子排布式为_______ 。
(2)化合物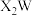 中W的杂化方式为
中W的杂化方式为_______ ;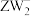 的空间结构为
的空间结构为_______ 。
(3)Y、R的最高价氧化物中沸点较高的是_______ (填化学式),原因是_______ 。
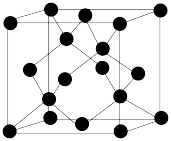
(4)Y有多种同素异形体,其中一种同素异形体的晶胞结构如图所示,该晶体的晶胞中所含Y原子的个数为_______ ;若晶胞的边长为 ,晶体的密度为
,晶体的密度为 ,则阿伏加德罗常数的值
,则阿伏加德罗常数的值 为
为_______ (用含a和p的代数式表示)。
Ⅱ.为了测定某有机物M的结构,设计了如下实验:
①将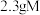 完全燃烧,测得生成
完全燃烧,测得生成 和
和 水;②用质谱仪测定其相对分子质量,得到如图1所示的质谱图;③用核磁共振仪处理该化合物,得到如图所示2的核磁共振氢谱,图中三个峰的面积之比是
水;②用质谱仪测定其相对分子质量,得到如图1所示的质谱图;③用核磁共振仪处理该化合物,得到如图所示2的核磁共振氢谱,图中三个峰的面积之比是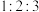 。试回答下列问题:
。试回答下列问题:
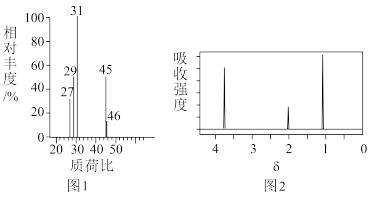
(5)有机物M的分子式为_______ ,结构简式为_______ 。
 个电子(n表示电子层序数)。请回答下列问题:
个电子(n表示电子层序数)。请回答下列问题:(1)
 的核外电子排布式为
的核外电子排布式为(2)化合物
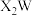 中W的杂化方式为
中W的杂化方式为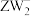 的空间结构为
的空间结构为(3)Y、R的最高价氧化物中沸点较高的是
(4)Y有多种同素异形体,其中一种同素异形体的晶胞结构如图所示,该晶体的晶胞中所含Y原子的个数为
 ,晶体的密度为
,晶体的密度为 ,则阿伏加德罗常数的值
,则阿伏加德罗常数的值 为
为
Ⅱ.为了测定某有机物M的结构,设计了如下实验:
①将
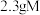 完全燃烧,测得生成
完全燃烧,测得生成 和
和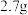 水;②用质谱仪测定其相对分子质量,得到如图1所示的质谱图;③用核磁共振仪处理该化合物,得到如图所示2的核磁共振氢谱,图中三个峰的面积之比是
水;②用质谱仪测定其相对分子质量,得到如图1所示的质谱图;③用核磁共振仪处理该化合物,得到如图所示2的核磁共振氢谱,图中三个峰的面积之比是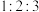 。试回答下列问题:
。试回答下列问题:
(5)有机物M的分子式为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐2】砷化镓 为黑灰色固体,是重要的半导体材料,用砷化镓制成的半导体器件具有低温性能好、抗辐射能力强等优点。请回答下列问题:
为黑灰色固体,是重要的半导体材料,用砷化镓制成的半导体器件具有低温性能好、抗辐射能力强等优点。请回答下列问题:
(1)基态 原子核外电子占据最高能级的电子云轮廓图为
原子核外电子占据最高能级的电子云轮廓图为________ 形。
(2)砷化镓可由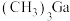 和
和 制得。在常温常压下,
制得。在常温常压下,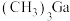 为无色透明液体,则
为无色透明液体,则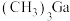 固体属于
固体属于________ 晶体。 的沸点低于
的沸点低于 的原因为
的原因为________ 。
(3)亚砷酸 是一种三元弱酸,分子中含有羟基数目为
是一种三元弱酸,分子中含有羟基数目为________ 个;根据价层电子对互斥理论推测 的空间构型为
的空间构型为________ ;与 互为等电子体的一种分子为
互为等电子体的一种分子为________ 。
(4) 的熔点为
的熔点为 ,晶胞结构如图所示:
,晶胞结构如图所示:

①在 晶体中,镓原子的配位数是
晶体中,镓原子的配位数是________ ,与同一个镓原子相连的砷原子构成的空间构型为________ 。
②若砷化镓晶胞边长为 。则该晶体密度为
。则该晶体密度为________  (用含
(用含 的代数式表示)。
的代数式表示)。
 为黑灰色固体,是重要的半导体材料,用砷化镓制成的半导体器件具有低温性能好、抗辐射能力强等优点。请回答下列问题:
为黑灰色固体,是重要的半导体材料,用砷化镓制成的半导体器件具有低温性能好、抗辐射能力强等优点。请回答下列问题:(1)基态
 原子核外电子占据最高能级的电子云轮廓图为
原子核外电子占据最高能级的电子云轮廓图为(2)砷化镓可由
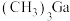 和
和 制得。在常温常压下,
制得。在常温常压下,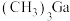 为无色透明液体,则
为无色透明液体,则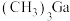 固体属于
固体属于 的沸点低于
的沸点低于 的原因为
的原因为(3)亚砷酸
 是一种三元弱酸,分子中含有羟基数目为
是一种三元弱酸,分子中含有羟基数目为 的空间构型为
的空间构型为 互为等电子体的一种分子为
互为等电子体的一种分子为(4)
 的熔点为
的熔点为 ,晶胞结构如图所示:
,晶胞结构如图所示:
①在
 晶体中,镓原子的配位数是
晶体中,镓原子的配位数是②若砷化镓晶胞边长为
 。则该晶体密度为
。则该晶体密度为 (用含
(用含 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐3】酞菁锌具有液晶的性质,在信息材料学领域有广泛应用,其结构如图所示。回答下列问题:

(1)基态Zn的价电子轨道表示式为____ ,C、N、O第一电离能由小到大的顺序是____ 。
(2)含有多个配位原子的配体与同一中心离子(或原子)通过螯合配位成环而形成的配合物为螯合物。1mol八氧基酞菁锌中通过螯合作用形成的配位键有____ mol,该螯合物中N的杂化方式有____ 种。
(3)离子型ZnO与ZnS熔沸点高低比较ZnO____ ZnS(填高于、低于),判断理由____ 。
(4)ZnS常用作分析试剂、荧光体、光导体材料。立方ZnS晶体晶胞结构如图所示:
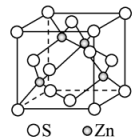
①在立方体体对角线的一维空间上S2-、Zn2+的分布规律正确的是____ (填选项)。
a. b.
b. 
c.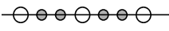 d.
d.
②已知晶体密度为dg•cm-3,阿伏加德罗常数为NA,则Zn2+和S2-之间的最短核间距(x)为____ nm(用代数式表示),一个Zn2+周围与其距离最近的Zn2+的数目为____ 。

(1)基态Zn的价电子轨道表示式为
(2)含有多个配位原子的配体与同一中心离子(或原子)通过螯合配位成环而形成的配合物为螯合物。1mol八氧基酞菁锌中通过螯合作用形成的配位键有
(3)离子型ZnO与ZnS熔沸点高低比较ZnO
(4)ZnS常用作分析试剂、荧光体、光导体材料。立方ZnS晶体晶胞结构如图所示:

①在立方体体对角线的一维空间上S2-、Zn2+的分布规律正确的是
a.
 b.
b. 
c.
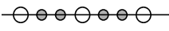 d.
d.
②已知晶体密度为dg•cm-3,阿伏加德罗常数为NA,则Zn2+和S2-之间的最短核间距(x)为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐1】储氢材料是一类能可逆地吸收和释放氢气的材料。LaNi5合金、NaBH4、H3B-NH3、Mg2NiH4等都是潜在储氢材料。回答下列问题:
(1)基态Ni原子的核外电子排布式为____ ,有___________ 个未成对的电子;
(2)NaBH4中H为-1价,Na、B、H电负性由大到小的顺序是_________ 。BH4-离子的立体构型为________ ,其中B的杂化轨道类型为_____ 。
(3)B2H6和NH3化合可以生成H3B-NH3,H3B-NH3加热时发生反应:H3B-NH3=BN+3H2,缓慢释放出H2。BN有类似于石墨的结构,B2H6、NH3和BN的沸点由高到低的顺序为_________ , 原因是___ 。
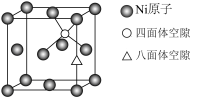
(4)X-射线衍射分析表明,Mg2NiH4 的立方晶胞的面心和顶点均被Ni原子占据,所有Mg原子的Ni配位数都相等。则Mg原子填入由Ni原子形成的_____ 空隙中(填“四面体”或“八面体”),其空隙占有百分率为_____ 。
(5)已知Mg2NiH4 晶体的晶胞参数为646.5 pm,液氢的密度为0.0708 g·cm-3。若以材料中氢的密度与液态氢密度之比定义储氢材料的储氢能力,则Mg2NiH4 的储氢能力是液氢的___ 倍(列出计算式即可)。
(1)基态Ni原子的核外电子排布式为
(2)NaBH4中H为-1价,Na、B、H电负性由大到小的顺序是
(3)B2H6和NH3化合可以生成H3B-NH3,H3B-NH3加热时发生反应:H3B-NH3=BN+3H2,缓慢释放出H2。BN有类似于石墨的结构,B2H6、NH3和BN的沸点由高到低的顺序为
(4)X-射线衍射分析表明,Mg2NiH4 的立方晶胞的面心和顶点均被Ni原子占据,所有Mg原子的Ni配位数都相等。则Mg原子填入由Ni原子形成的
(5)已知Mg2NiH4 晶体的晶胞参数为646.5 pm,液氢的密度为0.0708 g·cm-3。若以材料中氢的密度与液态氢密度之比定义储氢材料的储氢能力,则Mg2NiH4 的储氢能力是液氢的

您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
【推荐2】碳酸二甲酯(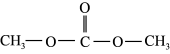 )是一种环保性能优异、用途广泛的化工原料。在催化剂作用下,由
)是一种环保性能优异、用途广泛的化工原料。在催化剂作用下,由 制备碳酸二甲酯的过程如图所示。回答下列问题:
制备碳酸二甲酯的过程如图所示。回答下列问题:
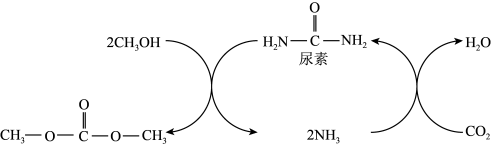
(1)尿素中N的第一电离能比O的高,原因是:
①O失去的是已经配对的电子,配对电子相互排斥,因而第一电离能较低;
②_______ 。
(2)下列有关 、
、 的叙述,正确的是_______(填标号)。
的叙述,正确的是_______(填标号)。
(3)含钛、铁、铜、锌的催化剂在制备碳酸二甲酯的过程中,催化效果较好。
①基态钛原子核外s能级和p能级的电子数之比为_______ 。
②含钛新型正极材料 具有高化学电位。
具有高化学电位。 的空间构型为
的空间构型为_______ 。
③已知:存在未成对电子的金属离子具有顺磁性。 、
、 、
、 、
、 中具有顺磁性的离子是
中具有顺磁性的离子是_______ (填离子符号);这四种金属离子各1mol中,未成对电子数最多的金属离子是_______ (填离子符号)。
④Ti(Ⅳ)在酸溶液中可形成多种离子。其中如图所示结构的离子符号为_______ 。
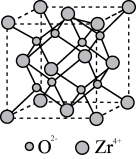
(4)在 固溶体的催化体系中也能将
固溶体的催化体系中也能将 转化为碳酸二甲酯。
转化为碳酸二甲酯。 晶胞结构如图所示,
晶胞结构如图所示, 在晶胞中的配位数是
在晶胞中的配位数是_______ 。若该晶胞的密度为 ,用NA表示阿伏加德罗常数的值,则该晶胞的体积是
,用NA表示阿伏加德罗常数的值,则该晶胞的体积是_______  (列出计算式)。
(列出计算式)。
 )是一种环保性能优异、用途广泛的化工原料。在催化剂作用下,由
)是一种环保性能优异、用途广泛的化工原料。在催化剂作用下,由 制备碳酸二甲酯的过程如图所示。回答下列问题:
制备碳酸二甲酯的过程如图所示。回答下列问题:
(1)尿素中N的第一电离能比O的高,原因是:
①O失去的是已经配对的电子,配对电子相互排斥,因而第一电离能较低;
②
(2)下列有关
 、
、 的叙述,正确的是_______(填标号)。
的叙述,正确的是_______(填标号)。A. 的键角小于 的键角小于 的键角,是因为 的键角,是因为 的中心原子上孤电子对对成键电子对有较大的斥力 的中心原子上孤电子对对成键电子对有较大的斥力 |
B. 极易溶解在水中,与氨分子为极性分子和氨分子与水分子间能形成氢键有关 极易溶解在水中,与氨分子为极性分子和氨分子与水分子间能形成氢键有关 |
C. 的沸点比 的沸点比 的高,是因为N-H键能比P-H键能大 的高,是因为N-H键能比P-H键能大 |
D.1mol 中含有12molσ键 中含有12molσ键 |
①基态钛原子核外s能级和p能级的电子数之比为
②含钛新型正极材料
 具有高化学电位。
具有高化学电位。 的空间构型为
的空间构型为③已知:存在未成对电子的金属离子具有顺磁性。
 、
、 、
、 、
、 中具有顺磁性的离子是
中具有顺磁性的离子是④Ti(Ⅳ)在酸溶液中可形成多种离子。其中如图所示结构的离子符号为

(4)在
 固溶体的催化体系中也能将
固溶体的催化体系中也能将 转化为碳酸二甲酯。
转化为碳酸二甲酯。 晶胞结构如图所示,
晶胞结构如图所示, 在晶胞中的配位数是
在晶胞中的配位数是 ,用NA表示阿伏加德罗常数的值,则该晶胞的体积是
,用NA表示阿伏加德罗常数的值,则该晶胞的体积是 (列出计算式)。
(列出计算式)。
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐3】氮在自然界中的存在十分广泛。某实验小组对不同含氮物质做了相关研究。请回答下列问题:
(1)氨的用途十分广泛,是制造硝酸和氮肥的重要原料。298K、101kPa条件下。合成氨每产生2molNH3,放出92.2kJ热量。已知:

1molN-H键断裂吸收的能量约等于___________ kJ。
(2)将NH3和NO2以一定的流速,分别通过甲、乙两种催化剂进行反应,相同时间内测量逸出气体中NO2含量,从而确定尾气脱氮率(即NO2的转化率),结果如图所示:

a点________ (填“是”或“不是”)平衡状态;脱氮率a~b段呈现如图变化,原因是_________ 。
(3)一种铁氮化合物具有高磁导率,可用于制电子元件,其晶胞结构如图所示。

①该铁氮化合物的化学式为___________ 。
②该晶体结构的另一种晶胞表示中,N处于顶点位置,则Fe(III)、Fe(II)分别处于___________ 、___________ 位置。
(4)25℃时,将10mL0.03mol/LNH4Cl溶液和10mL0.01mol/LAgNO3溶液混合(忽略溶液混合后的体积变化),混合后溶液中c(Ag+)为____________ [25℃时,Ksp(AgCl)=1.8×10-10]。用数字传感器探究AgCl的沉淀溶解平衡。实验测得悬浊液中溶解的氯化物浓度变化如图所示,其中a点表示AgCl溶于NH4Cl溶液形成的悬浊液,下列说法正确的是___________ (填字母标号)。
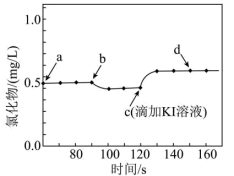
a.b点可能加入了NH4Cl(s) b.c点后无黄色沉淀生成
c.d点c(Ag+)<c(Cl-) d.由图可知:Ksp(AgI)<Ksp(AgCl)
(5)1939年捷姆金和佩热夫推出氨合成反应在接近平衡时净速率方程式为r(NH3)=k1p(N2)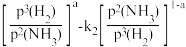 ,k1、k2分别为正反应和逆反应的速率常数;p(N2)、p(H2)、p(NH3)代表各组分的分压(分压=总压×物质的量分数);a为常数,工业上以铁为催化剂时,a=0.5。在一定条件下,向某容器中投入5molN2、15molH2,平衡时氨质量分数占40%,压强为32MPa.由此计算
,k1、k2分别为正反应和逆反应的速率常数;p(N2)、p(H2)、p(NH3)代表各组分的分压(分压=总压×物质的量分数);a为常数,工业上以铁为催化剂时,a=0.5。在一定条件下,向某容器中投入5molN2、15molH2,平衡时氨质量分数占40%,压强为32MPa.由此计算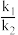 =
=___________ MPa-2(写出计算式即可)。
(1)氨的用途十分广泛,是制造硝酸和氮肥的重要原料。298K、101kPa条件下。合成氨每产生2molNH3,放出92.2kJ热量。已知:

1molN-H键断裂吸收的能量约等于
(2)将NH3和NO2以一定的流速,分别通过甲、乙两种催化剂进行反应,相同时间内测量逸出气体中NO2含量,从而确定尾气脱氮率(即NO2的转化率),结果如图所示:

a点
(3)一种铁氮化合物具有高磁导率,可用于制电子元件,其晶胞结构如图所示。

①该铁氮化合物的化学式为
②该晶体结构的另一种晶胞表示中,N处于顶点位置,则Fe(III)、Fe(II)分别处于
(4)25℃时,将10mL0.03mol/LNH4Cl溶液和10mL0.01mol/LAgNO3溶液混合(忽略溶液混合后的体积变化),混合后溶液中c(Ag+)为

a.b点可能加入了NH4Cl(s) b.c点后无黄色沉淀生成
c.d点c(Ag+)<c(Cl-) d.由图可知:Ksp(AgI)<Ksp(AgCl)
(5)1939年捷姆金和佩热夫推出氨合成反应在接近平衡时净速率方程式为r(NH3)=k1p(N2)
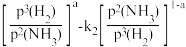 ,k1、k2分别为正反应和逆反应的速率常数;p(N2)、p(H2)、p(NH3)代表各组分的分压(分压=总压×物质的量分数);a为常数,工业上以铁为催化剂时,a=0.5。在一定条件下,向某容器中投入5molN2、15molH2,平衡时氨质量分数占40%,压强为32MPa.由此计算
,k1、k2分别为正反应和逆反应的速率常数;p(N2)、p(H2)、p(NH3)代表各组分的分压(分压=总压×物质的量分数);a为常数,工业上以铁为催化剂时,a=0.5。在一定条件下,向某容器中投入5molN2、15molH2,平衡时氨质量分数占40%,压强为32MPa.由此计算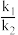 =
=
您最近一年使用:0次



