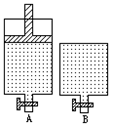
P(g)十Q(g) R(s),对此反应来说,下列能影响其反应速率的因素是:①温度②压强③生成物的浓度
R(s),对此反应来说,下列能影响其反应速率的因素是:①温度②压强③生成物的浓度
 R(s),对此反应来说,下列能影响其反应速率的因素是:①温度②压强③生成物的浓度
R(s),对此反应来说,下列能影响其反应速率的因素是:①温度②压强③生成物的浓度 | A.只有① | B.①和② | C.①和③ | D.②和③ |
9-10高一下·北京·期末 查看更多[1]
(已下线)2010年北京五中高一下学期期末考试化学试题
更新时间:2016-12-09 00:53:21
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列根据实验操作及现象所得出的结论正确的是
| 选项 | 实验操作及现象 | 结论 |
| A | 淀粉溶液和稀硫酸混合加热后,再加新制的 悬浊液加热,无砖红色沉淀产生 悬浊液加热,无砖红色沉淀产生 | 淀粉未水解 |
| B | 向氢氧化钠溶液中先加入少量 溶液,充分反应后再加入少量 溶液,充分反应后再加入少量 溶液,先产生白色沉淀,后产生蓝色沉淀 溶液,先产生白色沉淀,后产生蓝色沉淀 | 室温下, 比 比 的溶度积小 的溶度积小 |
| C | 向两支试管中分别加入 和 和 溶液,再向盛有 溶液,再向盛有 溶液的试管中加入 溶液的试管中加入 蒸馏水,最后同时向两支试管中加 蒸馏水,最后同时向两支试管中加 溶液,振荡,加入 溶液,振荡,加入 溶液的试管先出现浑浊 溶液的试管先出现浑浊 | 其他条件一定时,反应物浓度越大,反应速率越快 |
| D | 将 通入酸性 通入酸性 溶液中,取反应后的溶液于试管中,再向试管中加入 溶液中,取反应后的溶液于试管中,再向试管中加入 溶液,振荡,产生白色沉淀 溶液,振荡,产生白色沉淀 | 该环境中 的氧化产物为 的氧化产物为 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】已知放热反应 在密闭容器中进行。图中曲线a代表一定条件下该反应的过程,若使曲线b变为曲线a,可采取的措施是
在密闭容器中进行。图中曲线a代表一定条件下该反应的过程,若使曲线b变为曲线a,可采取的措施是
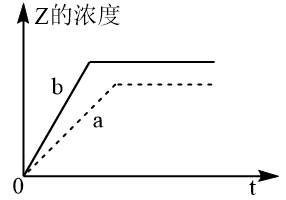
 在密闭容器中进行。图中曲线a代表一定条件下该反应的过程,若使曲线b变为曲线a,可采取的措施是
在密闭容器中进行。图中曲线a代表一定条件下该反应的过程,若使曲线b变为曲线a,可采取的措施是
| A.恒温恒容条件下,增大X和Y的初始投料比 |
| B.恒温条件下加压(减小容器的容积) |
C.恒温恒压条件下通入与反应无关的 |
| D.降低温度 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】科学家研究N2在催化剂表面与水能生成NH3:2N2(g)+6H2O(l) 4NH3(g)+3O2(g),下表是同一时间段(2h)NH3生成量与温度的关系,下列说法正确的是
4NH3(g)+3O2(g),下表是同一时间段(2h)NH3生成量与温度的关系,下列说法正确的是
 4NH3(g)+3O2(g),下表是同一时间段(2h)NH3生成量与温度的关系,下列说法正确的是
4NH3(g)+3O2(g),下表是同一时间段(2h)NH3生成量与温度的关系,下列说法正确的是 | T/K | 313 | 323 | 333 | 383 |
| NH3生成量/(mol) | 4.5 | 5.2 | 6.0 | 2.0 |
| A.该反应为吸热反应 |
| B.可通过适当增大压强来提高该反应速率 |
| C.323K时,该反应已经达到平衡状态 |
| D.333K时,该反应的平均反应速率为v(NH3)=6.0mol•h-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】CO可用于合成甲醇,反应的化学方程式为
 ,在密闭容器中充入一定量的CO和
,在密闭容器中充入一定量的CO和 ,在不同温度和压强下,CO的平衡转化率a如图所示。下列说法正确的
,在不同温度和压强下,CO的平衡转化率a如图所示。下列说法正确的
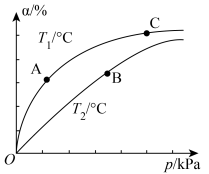

 ,在密闭容器中充入一定量的CO和
,在密闭容器中充入一定量的CO和 ,在不同温度和压强下,CO的平衡转化率a如图所示。下列说法正确的
,在不同温度和压强下,CO的平衡转化率a如图所示。下列说法正确的
A.温度: |
| B.增大体系压强,平衡向右移动,化学平衡常数K增大 |
C. |
D.A、B、C三点的平衡常数关系为 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】把在空气中久置的铝片5.0 g投入盛有500 mL0.5 mol/L H2SO4溶液的烧杯中,该铝片与硫酸反应产生氢气的速率v与反应时间t的关系可用下图来表示,下列说法错误的是


| A.O→a段不产生氢气是因为铝表面的氧化物隔离子铝和H2SO4溶液 |
| B.b→c段产生氢气的速率加快的主要原因是温度升高 |
| C.c时刻反应处于平衡状态 |
| D.c时刻之后,产生氢气的速率降低主要是因为溶液中c(H+)降低 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】少量铁粉与100mL0.01mol·L-1的稀盐酸反应,反应速率太慢,为了加快此反应速率而不改变H2的量,可以使用如下方法中的( )
①由铁粉换铁块②加NaNO3固体③将0.01mol·L-1的稀盐酸换成98%的硫酸溶液④改用100mL0.1mol·L-1盐酸 ⑤加NaCl溶液⑥滴入几滴硫酸铜溶液⑦升高温度(不考虑盐酸挥发)
①由铁粉换铁块②加NaNO3固体③将0.01mol·L-1的稀盐酸换成98%的硫酸溶液④改用100mL0.1mol·L-1盐酸 ⑤加NaCl溶液⑥滴入几滴硫酸铜溶液⑦升高温度(不考虑盐酸挥发)
| A.③⑤ | B.①③ | C.⑥⑦ | D.④⑦ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】下列条件下进行反应2H2O2=2H2O+O2↑,其中反应速率最快的是
| 选项 | H2O2的质量分数 | 温度 | 催化剂 |
| A | 10% | 5℃ | MnO2 |
| B | 10% | 40℃ | |
| MnO2 | |||
| C | 20% | 5℃ | 无 |
| D | 20% | 40℃ | MnO2 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】在锌与某浓度的盐酸反应的实验中,得到如下结果:
下列说法中,正确的是
①t1<t2 ②t1>150 ③实验1和实验2比较,单位时间内消耗的锌的质量前者小于后者
| 实验序号 | 锌的质量/g | 锌的形状 | 温度/℃ | 锌完全溶解于酸的时间/s |
1 | 2 | 薄片 | 15 | 150 |
2 | 2 | 薄片 | 35 | t1 |
3 | 2 | 粉末 | 35 | t2 |
①t1<t2 ②t1>150 ③实验1和实验2比较,单位时间内消耗的锌的质量前者小于后者
| A.只有① | B.①② | C.只有③ | D.②③ |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列关于化学反应速率和化学反应方向说法正确的是
| A.常温下,形状大小相同的锌片和铁片分别与同浓度的稀硫酸反应,速率:锌片>铁片 |
| B.放热反应都能自发进行 |
| C.增大体系压强,反应速率一定增大 |
| D.增加反应物浓度,正反应速率一定增大,逆反应速率一定减小 |
您最近一年使用:0次