室温下等体积的酸和碱混合,混合溶液的pH一定等于7的是
| A.pH=3的盐酸和pH=11的氨水 |
| B.pH=3的硝酸和pH=11的Ba(OH)2溶液 |
| C.pH=3的硫酸和pH=11的氨水 |
| D.pH=3的醋酸和pH=11的Ba(OH)2溶液 |
更新时间:2016-05-20 18:29:14
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】在25℃时,下列说法正确的是
A.常温下 的 的 溶液与 溶液与 的 的 等体积混合,溶液 等体积混合,溶液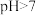 ,则 ,则 为强碱 为强碱 |
B. 与 与 的混合溶液中 的混合溶液中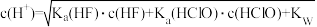 |
C.向 的氨水中加入少量硫酸铵固体,则溶液中 的氨水中加入少量硫酸铵固体,则溶液中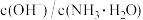 增大 增大 |
D. 的 的 溶液中加入少量 溶液中加入少量 晶体(碳酸钠没有被沉淀完全), 晶体(碳酸钠没有被沉淀完全), 水解程度减小,溶液的 水解程度减小,溶液的 减小 减小 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列说法正确的是 ( )
| A.用0.2000 mol·L-1 NaOH标准溶液滴定HCl与CH3COOH的混合溶液(混合液中两种酸的浓度均约为0.1 mol·L-1),至中性时,溶液中的酸未被完全中和 |
| B.为确定某酸H2A是强酸还是弱酸,可测NaHA溶液的pH。若pH>7,则H2A是弱酸;若pH<7,则H2A是强酸 |
| C.常温下,将pH=3的醋酸溶液稀释到原体积的10倍后,溶液的pH=4 |
| D.相同温度下,将足量氯化银固体分别放入相同体积的①蒸馏水、②0.1 mol·L-1盐酸、③0.1 mol·L-1氯化镁溶液、④0.1 mol·L-1硝酸银溶液中,Ag+浓度:①>④=②>③ |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】常温下,用0.1000 mol/L的盐酸滴定20.00 mL未知浓度的一元碱BOH溶液。溶液中,pH、B+的分布系数δ随滴加盐酸体积VHCl的变化关系如图所示。已知B+的分布系数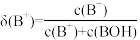 。下列叙述正确的是
。下列叙述正确的是

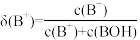 。下列叙述正确的是
。下列叙述正确的是
| A.BOH的电离常数Kb=1.0× 10-6 |
| B.滴定时,可以选择甲基橙作指示剂 |
| C.滴定过程中,水的电离程度: n<m<p |
| D.n点溶液中,粒子浓度大小为c(Cl-)>c(B+)> c(BOH) |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】实验室探究 溶液与碱反应的规律。实验数据和现象如下表所示(溶液体积均取用
溶液与碱反应的规律。实验数据和现象如下表所示(溶液体积均取用 )。
)。
下列说法正确的是
 溶液与碱反应的规律。实验数据和现象如下表所示(溶液体积均取用
溶液与碱反应的规律。实验数据和现象如下表所示(溶液体积均取用 )。
)。组别 | 药品1 | 药品2 | 实验现象 |
Ⅰ |
|
| 生成白色沉淀 |
Ⅱ |
|
| 无现象 |
Ⅲ |
|
| 生成白色沉淀 |
Ⅳ |
|
| 现象Ⅳ |
Ⅴ |
|
| 无现象 |
A.Ⅲ中反应的离子方程式为: |
B.Ⅲ中 是Ⅱ中 是Ⅱ中 的10倍,因此Ⅱ中无现象而Ⅲ中有沉淀 的10倍,因此Ⅱ中无现象而Ⅲ中有沉淀 |
| C.现象Ⅳ无法通过预测确定 |
D.上述实验说明: 溶液与氨水反应时,改变相同浓度时,氨水的影响大于氯化镁 溶液与氨水反应时,改变相同浓度时,氨水的影响大于氯化镁 |
您最近半年使用:0次

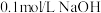 溶液
溶液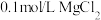 溶液
溶液 氨水
氨水 氨水
氨水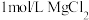 溶液
溶液 随pH的变化关系如图所示.下列说法不正确的是
随pH的变化关系如图所示.下列说法不正确的是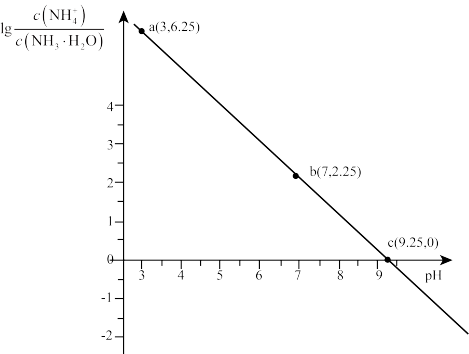
 点溶液中:c(NH
点溶液中:c(NH )>c(Cl-)
)>c(Cl-)

