氯化亚铜是一种重要的化工产品,常用作有机合成催化剂,还可用于颜料, 防腐等工业。该物质露置于空气中易被氧化为绿色的高价铜盐,在热水中易水解生成氧化铜水合物而呈红色。已知pH为5时,+2价铜已开始以碱式盐的形式沉淀。某兴趣小组去一家回收含铜电缆废料的工厂做社会调查,技术人员向他们展示了处理废料的综合利用方案:
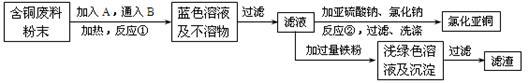
⑴ 加入的A是_____ ,通入的B是________ 。
⑵ 反应②的离子方程式是_______________ 。为提高Cu2Cl2的产率,常在反应②的溶液中加入适量稀碱溶液,控制pH为3.5。这样做的目的是________ 。
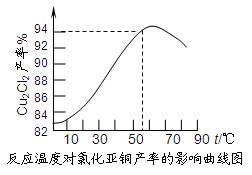
⑶ 保持各反应物的最佳配比,改变温度,测得Cu2Cl2产率的变化如下图所示。则溶液温度控制在________ 时,Cu2Cl2的产率已达到94%,当温度高于65℃时,Cu2Cl2产率会下降,其原因可能是______________ 。


⑴ 加入的A是
⑵ 反应②的离子方程式是
⑶ 保持各反应物的最佳配比,改变温度,测得Cu2Cl2产率的变化如下图所示。则溶液温度控制在
10-11高三上·江苏泰州·阶段练习 查看更多[1]
(已下线)2011届江苏省姜堰市二中高三上学期学情调查(三)化学试卷
更新时间:2011-01-14 11:31:31
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】聚合硫酸铁是一种新型高效净水剂。以黄铁矿(主要成分:FeS2,铁的化合价为+2价)烧渣(主要成分为Fe2O3、FeO、SiO2等)为原料制取聚合硫酸铁(铁的化合价为+3价)的实验步骤如下:

回答下列问题:
(1)用98%的浓硫酸配制28%的稀硫酸,需要的玻璃仪器除玻璃棒外,还需要________ (填写仪器名称)。
(2)“煅烧”过程发生反应的氧化产物是___________________________ ;SO2氧化为SO3是工业生产硫酸的重要反应,写出该反应的化学方程式_______________________ 。
(3)写出“酸浸”过程中发生反应的离子方程式___________________________ 。
(4)“氧化”过程中先产生无色气体,最终变成红棕色气体,写出加入NaNO3产生无色气体反应的离子方程式______________________________ ,若用H2O2代替NaNO3达到相同氧化效果,消耗H2O2和NaNO3的物质的量之比___________ 。
(5)为确定产品是否合格,需测定聚合硫酸铁中Fe3+和SO42-的物质的量之比,测定时需要的试剂为___________ (填写序号)。
a. FeSO4 b. BaCl2 c. NaOH d. NaCl

回答下列问题:
(1)用98%的浓硫酸配制28%的稀硫酸,需要的玻璃仪器除玻璃棒外,还需要
(2)“煅烧”过程发生反应的氧化产物是
(3)写出“酸浸”过程中发生反应的离子方程式
(4)“氧化”过程中先产生无色气体,最终变成红棕色气体,写出加入NaNO3产生无色气体反应的离子方程式
(5)为确定产品是否合格,需测定聚合硫酸铁中Fe3+和SO42-的物质的量之比,测定时需要的试剂为
a. FeSO4 b. BaCl2 c. NaOH d. NaCl
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】二氯化硫(SCl2)是一种红棕色液体,可用作于制造杀虫剂。 与水反应可生成
与水反应可生成 、
、 和
和 。为验证
。为验证 与水反应的产物,某小组设计如下图所示装置进行实验:
与水反应的产物,某小组设计如下图所示装置进行实验:
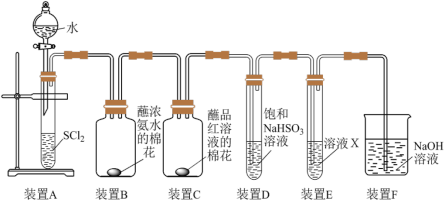
(1)SCl2分子中,各原子均满足最外层8电子稳定结构。 的电子式为
的电子式为___________ 。
(2)SCl2与水反应的化学方程式为___________ 。
(3)装置B、C中的实验现象分别为___________ 和___________ 。
(4)若溶液X为 ,实验中可观察到的现象是
,实验中可观察到的现象是___________ ,该现象表现了 的
的___________ 性。
(5)若溶液 为Ba(NO3)2溶液,写出该反应的离子方程式
为Ba(NO3)2溶液,写出该反应的离子方程式___________ 。
(6)工业上有多种方法可用于SO2的脱除。其中之一是用NaClO溶液作为吸收剂,调pH至5.5时吸收SO2,反应离子方程式是___________ 。
 与水反应可生成
与水反应可生成 、
、 和
和 。为验证
。为验证 与水反应的产物,某小组设计如下图所示装置进行实验:
与水反应的产物,某小组设计如下图所示装置进行实验:
(1)SCl2分子中,各原子均满足最外层8电子稳定结构。
 的电子式为
的电子式为(2)SCl2与水反应的化学方程式为
(3)装置B、C中的实验现象分别为
(4)若溶液X为
 ,实验中可观察到的现象是
,实验中可观察到的现象是 的
的(5)若溶液
 为Ba(NO3)2溶液,写出该反应的离子方程式
为Ba(NO3)2溶液,写出该反应的离子方程式(6)工业上有多种方法可用于SO2的脱除。其中之一是用NaClO溶液作为吸收剂,调pH至5.5时吸收SO2,反应离子方程式是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】 是石油化学工业的一种重要催化剂,其中Ag起催化作用,
是石油化学工业的一种重要催化剂,其中Ag起催化作用,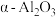 是载体且不溶于硝酸,该催化剂的回收实验如图1所示.其中的转化反应为:
是载体且不溶于硝酸,该催化剂的回收实验如图1所示.其中的转化反应为:

阅读上述实验流程,完成下列填空:
 加酸溶解应该选用装置
加酸溶解应该选用装置 图
图
______  选填a、b、
选填a、b、 .
.
 在实验操作
在实验操作 Ⅱ
Ⅱ ,如果用自来水代替蒸馏水进行洗涤,将会发生化学反应的离子方程式
,如果用自来水代替蒸馏水进行洗涤,将会发生化学反应的离子方程式 ______ .
 实验操作
实验操作 Ⅳ
Ⅳ 所需玻璃仪器为
所需玻璃仪器为 ______  填写三种
填写三种 .
.
 实验操作
实验操作 Ⅶ
Ⅶ 从
从 溶液获得
溶液获得 晶体需要进行的实验操作依次为:
晶体需要进行的实验操作依次为: ______  多选扣分
多选扣分 .
.
 蒸馏
蒸馏  蒸发
蒸发  灼烧
灼烧 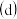 冷却结晶
冷却结晶
 已知:
已知: ;
;

NO和 的混合气体的组成可表示为
的混合气体的组成可表示为 该混合气体通入NaOH溶液被完全吸收时,x的值为
该混合气体通入NaOH溶液被完全吸收时,x的值为 ______
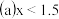
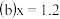

 已知
已知 中Ag的质量分数,若计算Ag的回收率,还必须知道的实验数据为
中Ag的质量分数,若计算Ag的回收率,还必须知道的实验数据为 ______ 和 ______ .
 是石油化学工业的一种重要催化剂,其中Ag起催化作用,
是石油化学工业的一种重要催化剂,其中Ag起催化作用,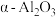 是载体且不溶于硝酸,该催化剂的回收实验如图1所示.其中的转化反应为:
是载体且不溶于硝酸,该催化剂的回收实验如图1所示.其中的转化反应为:

阅读上述实验流程,完成下列填空:
 加酸溶解应该选用装置
加酸溶解应该选用装置 图
图
 选填a、b、
选填a、b、 .
. 在实验操作
在实验操作 Ⅱ
Ⅱ ,如果用自来水代替蒸馏水进行洗涤,将会发生化学反应的离子方程式
,如果用自来水代替蒸馏水进行洗涤,将会发生化学反应的离子方程式  实验操作
实验操作 Ⅳ
Ⅳ 所需玻璃仪器为
所需玻璃仪器为  填写三种
填写三种 .
. 实验操作
实验操作 Ⅶ
Ⅶ 从
从 溶液获得
溶液获得 晶体需要进行的实验操作依次为:
晶体需要进行的实验操作依次为:  多选扣分
多选扣分 .
. 蒸馏
蒸馏  蒸发
蒸发  灼烧
灼烧 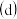 冷却结晶
冷却结晶  已知:
已知: ;
; 
NO和
 的混合气体的组成可表示为
的混合气体的组成可表示为 该混合气体通入NaOH溶液被完全吸收时,x的值为
该混合气体通入NaOH溶液被完全吸收时,x的值为 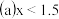
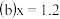

 已知
已知 中Ag的质量分数,若计算Ag的回收率,还必须知道的实验数据为
中Ag的质量分数,若计算Ag的回收率,还必须知道的实验数据为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】价类二维图是学习元素及其化合物知识的重要模型。它是以元素化合价为纵坐标,以物质类别为横坐标的二维平面图像。如图为氯元素的价类二维图。回答下列问题:

(1)上述6种物质,属于电解质有_______ 种 。
(2)⑤与⑥在酸性条件下反应的离子方程式为_______________________ 。
(3)将②与SO2按1∶1通入紫色石蕊试液中,现象为_____ ,解释原因(写离子方程式)______ 。
(4)管道工人通常用浓氨水检查输送②的管道是否漏气,如果有白烟现象,则说明管道漏气,写出产生该现象的化学方程式______________ 。
(5)③是国际上公认的对饮用水、食品等杀菌消毒的理想药剂。商业上常用“有效氯”来说明消毒剂的消毒能力。“有效氯”指的是一定质量的这种消毒剂与多少质量的氯气的氧化能力相当,其数值用此时的氯气的质量对消毒剂质量的百分比来表示。例如,100g某84消毒液与3.55g氯气的氧化能力相当,该产品的“有效氯”就是3.55%。据此计算试剂③的“有效氯”为___________ (保留三位有效数字)。

(1)上述6种物质,属于电解质有
(2)⑤与⑥在酸性条件下反应的离子方程式为
(3)将②与SO2按1∶1通入紫色石蕊试液中,现象为
(4)管道工人通常用浓氨水检查输送②的管道是否漏气,如果有白烟现象,则说明管道漏气,写出产生该现象的化学方程式
(5)③是国际上公认的对饮用水、食品等杀菌消毒的理想药剂。商业上常用“有效氯”来说明消毒剂的消毒能力。“有效氯”指的是一定质量的这种消毒剂与多少质量的氯气的氧化能力相当,其数值用此时的氯气的质量对消毒剂质量的百分比来表示。例如,100g某84消毒液与3.55g氯气的氧化能力相当,该产品的“有效氯”就是3.55%。据此计算试剂③的“有效氯”为
您最近一年使用:0次
【推荐2】煤燃烧的尾气是造成雾霾天气的原因之一,下列是一种变废为宝的处理方法

(1)上述流程中循环使用的物质有__________ ,吸收池Ⅰ吸收的气体有__________ 。
(2)向吸收池Ⅳ得到的 溶液中滴加CaCl2溶液,出现浑浊,pH降低,用平衡移动原理解释溶液pH降低的原因
溶液中滴加CaCl2溶液,出现浑浊,pH降低,用平衡移动原理解释溶液pH降低的原因__________ 。
(3)电解池Ⅴ制得 的原理如图a所示写出电解总反应的离子方程式
的原理如图a所示写出电解总反应的离子方程式__________ 。

(4)1molCO(g)和1molNO2(g)反应生成1molCO2(g)和1molNO(g),反应过程中的能量变化如图b,已知:①N2(g)+O2(g)=2NO(g)ΔH=+179.5kJ/mol
②2NO(g)+O2(g)=2NO2(g)ΔH=-112.3kJ/mol
请写出NO与CO反应生成无污染气体的热化学方程式__________ 。
(5)氧化池Ⅵ发生反应的离子方程式为__________ 。

(1)上述流程中循环使用的物质有
(2)向吸收池Ⅳ得到的
 溶液中滴加CaCl2溶液,出现浑浊,pH降低,用平衡移动原理解释溶液pH降低的原因
溶液中滴加CaCl2溶液,出现浑浊,pH降低,用平衡移动原理解释溶液pH降低的原因(3)电解池Ⅴ制得
 的原理如图a所示写出电解总反应的离子方程式
的原理如图a所示写出电解总反应的离子方程式
(4)1molCO(g)和1molNO2(g)反应生成1molCO2(g)和1molNO(g),反应过程中的能量变化如图b,已知:①N2(g)+O2(g)=2NO(g)ΔH=+179.5kJ/mol
②2NO(g)+O2(g)=2NO2(g)ΔH=-112.3kJ/mol
请写出NO与CO反应生成无污染气体的热化学方程式
(5)氧化池Ⅵ发生反应的离子方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】化学工业为疫情防控提供了强有力的物质支撑。氯的许多化合物既是重要化工原料,又是高效广谱的灭菌消毒剂。棕黄色的 气体是次氯酸的酸酐,溶于水生成次氯酸,实验室模拟工业制备次氯酸的装置如图所示(夹持装置已略)。
气体是次氯酸的酸酐,溶于水生成次氯酸,实验室模拟工业制备次氯酸的装置如图所示(夹持装置已略)。

已知:
① 气体在42℃以上会发生分解,浓度过大会发生爆炸;
气体在42℃以上会发生分解,浓度过大会发生爆炸;
②工业上用氯气与潮湿的碳酸钠反应制得 ,同时生成两种钠盐该反应放热。
,同时生成两种钠盐该反应放热。
(1)仪器m的名称___________ ;装置A中发生反应的离子反应方程式___________ ;
(2)装置B中盛放的适宜试剂是___________ ;B中通入空气的原因是___________ ;
(3)装置C中主要发生反应的化学方程式___________ ;
(4)实验中,装置C需要冷却的原因是___________ ;
(5)装置D中多孔球泡的作用___________ ;装置E中碱石灰的作用是___________ ;
(6)此法相对于用氯气直接溶于水制备次氯酸溶液的优点是___________ (答出一条即可)。
 气体是次氯酸的酸酐,溶于水生成次氯酸,实验室模拟工业制备次氯酸的装置如图所示(夹持装置已略)。
气体是次氯酸的酸酐,溶于水生成次氯酸,实验室模拟工业制备次氯酸的装置如图所示(夹持装置已略)。
已知:
①
 气体在42℃以上会发生分解,浓度过大会发生爆炸;
气体在42℃以上会发生分解,浓度过大会发生爆炸;②工业上用氯气与潮湿的碳酸钠反应制得
 ,同时生成两种钠盐该反应放热。
,同时生成两种钠盐该反应放热。(1)仪器m的名称
(2)装置B中盛放的适宜试剂是
(3)装置C中主要发生反应的化学方程式
(4)实验中,装置C需要冷却的原因是
(5)装置D中多孔球泡的作用
(6)此法相对于用氯气直接溶于水制备次氯酸溶液的优点是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】溴化亚铜(CuBr)微溶于水,不溶于乙醇,可用作有机合成中的催化剂。实验室中可利用无水硫酸铜、溴化钠为主要原料制备溴化亚铜,制备流程如下:

回答下列问题:
(1)过程①用到的玻璃仪器有烧杯、_____ ,其中无水CuSO4能否用蓝矾代替?做出判断,并说明理由:_______ 。
(2)制备CuBr的反应在装置乙中进行,向其中加入32 g CuSO4和23 g NaBr配制成的150 mL水溶液,然后通入足量的SO2(部分夹持及加热装置已略去)。

①装置甲中的反应_____ (填“是”或“不是”)氧化还原反应,该装置中不能采用浓度为98%的浓硫酸,一般采用浓度为70%左右的浓硫酸,其原因是______ 。
②装置乙的名称为______ ,写出装置乙中发生反应的离子方程式_____ ,该反应需保持反应液在60℃,最佳加热方式为_____ ,该装置中应用搅拌器搅拌的目的是_____ ,Cu2+、Br-反应完毕的标志是_____ 。
③丙中倒扣的漏斗可防止液体倒吸,下列装置中不能防止液体倒吸的是_____ (填标号)。

(3)洗涤CuBr沉淀时采用SO2的水溶液而不采用蒸馏水,其目的是_______ 。
(4)最后经洗涤、干燥得到21.6 g产品,则该实验的产率是________ 。

回答下列问题:
(1)过程①用到的玻璃仪器有烧杯、
(2)制备CuBr的反应在装置乙中进行,向其中加入32 g CuSO4和23 g NaBr配制成的150 mL水溶液,然后通入足量的SO2(部分夹持及加热装置已略去)。

①装置甲中的反应
②装置乙的名称为
③丙中倒扣的漏斗可防止液体倒吸,下列装置中不能防止液体倒吸的是

(3)洗涤CuBr沉淀时采用SO2的水溶液而不采用蒸馏水,其目的是
(4)最后经洗涤、干燥得到21.6 g产品,则该实验的产率是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】某无色透明溶液中可能大量含有 、
、 、
、 、
、 、
、 、
、 中的若干种,现对其进行如下实验:
中的若干种,现对其进行如下实验:
i:取少量该溶液,加入过量 溶液,产生白色沉淀,过滤;
溶液,产生白色沉淀,过滤;
ii:向i中所得沉淀中加入足量盐酸,沉淀全部溶解,并有无色气体生成;
iii:向i中所得滤液中加入足量硝酸酸化后,再加入 溶液,有白色沉淀生成。
溶液,有白色沉淀生成。
回答下列问题:
(1)无需实验即可推断溶液中一定不会大量存在的离子为___________ 。
(2)通过实验i可知溶液中一定不会大量存在的离子为___________ 。
(3)由实验ii可知溶液中一定不会大量存在的离子为___________ 。
(4)由上述实验得到结论:该溶液一定大量存在的离子为___________ ,可能大量存在的离子为___________ 。
(5)写出实验ii中沉淀溶解的离子方程式___________ 。
 、
、 、
、 、
、 、
、 、
、 中的若干种,现对其进行如下实验:
中的若干种,现对其进行如下实验:i:取少量该溶液,加入过量
 溶液,产生白色沉淀,过滤;
溶液,产生白色沉淀,过滤;ii:向i中所得沉淀中加入足量盐酸,沉淀全部溶解,并有无色气体生成;
iii:向i中所得滤液中加入足量硝酸酸化后,再加入
 溶液,有白色沉淀生成。
溶液,有白色沉淀生成。回答下列问题:
(1)无需实验即可推断溶液中一定不会大量存在的离子为
(2)通过实验i可知溶液中一定不会大量存在的离子为
(3)由实验ii可知溶液中一定不会大量存在的离子为
(4)由上述实验得到结论:该溶液一定大量存在的离子为
(5)写出实验ii中沉淀溶解的离子方程式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】铜是不活泼的金属,常见有+1价、+2价。为探究铜与其化合物的性质,完成了两组实验,部分记录如下:
第一组:
完成下列填空:
(1)铜不活泼,通常情况下,不与稀硫酸反应,但向铜和稀硫酸溶液中加入双氧水,溶液很快变蓝。请写出该反应的离子方程式:___________ 。
(2)写出本题试管1中发生反应的离子方程式:___________ 。
(3)试管2,预测步骤ii后溶液不应呈红色,依据是___________ 写出发生反应的离子方程式:______ 。
(4)经测定试管②中得到的白色沉淀是CuSCN。对生成CuSCN有两种猜测:
猜测①Cu2+和SCN-反应生成CuSCN,根据___________ ,推知这一猜测错误。
猜想②生成白色沉淀是因为:Cu++SCN-→CuSCN↓。再请结合步骤ii溶液出现红色的现象,解释生成沉淀的可能原因:___________ (用离子方程式表示)。
第二组:水合肼(N2H4·H2O)和碱性铜氨([Cu(NH3)4]2+)溶液混合反应生成铜。
(5)水合肼溶液显弱碱性,其电离与NH3·H2O相似,写出水合肼的电离方程式:___________ 。
(6)水合肼可用于还原锅炉水中溶解的O2,防止锅炉被腐蚀。与Na2SO3相比,使用水合肼处理水中溶解O2的优点是___________ (任写一点)。
第一组:
| 序号 | 试剂 | 实验步骤 | 实验现象 |
| ① | 试管1中加2mL 0.05mol·L-1 Fe2(SO4)3溶液 | 加入1mL 0.1mol·L-1 KSCN溶液 | 溶液变为红色 |
| ② | 试管2中加入2mL 0.05mol·L-1 Fe2(SO4)3溶液 | i 加入0.16g铜粉 | 黄色溶液变为浅蓝色 |
| ii 取上层清液,加入1滴0.1mol·L-1 KSCN溶液 | 液滴接触上方变为红色,下方有白色沉淀生成 | ||
| ③ | 试管3中加2mL 0.1mol·L-1 CuSO4溶液 | 加入1mL 0.1mol·L-1 KSCN溶液 | 溶液变为绿色 |
(1)铜不活泼,通常情况下,不与稀硫酸反应,但向铜和稀硫酸溶液中加入双氧水,溶液很快变蓝。请写出该反应的离子方程式:
(2)写出本题试管1中发生反应的离子方程式:
(3)试管2,预测步骤ii后溶液不应呈红色,依据是
(4)经测定试管②中得到的白色沉淀是CuSCN。对生成CuSCN有两种猜测:
猜测①Cu2+和SCN-反应生成CuSCN,根据
猜想②生成白色沉淀是因为:Cu++SCN-→CuSCN↓。再请结合步骤ii溶液出现红色的现象,解释生成沉淀的可能原因:
第二组:水合肼(N2H4·H2O)和碱性铜氨([Cu(NH3)4]2+)溶液混合反应生成铜。
(5)水合肼溶液显弱碱性,其电离与NH3·H2O相似,写出水合肼的电离方程式:
(6)水合肼可用于还原锅炉水中溶解的O2,防止锅炉被腐蚀。与Na2SO3相比,使用水合肼处理水中溶解O2的优点是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】我国有广阔的海岸线,海水是巨大的资源宝库,海水淡化及其综合利用具有重要意义。请回答下列问题:

(1)历史最久,技术和工艺也比较成熟,但成本较高的海水淡化的方法是___________ 法:
(2)步骤1中,粗盐中含有Ca2+、Mg2+、 等杂质离子,精制时常用的试剂有:①稀盐酸;②氯化钡溶液;③氢氧化钠溶液;④碳酸钠溶液。下列加入试剂的顺序正确的是_______(填字母)
等杂质离子,精制时常用的试剂有:①稀盐酸;②氯化钡溶液;③氢氧化钠溶液;④碳酸钠溶液。下列加入试剂的顺序正确的是_______(填字母)
(3)步骤II通入热空气或水蒸气吹出Br2,利用了溴的___________(填字母)
(4)写出步骤III反应的离子方程式___________ ;
(5)从理论上考虑,下列物质的溶液也能与Br2反应的是___________(填字母)
(6)在实验室中可以用萃取的方法提取溴,可选用的试剂是___________ (填字母)
A.乙醇 B.乙酸 C.裂化汽油 D.四氯化碳
所用主要玻璃仪器的名称是___________ 。

(1)历史最久,技术和工艺也比较成熟,但成本较高的海水淡化的方法是
(2)步骤1中,粗盐中含有Ca2+、Mg2+、
 等杂质离子,精制时常用的试剂有:①稀盐酸;②氯化钡溶液;③氢氧化钠溶液;④碳酸钠溶液。下列加入试剂的顺序正确的是_______(填字母)
等杂质离子,精制时常用的试剂有:①稀盐酸;②氯化钡溶液;③氢氧化钠溶液;④碳酸钠溶液。下列加入试剂的顺序正确的是_______(填字母)| A.①②③④ | B.②③④① | C.④③②① | D.③④②① |
| A.氧化性 | B.还原性 | C.挥发性 | D.腐蚀性 |
(5)从理论上考虑,下列物质的溶液也能与Br2反应的是___________(填字母)
| A.NaCl | B.Na2CO3 | C.Na2SO4 | D.FeCl3 |
A.乙醇 B.乙酸 C.裂化汽油 D.四氯化碳
所用主要玻璃仪器的名称是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】目前世界上60%的镁是从海水中提取的。学生就这个课题展开了讨论的。已知海水提镁的主要步骤如下:

学生就这个课题提出了以下问题:
(一)在海水提镁的过程中如何实现对镁离子的富集?
有三个学生提出自己的观点。
学生甲的观点:直接往海水中加入沉淀剂。
学生乙的观点:高温加热蒸发海水后,再加入沉淀剂。
学生丙的观点:利用晒盐后的苦卤水,再加入沉淀剂。
请你评价三个学生提出的观点是否正确(填是或否),并简述理由。
(二)在海水提镁的过程中如何实现对镁离子的分离?
(1)为了使镁离子沉淀下来,加入的足量试剂①是_______ (填化学式)。
(2)加入的足量试剂②是_______ (填化学式)。
(3)试从节约能源,提高金属镁的纯度分析,以下适宜的冶镁方法是________ 。
A.
B.
C.
D.

学生就这个课题提出了以下问题:
(一)在海水提镁的过程中如何实现对镁离子的富集?
有三个学生提出自己的观点。
学生甲的观点:直接往海水中加入沉淀剂。
学生乙的观点:高温加热蒸发海水后,再加入沉淀剂。
学生丙的观点:利用晒盐后的苦卤水,再加入沉淀剂。
请你评价三个学生提出的观点是否正确(填是或否),并简述理由。
| 是否正确 | 简述理由 | |
| 学生甲的观点 | ||
| 学生乙的观点 | ||
| 学生丙的观点 |
(二)在海水提镁的过程中如何实现对镁离子的分离?
(1)为了使镁离子沉淀下来,加入的足量试剂①是
(2)加入的足量试剂②是
(3)试从节约能源,提高金属镁的纯度分析,以下适宜的冶镁方法是
A.

B.

C.

D.

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】为了证明在实验室制备得到的Cl2中会混有HCl,甲同学设计了如图所示的实验装置,按要求回答下列问题。已知:湿润的KI−淀粉试纸遇Cl2能显蓝色。
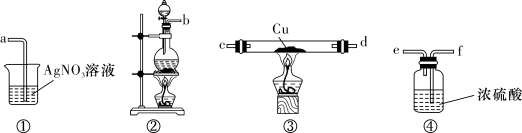
(1)请根据甲同学的示意图,将所需实验装置按从左至右的连接顺序:装置②→_______ 。
(2)装置②中滴加反应物的仪器名称是____ ,装置②中发生反应的离子方程式为_______ 。
(3)装置③中Cu的作用是_______ 。
(4)乙同学认为甲同学实验设计仍然存在缺陷,不能证明最终通入AgNO3溶液中的气体只有一种。为此,乙同学提出气体通入装置①之前,要加装一个检验装置⑤,以证明最终通入AgNO3溶液中的气体只有一种。你认为装置⑤应放入_______ 。
(5)丙同学看到甲同学设计的装置后提出无需多加装置,只需将原来烧杯中的AgNO3溶液换成紫色石蕊试液,如果观察到_______ 的现象,则证明制Cl2时有HCl挥发出来。

(1)请根据甲同学的示意图,将所需实验装置按从左至右的连接顺序:装置②→
(2)装置②中滴加反应物的仪器名称是
(3)装置③中Cu的作用是
(4)乙同学认为甲同学实验设计仍然存在缺陷,不能证明最终通入AgNO3溶液中的气体只有一种。为此,乙同学提出气体通入装置①之前,要加装一个检验装置⑤,以证明最终通入AgNO3溶液中的气体只有一种。你认为装置⑤应放入
(5)丙同学看到甲同学设计的装置后提出无需多加装置,只需将原来烧杯中的AgNO3溶液换成紫色石蕊试液,如果观察到
您最近一年使用:0次



