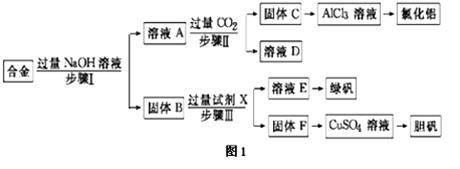
某工厂的废金属屑的主要成分为铝、铁和铜,某化学兴趣小组在学习了元素及其化合物的相关知识后,设计了如图1实验流程,用该工厂的金属废料制取氯化铝、绿矾晶体(FeSO4·7H2O)和胆矾晶体(CuSO4·5H2O)。
请回答:
(1)写出步骤Ⅱ反应的离子方程式:________________ 。
(2)步骤Ⅰ、Ⅱ、Ⅲ进行的实验操作中均需用到的玻璃仪有________________ 。
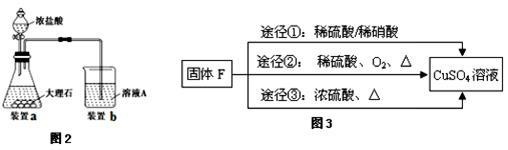
(3)进行步骤Ⅱ时,该小组用如图2所示装置及试剂制取CO2并将制得的气体通入溶液A中一段时间后,观察到烧杯中产生的白色沉淀会逐渐减少,原因是_________________ 。
(4)从溶液E得到绿矾晶体的实验操作是___________ 、___________ 过滤。
(5)用固体F制备CuSO4溶液,可设计如图3三种途径:
写出途径③中反应的化学方程式:_________________ ,用途径①制备CuSO4溶液时,混酸中硫酸和硝酸的最佳物质的量之比为_________ 。
(6)用惰性电极电解硫酸铜溶液一段时间后,阴极增重3.2g。阳极产生________ L气体(标准状况)。


请回答:
(1)写出步骤Ⅱ反应的离子方程式:
(2)步骤Ⅰ、Ⅱ、Ⅲ进行的实验操作中均需用到的玻璃仪有
(3)进行步骤Ⅱ时,该小组用如图2所示装置及试剂制取CO2并将制得的气体通入溶液A中一段时间后,观察到烧杯中产生的白色沉淀会逐渐减少,原因是
(4)从溶液E得到绿矾晶体的实验操作是
(5)用固体F制备CuSO4溶液,可设计如图3三种途径:
写出途径③中反应的化学方程式:
(6)用惰性电极电解硫酸铜溶液一段时间后,阴极增重3.2g。阳极产生
更新时间:2016-12-09 16:50:15
|
相似题推荐
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐1】五氧化二钒(V2O5)广泛用作合金添加剂及有机化工催化剂。从废钒催化剂(含有V2O5、VOSO4及少量Fe2O3、Al2O3等杂质)回收V2O5的部分工艺流程如下:
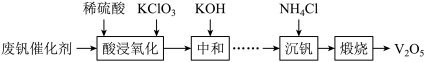
已知:a.常温下,部分含钒物质在水中的溶解性见下表:
b.+5价钒在溶液中的主要存在形式与溶液pH的关系见下表:
(1)“酸浸、氧化”时,VO2+发生反应的离子方程式为___________ 。
(2)“中和”时调节pH为7的目的,一是沉淀部分杂质离子;二是___________ 。
(3)①“沉钒”前需将溶液先进行“离子交换”和“洗脱”,再加入NH4Cl生成NH4VO3;“离子交换”和“洗脱”两步操作可表示为ROH+VO
 RVO3+OH-(ROH为强碱性阴离子交换树脂)。为了提高洗脱效率,淋洗液应该呈
RVO3+OH-(ROH为强碱性阴离子交换树脂)。为了提高洗脱效率,淋洗液应该呈___________ (填“酸性”或“碱性”),理由是___________ 。
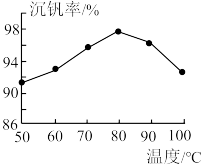
②用沉钒率(NH4VO3沉淀中V的质量和废钒催化剂中V的质量之比)表示该工艺钒的回收率。图1中是沉钒率随温度变化的关系曲线,沉钒时,温度超过80℃以后,沉钒率下降的可能原因是___________ 。
(4)在Ar气氛中加热“煅烧”NH4VO3,测得加热升温过程中固体的质量变化如图2所示,加热分解NH4VO3制备V2O5需要控制的温度为___________ 。


已知:a.常温下,部分含钒物质在水中的溶解性见下表:
| 物质 | V2O5 | VOSO4 | (VO2)2SO4 | NH4VO3 |
| 溶解性 | 难溶 | 可溶 | 易溶 | 难溶 |
| pH | <6 | 6~8 | 8~10 | 10~12 |
| 主要离子 | VO | VO | V2O | VO |
(1)“酸浸、氧化”时,VO2+发生反应的离子方程式为
(2)“中和”时调节pH为7的目的,一是沉淀部分杂质离子;二是
(3)①“沉钒”前需将溶液先进行“离子交换”和“洗脱”,再加入NH4Cl生成NH4VO3;“离子交换”和“洗脱”两步操作可表示为ROH+VO

 RVO3+OH-(ROH为强碱性阴离子交换树脂)。为了提高洗脱效率,淋洗液应该呈
RVO3+OH-(ROH为强碱性阴离子交换树脂)。为了提高洗脱效率,淋洗液应该呈②用沉钒率(NH4VO3沉淀中V的质量和废钒催化剂中V的质量之比)表示该工艺钒的回收率。图1中是沉钒率随温度变化的关系曲线,沉钒时,温度超过80℃以后,沉钒率下降的可能原因是

(4)在Ar气氛中加热“煅烧”NH4VO3,测得加热升温过程中固体的质量变化如图2所示,加热分解NH4VO3制备V2O5需要控制的温度为

您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐2】湿法炼锌综合回收系统产出的萃余液中含有 、
、 、
、 ,还含有
,还含有 、
、 、
、 、
、 、
、 、
、 等,一种将萃余液中有价离子分步分离、富集回收工艺流程如下:
等,一种将萃余液中有价离子分步分离、富集回收工艺流程如下:
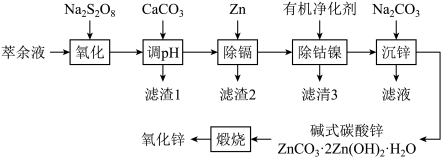
回答下列问题:
(1)“氧化”时, 、
、 均发生反应。后者发生反应时,氧化剂与还原剂的物质的量之比为
均发生反应。后者发生反应时,氧化剂与还原剂的物质的量之比为___________ 。
(2)“调pH”时,所得“滤渣1”中除含有 和
和 外,还有
外,还有___________ 。
(3)“除镉”时,发生反应的类型为___________ 。
(4)“除钴镍”时,有机净化剂的基本组分为大分子立体网格结构的聚合物。其净化原理可表示为:
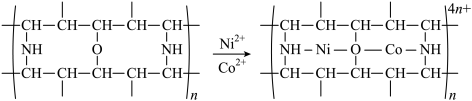
反应时,接受电子对的一方是___________ ; 、
、 能发生上述转化而
能发生上述转化而 不能,推测可能的原因为
不能,推测可能的原因为___________ 。
(5)“沉锌”时有气体生成,则生成碱式碳酸锌的离子方程式为___________ 。
(6)“沉锌”时,所得滤液经硫酸酸化后,用惰性电极电解可制备 ,从而实现原料的循环利用,该电解过程中总反应的化学方程式为
,从而实现原料的循环利用,该电解过程中总反应的化学方程式为___________ 。
 、
、 、
、 ,还含有
,还含有 、
、 、
、 、
、 、
、 、
、 等,一种将萃余液中有价离子分步分离、富集回收工艺流程如下:
等,一种将萃余液中有价离子分步分离、富集回收工艺流程如下:
回答下列问题:
(1)“氧化”时,
 、
、 均发生反应。后者发生反应时,氧化剂与还原剂的物质的量之比为
均发生反应。后者发生反应时,氧化剂与还原剂的物质的量之比为(2)“调pH”时,所得“滤渣1”中除含有
 和
和 外,还有
外,还有(3)“除镉”时,发生反应的类型为
(4)“除钴镍”时,有机净化剂的基本组分为大分子立体网格结构的聚合物。其净化原理可表示为:

反应时,接受电子对的一方是
 、
、 能发生上述转化而
能发生上述转化而 不能,推测可能的原因为
不能,推测可能的原因为(5)“沉锌”时有气体生成,则生成碱式碳酸锌的离子方程式为
(6)“沉锌”时,所得滤液经硫酸酸化后,用惰性电极电解可制备
 ,从而实现原料的循环利用,该电解过程中总反应的化学方程式为
,从而实现原料的循环利用,该电解过程中总反应的化学方程式为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐3】纳米级硒化铜 是钠离子电池的正极材料。某小组以黄铜矿粉末(主要含
是钠离子电池的正极材料。某小组以黄铜矿粉末(主要含 ,含少量
,含少量 、
、 等)为原料,在酸性条件下生物催化氧化法制备纳米级硒化铜的流程如图。
等)为原料,在酸性条件下生物催化氧化法制备纳米级硒化铜的流程如图。

请回答下列问题:
(1)“浸取”中,其他条件相同,测得温度与金属浸出率的关系如图所示。简述40℃达到峰值的原因:_______ 。
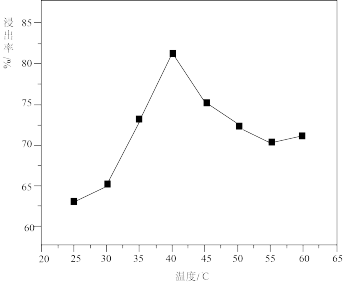
(2)写出“浸取”中 反应的离子方程式:
反应的离子方程式:_______ 。
(3)加入过量氨水时,反应分两步进行,写出 参与反应的化学方程式:
参与反应的化学方程式:_______ 。滤渣的主要成分是_______ (填化学式)。
(4)有人认为,用 或
或 代替氨水调节溶液的pH也可以达到相同的目的。请你判断此法是否可行:
代替氨水调节溶液的pH也可以达到相同的目的。请你判断此法是否可行:_______ 。若可行,需调节溶液的pH最低为_______ {若不可行,此空可不填。已知:常温下残留在溶液中的离子浓度小于 时,可认为沉淀完全,
时,可认为沉淀完全,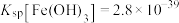 ,
,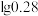 的值取-0.6}。
的值取-0.6}。
(5)在高压、加热条件下,用 还原
还原 溶液的反应中,氧化剂和还原剂的物质的量之比为
溶液的反应中,氧化剂和还原剂的物质的量之比为_______ 。
(6)已知Cu2-xSe晶胞结构如图所示,设晶胞参数为anm。
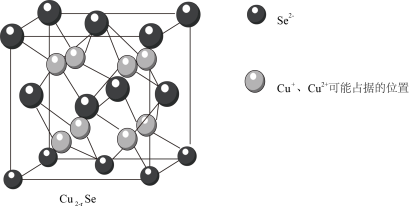
①该晶胞中 和
和 的个数比为
的个数比为_______ (用含 的代数式表示)。
的代数式表示)。
②该晶胞中 与
与 或
或 之间的最短距离为
之间的最短距离为_______  。
。
 是钠离子电池的正极材料。某小组以黄铜矿粉末(主要含
是钠离子电池的正极材料。某小组以黄铜矿粉末(主要含 ,含少量
,含少量 、
、 等)为原料,在酸性条件下生物催化氧化法制备纳米级硒化铜的流程如图。
等)为原料,在酸性条件下生物催化氧化法制备纳米级硒化铜的流程如图。
请回答下列问题:
(1)“浸取”中,其他条件相同,测得温度与金属浸出率的关系如图所示。简述40℃达到峰值的原因:

(2)写出“浸取”中
 反应的离子方程式:
反应的离子方程式:(3)加入过量氨水时,反应分两步进行,写出
 参与反应的化学方程式:
参与反应的化学方程式:(4)有人认为,用
 或
或 代替氨水调节溶液的pH也可以达到相同的目的。请你判断此法是否可行:
代替氨水调节溶液的pH也可以达到相同的目的。请你判断此法是否可行: 时,可认为沉淀完全,
时,可认为沉淀完全,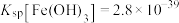 ,
,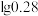 的值取-0.6}。
的值取-0.6}。(5)在高压、加热条件下,用
 还原
还原 溶液的反应中,氧化剂和还原剂的物质的量之比为
溶液的反应中,氧化剂和还原剂的物质的量之比为(6)已知Cu2-xSe晶胞结构如图所示,设晶胞参数为anm。

①该晶胞中
 和
和 的个数比为
的个数比为 的代数式表示)。
的代数式表示)。②该晶胞中
 与
与 或
或 之间的最短距离为
之间的最短距离为 。
。
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
【推荐1】苯胺在染料、医药、农药、香料等领域有广泛的应用,实验室可在酸性溶液中用铁还原硝基苯制取苯胺。实验流程如下:

已知:a.反应方程式为:4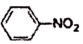 +9Fe+4H2O
+9Fe+4H2O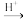 4
4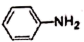 +3Fe3O4 (剧烈放热)
+3Fe3O4 (剧烈放热)
b.苯胺有碱性,与酸溶液反应生成可溶性盐。
c.相关物质物理性质如下:
(1)步骤I在250 mL三颈烧瓶中加入40 g铁屑和50 mL水,然后加入2 mL冰醋酸,最后再加硝基苯。硝基苯须缓慢滴加,其原因可能是___________ 。
(2)步骤II在小火加热下反应回流约1小时。步骤I、II需用到的仪器除三颈烧瓶等之外,还需以下的___________ 。
A.搅拌器B. 球形冷凝管C.分液漏斗D.恒压滴液漏斗
(3)步骤II,多步操作为:
①反应完全后,冷却,边搅拌边加入氢氧化钠至反应物呈碱性;
②用少量水冲洗冷凝管和搅拌器,洗涤液并入三颈烧瓶中;
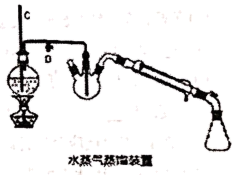
③如图组装好水蒸气蒸馏装置,进行水蒸气蒸馏得到苯胺粗产品。(注:水蒸气蒸馏是将水蒸气通入不溶或微溶于水的有机物中,使待提纯的有机物随水蒸气一起被蒸馏出来,从而达到分离提纯的目的。)
下列有关步骤II说法不正确的是___________ 。
A.操作①,可用甲基橙试液指示氢氧化钠的加入量
B.操作②,用水冲洗冷凝管和搅拌器,目的是除去杂质,以提高产品纯度
C.操作③,水蒸气蒸馏装置中导管C的作用是平衡气压,起到预警的作用
D.操作③,水蒸气蒸馏结束后,应先停止加热,再打开D处活塞,以防倒吸
步骤III提纯产品苯胺时,涉及以下部分操作,选出其正确的操作并按序列出字母:水蒸气蒸馏馏出液加入研细的精食盐使溶液接近饱和,分离出苯胺层→___________ →___________ →___________ →___________ →___________ →h。
a.用块状氢氧化钠(约2 g)干燥b.水层用30 mL乙醚分三次萃取
c.过滤d.冷却结晶
e.合并苯胺与乙醚萃取液f.滤液用热水浴加热蒸馏,接收33~35°C的馏分
g.趁热过滤h.加热蒸馏,接收182~185°C的馏分
上述操作流程中,加入精食盐的目的是___________ 。

已知:a.反应方程式为:4
 +9Fe+4H2O
+9Fe+4H2O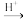 4
4 +3Fe3O4 (剧烈放热)
+3Fe3O4 (剧烈放热)b.苯胺有碱性,与酸溶液反应生成可溶性盐。
c.相关物质物理性质如下:
| 名称 | 颜色状态 | 溶解性 | 沸点(℃) | 密度(g/cm3) |
| 硝基苯 | 无色油状液体(常呈淡黄色) | 难溶于水, 易溶于乙醇、乙醚、苯 | 211 | 1.2 |
| 苯胺 | 无色油状液体 | 微溶于水,易溶于乙醇、乙醚、苯 | 184.4 | 1.02 |
| 乙醚 | 无色透明液体 | 微溶于水,与硝基苯、 苯胺混溶 | 34.6 | 0.71 |
(1)步骤I在250 mL三颈烧瓶中加入40 g铁屑和50 mL水,然后加入2 mL冰醋酸,最后再加硝基苯。硝基苯须缓慢滴加,其原因可能是
(2)步骤II在小火加热下反应回流约1小时。步骤I、II需用到的仪器除三颈烧瓶等之外,还需以下的
A.搅拌器B. 球形冷凝管C.分液漏斗D.恒压滴液漏斗
(3)步骤II,多步操作为:
①反应完全后,冷却,边搅拌边加入氢氧化钠至反应物呈碱性;
②用少量水冲洗冷凝管和搅拌器,洗涤液并入三颈烧瓶中;
③如图组装好水蒸气蒸馏装置,进行水蒸气蒸馏得到苯胺粗产品。(注:水蒸气蒸馏是将水蒸气通入不溶或微溶于水的有机物中,使待提纯的有机物随水蒸气一起被蒸馏出来,从而达到分离提纯的目的。)

下列有关步骤II说法不正确的是
A.操作①,可用甲基橙试液指示氢氧化钠的加入量
B.操作②,用水冲洗冷凝管和搅拌器,目的是除去杂质,以提高产品纯度
C.操作③,水蒸气蒸馏装置中导管C的作用是平衡气压,起到预警的作用
D.操作③,水蒸气蒸馏结束后,应先停止加热,再打开D处活塞,以防倒吸
步骤III提纯产品苯胺时,涉及以下部分操作,选出其正确的操作并按序列出字母:水蒸气蒸馏馏出液加入研细的精食盐使溶液接近饱和,分离出苯胺层→
a.用块状氢氧化钠(约2 g)干燥b.水层用30 mL乙醚分三次萃取
c.过滤d.冷却结晶
e.合并苯胺与乙醚萃取液f.滤液用热水浴加热蒸馏,接收33~35°C的馏分
g.趁热过滤h.加热蒸馏,接收182~185°C的馏分
上述操作流程中,加入精食盐的目的是
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐2】二氧化钛是钛的重要化合物,钛白(纯净的二氧化钛)是一种折射率高、着色力和遮盖力强、化学性质稳定的白色颜料。钛铁矿的主要成分为FeTiO3(可表示为FeO·TiO2),含有Fe2O3、SiO2等杂质,由钛铁矿制取二氧化钛,常用硫酸法,其流程如下:
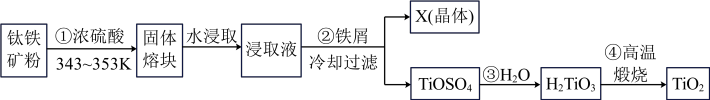
(1)钛铁矿主要成分与浓硫酸反应的主要产物是TiOSO4和FeSO4,该反应的化学方程式为__________________ 。
(2)为提高“固体熔块”水浸取时的浸出率,除了采用循环浸取、延长时间外,适宜的条件还可以选择______________ 。(任写一种均可)
(3)浸取液与铁屑反应的离子方程式为_________ ;从滤液中获得晶体X的基本操作是___________ 、____________ 、过滤、洗涤、干燥。
(4)第③步反应化学方程式______________ 。
(5)取少量H2TiO3,加入盐酸并振荡,滴加KSCN溶液后无明显现象,再加H2O2后出现微红色,说明H2TiO3中存在的杂质离子是____________ 。这种H2TiO3即使用水充分洗涤,煅烧后获得的TiO2也会发黄,发黄的杂质是________ (填化学式)。

(1)钛铁矿主要成分与浓硫酸反应的主要产物是TiOSO4和FeSO4,该反应的化学方程式为
(2)为提高“固体熔块”水浸取时的浸出率,除了采用循环浸取、延长时间外,适宜的条件还可以选择
(3)浸取液与铁屑反应的离子方程式为
(4)第③步反应化学方程式
(5)取少量H2TiO3,加入盐酸并振荡,滴加KSCN溶液后无明显现象,再加H2O2后出现微红色,说明H2TiO3中存在的杂质离子是
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐3】某硫酸工业废渣的主要成分为SiO2、MgO、Al2O3、Fe2O3等。回收废渣中金属元素的工艺流程如下:

已知常温条件下:
①阳离子以氢氧化物形式开始沉淀和恰好完全沉淀(阳离子浓度等于10-5mol·L-1 )时的pH 如下表所
示。
②饱和氨水溶液中c(OH-)约为1×10-3mol·L-1。
请回答下列问题:
(1)固体C为_________ (填化学式)。
(2)上述流程中两次使用试剂X,试剂X是_________ (填“氨水”或“氢氧化钠”),其理由是_________________ 。
(3)溶液D→固体E的过程中需要控制溶液pH=13,如果pH过小,可能导致的后果是________________ 。
(4)写出溶液F→溶液H 的离子方程式:__________________ 。
(5)Ksp[Mg (OH )2]=_____________ 。

已知常温条件下:
①阳离子以氢氧化物形式开始沉淀和恰好完全沉淀(阳离子浓度等于10-5mol·L-1 )时的pH 如下表所
示。
| 阳离子 | Fe3+ | Al3+ | Mg2+ |
| 开始沉淀时的pH | 1.9 | 3.7 | 9.6 |
| 恰好完全沉淀时的pH | 3.2 | 5.2 | 11.0 |
请回答下列问题:
(1)固体C为
(2)上述流程中两次使用试剂X,试剂X是
(3)溶液D→固体E的过程中需要控制溶液pH=13,如果pH过小,可能导致的后果是
(4)写出溶液F→溶液H 的离子方程式:
(5)Ksp[Mg (OH )2]=
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐1】碱式硫酸镁晶须 是一种无机镁盐晶须,将其添加到以橡胶、塑料为基体的复合材料中,能使该复合材料有良好的阻燃功效。一种以蛇纹石(主要含
是一种无机镁盐晶须,将其添加到以橡胶、塑料为基体的复合材料中,能使该复合材料有良好的阻燃功效。一种以蛇纹石(主要含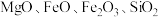 等)为原料制备碱式硫酸镁晶须的流程如图:
等)为原料制备碱式硫酸镁晶须的流程如图:
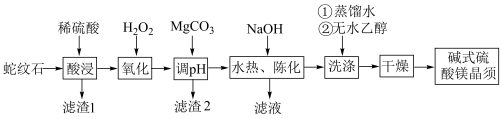
回答下列问题:
(1)酸浸时须将蛇纹石粉碎,其目的是_______ 。
(2)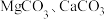 在高温下均易分解,但
在高温下均易分解,但 的分解温度比
的分解温度比 的低,试从结构角度解释其原因:
的低,试从结构角度解释其原因:_______ 。
(3)洗涤步骤中用无水乙醇洗涤的目的是_______ 。
(4)氧化的目的是_______ (用离子方程式表示),为检验溶液中的离子是否完全被氧化,可使用的试剂为_______ (填化学式)。
(5)将碱式硫酸镁晶须 进行热重分析测定其化学式,
进行热重分析测定其化学式,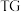 热重曲线[样品的固体残留率(
热重曲线[样品的固体残留率( )随温度变化]
)随温度变化] (微商热重曲线,表示质量的变化速率随温度的变化)如图1所示,第一次失重发生反应的化学方程式为
(微商热重曲线,表示质量的变化速率随温度的变化)如图1所示,第一次失重发生反应的化学方程式为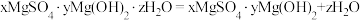 ,第三次失重后获得的晶体的晶胞结构如图2所示。
,第三次失重后获得的晶体的晶胞结构如图2所示。
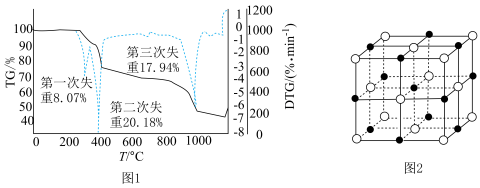
①x、y、z为最简整数比,则碱式硫酸镁晶须的化学式为_______ ;第二次失重发生反应的化学方程式为_______ 。
②图2中的晶胞参数为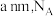 为阿伏加德罗常数的值,则晶胞中白球的配位数为
为阿伏加德罗常数的值,则晶胞中白球的配位数为_______ ,该晶体的密度为_______  。
。
 是一种无机镁盐晶须,将其添加到以橡胶、塑料为基体的复合材料中,能使该复合材料有良好的阻燃功效。一种以蛇纹石(主要含
是一种无机镁盐晶须,将其添加到以橡胶、塑料为基体的复合材料中,能使该复合材料有良好的阻燃功效。一种以蛇纹石(主要含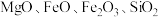 等)为原料制备碱式硫酸镁晶须的流程如图:
等)为原料制备碱式硫酸镁晶须的流程如图:
回答下列问题:
(1)酸浸时须将蛇纹石粉碎,其目的是
(2)
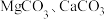 在高温下均易分解,但
在高温下均易分解,但 的分解温度比
的分解温度比 的低,试从结构角度解释其原因:
的低,试从结构角度解释其原因:(3)洗涤步骤中用无水乙醇洗涤的目的是
(4)氧化的目的是
(5)将碱式硫酸镁晶须
 进行热重分析测定其化学式,
进行热重分析测定其化学式,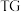 热重曲线[样品的固体残留率(
热重曲线[样品的固体残留率( )随温度变化]
)随温度变化] (微商热重曲线,表示质量的变化速率随温度的变化)如图1所示,第一次失重发生反应的化学方程式为
(微商热重曲线,表示质量的变化速率随温度的变化)如图1所示,第一次失重发生反应的化学方程式为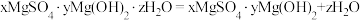 ,第三次失重后获得的晶体的晶胞结构如图2所示。
,第三次失重后获得的晶体的晶胞结构如图2所示。
①x、y、z为最简整数比,则碱式硫酸镁晶须的化学式为
②图2中的晶胞参数为
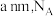 为阿伏加德罗常数的值,则晶胞中白球的配位数为
为阿伏加德罗常数的值,则晶胞中白球的配位数为 。
。
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐2】氮化硼(BN)是一种重要的功能陶瓷材料,有广泛应用。以铁硼矿(主要成分有Mg2B2O5·H2O、Fe3O4,次要成分有Fe2O3、FeO、 CaO、Al2O3、 SiO2) 为原料制备氮化硼的流程如图所示:

已知:相关金属离子[c( Mn+)= 0.1mol ·l-1]形成氢氧化物沉淀的pH范围如下:
回答下列问题:
(1)用稀硫酸酸浸时,若其他条件不变,工业中采取下列措施能提高硼元素浸出率的有_______ (填序号)。
A.适当升高酸浸温度 B.适当加快搅拌速度 C.适当缩短酸浸时间
(2)滤渣1的主要成分为_______ 。
(3)加氨水过程中常常要加热,加热的目的是_______ 。
(4)从硫酸镁溶液中提取MgSO4·7H2O的操作包括_______ 、过滤、 洗涤、干燥。
(5)写出B2O3与氨气在高温下反应制备BN的化学方程式:_______
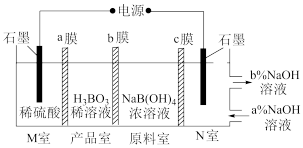
(6)H3BO3 (硼酸)还可以利用电解NaB(OH)4溶液的方法制备,工作原理如图所示,c为_______ (填“阴离子交换膜”或“阳离子交换膜”), 产品室中发生反应的离子方程式为_______ 。

已知:相关金属离子[c( Mn+)= 0.1mol ·l-1]形成氢氧化物沉淀的pH范围如下:
| 金属离子 | Fe3+ | Fe2+ | Al3+ |
| 开始沉淀的pH | 1.5 | 6.3 | 3.2 |
| 沉淀完全的pH | 2.8 | 8.3 | 5.0 |
(1)用稀硫酸酸浸时,若其他条件不变,工业中采取下列措施能提高硼元素浸出率的有
A.适当升高酸浸温度 B.适当加快搅拌速度 C.适当缩短酸浸时间
(2)滤渣1的主要成分为
(3)加氨水过程中常常要加热,加热的目的是
(4)从硫酸镁溶液中提取MgSO4·7H2O的操作包括
(5)写出B2O3与氨气在高温下反应制备BN的化学方程式:
(6)H3BO3 (硼酸)还可以利用电解NaB(OH)4溶液的方法制备,工作原理如图所示,c为

您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐3】工业上用赤铁矿(含Fe2O3、FeO,也含有Al2O3、MnO2、CuO等)制备FeSO4·7H2O(绿矾)的流程如下:

(1)实验室中操作①的名称为____ 。所需的玻璃仪器有烧杯、______ 、_____ 。
(2)氢氧化钠溶液加入赤铁矿中发生反应的离子方程式为_______________________ 。
(3)加入滤渣Ⅰ中的试剂a是___________ ,滤液Ⅱ中的主要金属阳离子有_____ 。
(4)试剂b为__________________ 。
(5)滤渣Ⅲ中的主要成分是____________ 。操作④隔绝空气的目的是___________ 。

(1)实验室中操作①的名称为
(2)氢氧化钠溶液加入赤铁矿中发生反应的离子方程式为
(3)加入滤渣Ⅰ中的试剂a是
(4)试剂b为
(5)滤渣Ⅲ中的主要成分是
您最近一年使用:0次



