【化学-选修3:物质结构与性质】
铁、铜及其化合物在日常生产、生活有着广泛的应用。请回答下列问题:
(1)铁在元素周期表中的位置是___ ,基态铜原子的核外电子排布式为___ 。
(2)配合物Fe(CO)x常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断Fe(CO)x晶体属于_____ (填晶体类型)。
(3)CO和CO的一种生活中常见等电子体分子,两者相比较沸点较高的为___ (填化学式)。CN-中碳原子杂化轨道类型为_______ ,C、N、O三元素的第一电离能最大的为_______ (用元素符号表示)。
(4)铜晶体中铜原子的堆积方式如图1所示。每个铜原子周围距离最近的铜原子数目___ 。
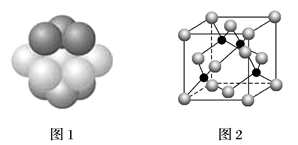
(5)M原子的价电子排布式为3s23p5,铜与M形成化合物的晶胞如图2所示(黑点代表铜原子)。
①该晶体的化学式为___ 。
②已知铜和M的电负性分别为1.9和3.0,则铜与M形成的化合物属于____ (填“离子”、“共价”)化合物。
③已知该晶体的密度为ρg·cm-3,阿伏加德罗常数为NA,已知该晶体中铜原子和M原子之间的最短距离为体对角线的1/4,则该晶体中铜原子和M原子之间的最短距离为____ pm(只写计算式)。
铁、铜及其化合物在日常生产、生活有着广泛的应用。请回答下列问题:
(1)铁在元素周期表中的位置是
(2)配合物Fe(CO)x常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断Fe(CO)x晶体属于
(3)CO和CO的一种生活中常见等电子体分子,两者相比较沸点较高的为
(4)铜晶体中铜原子的堆积方式如图1所示。每个铜原子周围距离最近的铜原子数目

(5)M原子的价电子排布式为3s23p5,铜与M形成化合物的晶胞如图2所示(黑点代表铜原子)。
①该晶体的化学式为
②已知铜和M的电负性分别为1.9和3.0,则铜与M形成的化合物属于
③已知该晶体的密度为ρg·cm-3,阿伏加德罗常数为NA,已知该晶体中铜原子和M原子之间的最短距离为体对角线的1/4,则该晶体中铜原子和M原子之间的最短距离为
更新时间:2016-12-09 17:10:06
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
【推荐1】硫铁化合物( 、
、 等)应用广泛。
等)应用广泛。
(1)纳米 可去除水中微量六价铬
可去除水中微量六价铬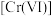 。在
。在 的水溶液中,纳米
的水溶液中,纳米 颗粒表面带正电荷,
颗粒表面带正电荷, 主要以
主要以 、
、 、
、 等形式存在,纳米
等形式存在,纳米 去除水中
去除水中 主要经过“吸附→反应→沉淀”的过程。
主要经过“吸附→反应→沉淀”的过程。
已知: ,
,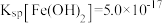 ;
; 电离常数分别为
电离常数分别为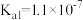 、
、 。
。
①在弱碱性溶液中, 与
与 反应生成
反应生成 、
、 和单质S,其离子方程式为
和单质S,其离子方程式为_______ 。
②在弱酸性溶液中,反应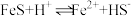 的平衡常数K的数值为
的平衡常数K的数值为_______ 。
③在 溶液中,pH越大,
溶液中,pH越大, 去除水中
去除水中 的速率越慢,原因是
的速率越慢,原因是_______ 。
(2) 具有良好半导体性能。
具有良好半导体性能。 的一种晶体与
的一种晶体与 晶体的结构相似,该
晶体的结构相似,该 晶体的一个晶胞中
晶体的一个晶胞中 的数目为
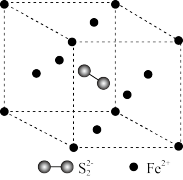
的数目为_______ ,在 晶体中,每个S原子与三个
晶体中,每个S原子与三个 紧邻,且
紧邻,且 间距相等,如图给出了
间距相等,如图给出了 晶胞中的
晶胞中的 和位于晶胞体心的
和位于晶胞体心的 (
( 中的
中的 键位于晶胞体对角线上,晶胞中的其他
键位于晶胞体对角线上,晶胞中的其他 已省略)。如图中用“-”将其中一个S原子与紧邻的
已省略)。如图中用“-”将其中一个S原子与紧邻的 连接起来
连接起来_______ 。
(3) 、
、 在空气中易被氧化,将
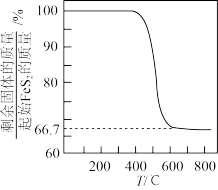
在空气中易被氧化,将 在空气中氧化,测得氧化过程中剩余固体的质量与起始
在空气中氧化,测得氧化过程中剩余固体的质量与起始 的质量的比值随温度变化的曲线如图所示。
的质量的比值随温度变化的曲线如图所示。 时,
时, 氧化成含有两种元素的固体产物为
氧化成含有两种元素的固体产物为_______ (填化学式,写出计算过程)。
 、
、 等)应用广泛。
等)应用广泛。(1)纳米
 可去除水中微量六价铬
可去除水中微量六价铬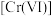 。在
。在 的水溶液中,纳米
的水溶液中,纳米 颗粒表面带正电荷,
颗粒表面带正电荷, 主要以
主要以 、
、 、
、 等形式存在,纳米
等形式存在,纳米 去除水中
去除水中 主要经过“吸附→反应→沉淀”的过程。
主要经过“吸附→反应→沉淀”的过程。已知:
 ,
,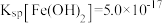 ;
; 电离常数分别为
电离常数分别为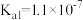 、
、 。
。①在弱碱性溶液中,
 与
与 反应生成
反应生成 、
、 和单质S,其离子方程式为
和单质S,其离子方程式为②在弱酸性溶液中,反应
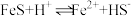 的平衡常数K的数值为
的平衡常数K的数值为③在
 溶液中,pH越大,
溶液中,pH越大, 去除水中
去除水中 的速率越慢,原因是
的速率越慢,原因是(2)
 具有良好半导体性能。
具有良好半导体性能。 的一种晶体与
的一种晶体与 晶体的结构相似,该
晶体的结构相似,该 晶体的一个晶胞中
晶体的一个晶胞中 的数目为
的数目为 晶体中,每个S原子与三个
晶体中,每个S原子与三个 紧邻,且
紧邻,且 间距相等,如图给出了
间距相等,如图给出了 晶胞中的
晶胞中的 和位于晶胞体心的
和位于晶胞体心的 (
( 中的
中的 键位于晶胞体对角线上,晶胞中的其他
键位于晶胞体对角线上,晶胞中的其他 已省略)。如图中用“-”将其中一个S原子与紧邻的
已省略)。如图中用“-”将其中一个S原子与紧邻的 连接起来
连接起来
(3)
 、
、 在空气中易被氧化,将
在空气中易被氧化,将 在空气中氧化,测得氧化过程中剩余固体的质量与起始
在空气中氧化,测得氧化过程中剩余固体的质量与起始 的质量的比值随温度变化的曲线如图所示。
的质量的比值随温度变化的曲线如图所示。 时,
时, 氧化成含有两种元素的固体产物为
氧化成含有两种元素的固体产物为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】黄铜矿(CuFeS2)是炼铜的主要矿物,在野外很容易被误会为黄金,因此被称为愚人金。回答下列问题:
(1)处于激发态的S原子,其中1个3s电子跃迁到3p轨道上,该激发态S原子的核外电子排布式为__ 。同族元素的氢化物中,H2O比H2Te沸点高的原因是__ 。
(2)检验Fe2+的试剂有多种,其中之一是铁氰化钾(K3[Fe(CN)6]),又称赤血盐。
①在配合物K3[Fe(CN)6]中,易提供孤电子对的成键原子是__ (填元素名称),含有12molσ键的K3[Fe(CN)6]的物质的量为__ mol。
②赤血盐中C原子的杂化方式为__ ;C、N、O三种元素第一电离能由大到小的排序为___ ;写出与CN-互为等电子体的一种化合物的化学式__ 。
③Fe、Na、K的晶胞结构相同,但钠的熔点比钾更高,原因是___ 。
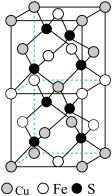
(3)CuFeS2的晶胞结构如图所示。已知:晶胞参数a=0.524nm,c=1.032nm。则CuFeS2的晶胞中每个Cu原子与__ 个S原子相连,晶体密度ρ=__ g·cm-3(列出计算表达式)。
(1)处于激发态的S原子,其中1个3s电子跃迁到3p轨道上,该激发态S原子的核外电子排布式为
(2)检验Fe2+的试剂有多种,其中之一是铁氰化钾(K3[Fe(CN)6]),又称赤血盐。
①在配合物K3[Fe(CN)6]中,易提供孤电子对的成键原子是
②赤血盐中C原子的杂化方式为
③Fe、Na、K的晶胞结构相同,但钠的熔点比钾更高,原因是
(3)CuFeS2的晶胞结构如图所示。已知:晶胞参数a=0.524nm,c=1.032nm。则CuFeS2的晶胞中每个Cu原子与

您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】A、B、C、D、E、F、G七种前四周期元素且原子序数依次增大,A的最高正价和最低负价的绝对值相等,B的基态原子有3个不同的能级且各能级中电子数相等,D的基态原子与B的基态原子的未成对电子数目相同,E的基态原子s能级的电子总数与p能级的电子数相等,F的基态原子的3d轨道电子数是4s电子数的4倍,G2+的3d轨道有9个电子,请回答下列问题:
(1)元素D在周期表中的位置是_____________ 。
(2)G的基态原子电子排布式为_____________ 。
(3)B、C、D原子的第一电离能由小到大的顺序为_____________ (用元素符号回答)
(4)CA3中心原子C的杂化类型是________________ ,分子的立体构型是_____________ 。
(5)向GSO4(aq)中逐滴加入氨水至过量,会观察到_________________ 现象。后一步反应的离子反应方程式为:_____________ 。
(6)某电池放电时的总反应为:Fe+F2O3+3H2O = Fe(OH)2+2F(OH)2(注:F2O3和F(OH)2为上面F元素对应的化合物),写出该电池放电时的正极反应式_____________ 。
(1)元素D在周期表中的位置是
(2)G的基态原子电子排布式为
(3)B、C、D原子的第一电离能由小到大的顺序为
(4)CA3中心原子C的杂化类型是
(5)向GSO4(aq)中逐滴加入氨水至过量,会观察到
(6)某电池放电时的总反应为:Fe+F2O3+3H2O = Fe(OH)2+2F(OH)2(注:F2O3和F(OH)2为上面F元素对应的化合物),写出该电池放电时的正极反应式
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】祖母绿是四大名贵宝石之一,主要成分为Be3Al2Si6O18,含有微量的Cr、Ni、Fe元素而呈现各种颜色。回答下列问题:
(1)基态Ni2+的电子排布式为____ ;宝石中Si的化合价是____ ;基态Al原子电子占据最高能级的电子云轮廓图形状为____ 。
(2)铍与相邻主族的铝元素性质相似。下列有关铍和铝的叙述正确的有____ 。(填字母)
A.都属于p区主族元素 B.电负性都比镁大
C.第一电离能都比镁大 D.氯化物的水溶液pH均小于7
(3)六羰基铬[Cr(CO)6]用于制高纯度铬粉,它的沸点为220℃。
①Cr(CO)6的晶体类型是____ ,1 mol Cr(CO)6含δ键的数目为____ ;
②加热Cr(CO)6可得到高纯度铬粉和CO,反应破坏的作用力类型为____ 。
a.离子键 b.配位键 c.金属键 d.分子间作用力
(4)多数配离子显示颜色与d轨道的分裂能有关。分裂能是指配离子的中心原子(离子)的一个电子从较低能量的d轨道跃迁到较高能量的d轨道所需的能量(用Δ表示),它与中心离子的电子排布结构、电荷、配体有关。试判断分裂能Δ[Fe(H2O)6]3+____ Δ[Fe(H2O)6]2+(填“>”“<”或“=”),理由是_________ 。
(5)①氧化镍晶胞如图甲所示,A的原子坐标参数为:(0,0, ),则底面面心B的原子坐标参数为
),则底面面心B的原子坐标参数为____ 。

②按图乙所示无限拓宽延长,NiO可形成“单层分子”,氧离子和镍离子均看成球体,其半径分别为a pm、b pm,“单层分子”截割出的最小重复结构单元在空间呈长方体,则离子在长方体内的空间利用率为____ (列出计算式即可)。
(1)基态Ni2+的电子排布式为
(2)铍与相邻主族的铝元素性质相似。下列有关铍和铝的叙述正确的有
A.都属于p区主族元素 B.电负性都比镁大
C.第一电离能都比镁大 D.氯化物的水溶液pH均小于7
(3)六羰基铬[Cr(CO)6]用于制高纯度铬粉,它的沸点为220℃。
①Cr(CO)6的晶体类型是
②加热Cr(CO)6可得到高纯度铬粉和CO,反应破坏的作用力类型为
a.离子键 b.配位键 c.金属键 d.分子间作用力
(4)多数配离子显示颜色与d轨道的分裂能有关。分裂能是指配离子的中心原子(离子)的一个电子从较低能量的d轨道跃迁到较高能量的d轨道所需的能量(用Δ表示),它与中心离子的电子排布结构、电荷、配体有关。试判断分裂能Δ[Fe(H2O)6]3+
(5)①氧化镍晶胞如图甲所示,A的原子坐标参数为:(0,0,
 ),则底面面心B的原子坐标参数为
),则底面面心B的原子坐标参数为
②按图乙所示无限拓宽延长,NiO可形成“单层分子”,氧离子和镍离子均看成球体,其半径分别为a pm、b pm,“单层分子”截割出的最小重复结构单元在空间呈长方体,则离子在长方体内的空间利用率为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐2】金属锂及其化合物因独特的性质而具有重要的应用价值。例如:Li是最轻的固体金属,可应用于生产电池:Li2O可用于特种玻璃、陶瓷、医药等领域:LiH、LiBH4、LiNH2为常见的储氢材料等。回答下列问题:
(1)基态Li原子核外有___________ 种运动状态不同的电子。
(2)LiH、LiBH4、LiNH2中所含非金属元素的电负性由小到大的顺序为___________ (用元素符号表示);LiNH2中阴离子的空间构型为___________ 。
(3)锂电池负极材料晶体为Li+嵌入两层石墨层中导致石墨堆积方式发生改变,上下层一样,形成如图所示的晶胞结构。晶胞中锂离子和碳原子的个数之比为___________ ;其中与一个Li+距离最近且相等的C原子数为___________ 。
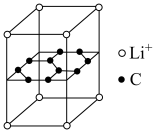
(4)Li3N与H2在一定条件下反应生成LiNH2和LiH,写出该反应的化学方程式:___________ 。该反应还可能得到副产物Li2NH,通过对LiNH2和Li2NH的结构比较,发现两者均为反萤石结构,Li2NH的晶胞结构如图2所示。若Li+的半径为apm,NH2+的半径为bpm,Li2NH的摩尔质量为Mg/mol,NA表示阿伏加德罗常数的值,则Li2NH的密度为___________ g/cm3(用含a、b、M、NA的代数式表示,列出计算式即可)。

(1)基态Li原子核外有
(2)LiH、LiBH4、LiNH2中所含非金属元素的电负性由小到大的顺序为
(3)锂电池负极材料晶体为Li+嵌入两层石墨层中导致石墨堆积方式发生改变,上下层一样,形成如图所示的晶胞结构。晶胞中锂离子和碳原子的个数之比为

(4)Li3N与H2在一定条件下反应生成LiNH2和LiH,写出该反应的化学方程式:

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】Ⅰ.Na、Cu、O、Si、S、Cl是常见的六种元素。
(1)Na位于元素周期表第________ 周期________ 族;S的基态原子核外有________ 个未成对电子;Si的基态原子核外电子排布式为____________________ 。
(2)用“>”或“<”填空:
Ⅱ.下表是元素周期表的一部分,表中所列的字母分别代表一种化学元素。试回答下列问题:
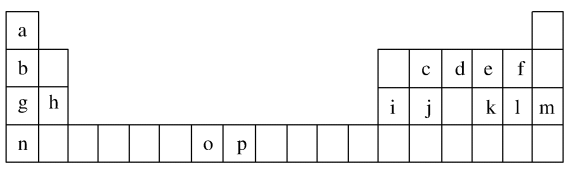
(3)h的单质在空气中燃烧发出耀眼的白光,请用原子结构的知识解释发光的原因:_____ 。
(4)o、p两元素的部分电离能数据列于下表:
比较两元素的I2、I3可知,气态o2+再失去一个电子比气态p2+再失去一个电子难。对此,你的解释是__________________________________________ 。
(5)已知稀有气体熔、沸点均为同周期的最低者,第三周期8种元素按单质熔点由低到高的顺序排列如图甲所示,其中电负性最大的是________ (填图中的序号)。
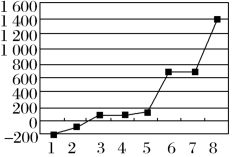
甲
(6)表中所列的某主族元素的电离能情况如图乙所示,则该元素是____________ (填元素符号)。
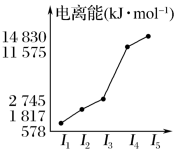
乙
(1)Na位于元素周期表第
(2)用“>”或“<”填空:
| 第一电离能 | 离子半径 | 熔点 | 酸性 |
| Si | O2- | NaCl | H2SO4 |

(3)h的单质在空气中燃烧发出耀眼的白光,请用原子结构的知识解释发光的原因:
(4)o、p两元素的部分电离能数据列于下表:
| 元素 | o | p | |
| 电离能/ (kJ·mol-1) | I1 | 717 | 759 |
| I2 | 1 509 | 1 561 | |
| I3 | 3 248 | 2 957 | |
(5)已知稀有气体熔、沸点均为同周期的最低者,第三周期8种元素按单质熔点由低到高的顺序排列如图甲所示,其中电负性最大的是

甲
(6)表中所列的某主族元素的电离能情况如图乙所示,则该元素是

乙
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】回答下列问题:
(1)三价铬离子能形成多种配位化合物。 中提供电子对形成配位键的原子是
中提供电子对形成配位键的原子是_______ ,中心离子的配位数为_______ 。
(2) 分子中,
分子中, 化学键称为
化学键称为_______ 键,其电子对由_______ 提供。
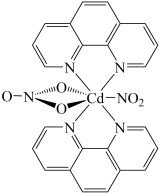
(3)含有多个配位原子的配体与同一中心离子(或原子)通过螯合配位成环而形成的配合物为螯合物。一种 配合物的结构如图所示,
配合物的结构如图所示, 该配合物中通过螯合作用形成的配位键有
该配合物中通过螯合作用形成的配位键有_______ mol,该螯合物中N的杂化方式有_______ 种。
(4)乙二胺 是一种有机化合物,乙二胺能与
是一种有机化合物,乙二胺能与 、
、 等金属离子形成稳定环状离子,其原因是
等金属离子形成稳定环状离子,其原因是_______ ,其中与乙二胺形成的化合物稳定性相对较高的是_______ (填“ ”或“
”或“ ”。
”。
(5) 中的化学键具有明显的共价性,蒸气状态下以双聚分子存在的
中的化学键具有明显的共价性,蒸气状态下以双聚分子存在的 的结构式为
的结构式为_______ ,其中 的配位数为
的配位数为_______ 。
(1)三价铬离子能形成多种配位化合物。
 中提供电子对形成配位键的原子是
中提供电子对形成配位键的原子是(2)
 分子中,
分子中, 化学键称为
化学键称为(3)含有多个配位原子的配体与同一中心离子(或原子)通过螯合配位成环而形成的配合物为螯合物。一种
 配合物的结构如图所示,
配合物的结构如图所示, 该配合物中通过螯合作用形成的配位键有
该配合物中通过螯合作用形成的配位键有
(4)乙二胺
 是一种有机化合物,乙二胺能与
是一种有机化合物,乙二胺能与 、
、 等金属离子形成稳定环状离子,其原因是
等金属离子形成稳定环状离子,其原因是 ”或“
”或“ ”。
”。(5)
 中的化学键具有明显的共价性,蒸气状态下以双聚分子存在的
中的化学键具有明显的共价性,蒸气状态下以双聚分子存在的 的结构式为
的结构式为 的配位数为
的配位数为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】“嫦娥五号”首次实现了我国地外天体采样返回,它的成功发射标志着我国航天事业向前迈出了一大步。“嫦娥五号”的制作材料中包含了Ti、Fe、Ni、C、O等多种元素。回答下列问题:___________ ,与Ni同周期且未成对电子数相同的元素还有___________ 种。
(2)图a为Ni、N、C三种元素构成的一种单元结构,它___________ 晶胞单元(填“是”或“不是”),理由是___________ 。
(3)有机物COF和Ni配合物形成的超分子催化体系的局部结构如图b所示。①、②、③处氮原子的杂化方式分别为___________ ,每个配体与Ni形成___________ 个配位键。
(4)图c为科学家发现的一种只由钛原子和碳原子构成的气态团簇分子,其中位于棱心和体心的原子半径小,这种化合物的化学式为___________ 。
(5)常温下可用Na还原 制备钛单质,已知NaCl的熔点为:801℃,常温下
制备钛单质,已知NaCl的熔点为:801℃,常温下 呈液态,请解释
呈液态,请解释 比NaCl熔点低很多的原因
比NaCl熔点低很多的原因___________ 。
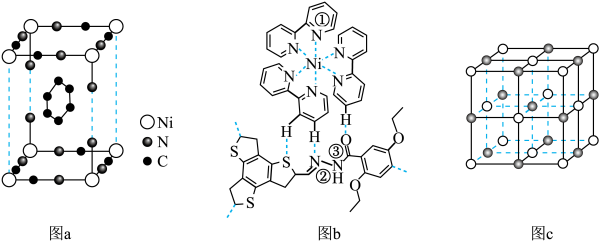
(2)图a为Ni、N、C三种元素构成的一种单元结构,它
(3)有机物COF和Ni配合物形成的超分子催化体系的局部结构如图b所示。①、②、③处氮原子的杂化方式分别为
(4)图c为科学家发现的一种只由钛原子和碳原子构成的气态团簇分子,其中位于棱心和体心的原子半径小,这种化合物的化学式为
(5)常温下可用Na还原
 制备钛单质,已知NaCl的熔点为:801℃,常温下
制备钛单质,已知NaCl的熔点为:801℃,常温下 呈液态,请解释
呈液态,请解释 比NaCl熔点低很多的原因
比NaCl熔点低很多的原因
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐3】三价铬离子( )是葡萄糖耐量因子(GTF)的重要组成成分,GTF能够协助胰岛素发挥作用。构成葡萄糖耐量因子和蛋白质的元素有C、H、O、N、S、Cr等。回答下列问题:
)是葡萄糖耐量因子(GTF)的重要组成成分,GTF能够协助胰岛素发挥作用。构成葡萄糖耐量因子和蛋白质的元素有C、H、O、N、S、Cr等。回答下列问题:
(1)Cr的价层电子排布式为_______ 。
(2)O、N、S的原子半径由大到小的顺序为_______ 。
(3) 分子的 VSEPR模型名称为
分子的 VSEPR模型名称为_______
(4)化学式为 的化合物有多种结构,其中一种可表示为
的化合物有多种结构,其中一种可表示为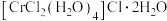 ,该物质的配离子中提供孤电子对的原子为
,该物质的配离子中提供孤电子对的原子为_______ ,配位数为_______ 。
(5)由碳元素形成的某种晶体的晶胞结构如图所示,若阿伏加德罗常数的值为 ,晶体密度为
,晶体密度为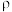
 ,则该晶胞的棱长为
,则该晶胞的棱长为_______ pm。

 )是葡萄糖耐量因子(GTF)的重要组成成分,GTF能够协助胰岛素发挥作用。构成葡萄糖耐量因子和蛋白质的元素有C、H、O、N、S、Cr等。回答下列问题:
)是葡萄糖耐量因子(GTF)的重要组成成分,GTF能够协助胰岛素发挥作用。构成葡萄糖耐量因子和蛋白质的元素有C、H、O、N、S、Cr等。回答下列问题:(1)Cr的价层电子排布式为
(2)O、N、S的原子半径由大到小的顺序为
(3)
 分子的 VSEPR模型名称为
分子的 VSEPR模型名称为(4)化学式为
 的化合物有多种结构,其中一种可表示为
的化合物有多种结构,其中一种可表示为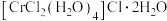 ,该物质的配离子中提供孤电子对的原子为
,该物质的配离子中提供孤电子对的原子为(5)由碳元素形成的某种晶体的晶胞结构如图所示,若阿伏加德罗常数的值为
 ,晶体密度为
,晶体密度为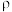
 ,则该晶胞的棱长为
,则该晶胞的棱长为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐1】BaTiO3和MgTiO3都是重要的介电材料,BaTiO3可利用熔融态的反应:TiO2+BaCO3=BaTiO3+CO2↑制备。试回答下列问题:
(1)基态Ti原子中有___________ 个未成对电子,若其价层的某一个电子受激发后得到激发态的Ti原子,该激发态的Ti原子中最多有 ___________ 个未成对电子。
(2)制备BaTiO3的反应的各物质中,电负性最小的元素是___________ (填元素符号)。
(3)BaCO3中阴离子的中心原子的价层电子对数为___________ ,写出一个与该阴离子互为等电子体的分子的化学式___________ 。
(4)TiO2的熔沸点远高于CO2的原因是___________ ,MgTiO3的熔点高于BaTiO3的原因是___________ 。
(5)在BaTiO3的立方晶胞结构中,Ba2+位于晶胞顶点位置,则Ti4+最可能位于___________ ,O2-最可能位于___________ 。将晶胞中部分Ba2+替换为Mg2+或Ca2+可改良材料性能,设晶胞中分别有x、y个Ba2+被替换为Mg2+、Ca2+,则改良后的晶胞化学式为___________ 。
(1)基态Ti原子中有
(2)制备BaTiO3的反应的各物质中,电负性最小的元素是
(3)BaCO3中阴离子的中心原子的价层电子对数为
(4)TiO2的熔沸点远高于CO2的原因是
(5)在BaTiO3的立方晶胞结构中,Ba2+位于晶胞顶点位置,则Ti4+最可能位于
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
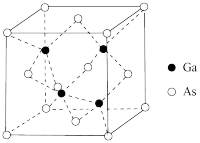
【推荐2】第ⅢA、ⅤA原元素组成的化合物GaN、GaP等是人工合成的新型半导体材料,其晶体结构与单晶硅相似,砷化镓是优良的半导体材料,可用于制作微型激光器或太阳能电池的材料等。
(1)砷化镓的晶胞结构如图所示,则砷化镓的化学式为___ 。
(2)基态As原子的核外电子排布式为___ 。
(3)第一电离能:Ga___ As(选填“>”或“<")。
(4)AsCl3分子的立体构型为___ ,其中As原子轨道的杂化类型为___ 。
(5)在GaN晶体中,每个Ga原子与___ 个N原子相连,在四大晶体类型中,GaN属于___ 晶体。
(6)GaF3的熔点高于1000℃,GaCl3的熔点为77.9℃,其原因是___ 。
(1)砷化镓的晶胞结构如图所示,则砷化镓的化学式为

(2)基态As原子的核外电子排布式为
(3)第一电离能:Ga
(4)AsCl3分子的立体构型为
(5)在GaN晶体中,每个Ga原子与
(6)GaF3的熔点高于1000℃,GaCl3的熔点为77.9℃,其原因是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
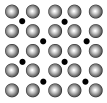
【推荐3】(1)诺贝尔化学奖获得者Gerhard Ertl利用光电子能谱证实:洁净铁(可用于合成氨反应的催化剂)的表面上存在氮原子,图为氮原子在铁的晶面上的单层附着局部示意图(图中小的黑色球代表氮原子,大的灰色球代表铁原子)。则在图示状况下,铁颗粒表面上N/Fe原子数比值的最大值为________________ 。
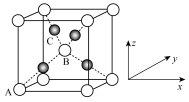
(2)Cu与O形成的某种化合物X,其晶胞结构如下图所示。O在顶点和体心。已知X晶胞中原子坐标参数:A为(0,0,0),B为( ,
, ,
, ),则C原子的坐标参数为
),则C原子的坐标参数为___________ 。
物质结构用到多种模型,请结合模型完成下列问题:
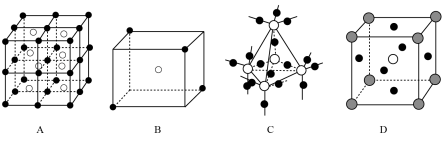
(3)D图是CaTiO3晶胞模型,同一种微粒位置相同,Ca2+位于立方体的体心,则Ti4+位于____ (填顶点或面心)
(4)已知A图是CsCl晶胞模型,体心为Cs+,与其紧邻等距离的Cs+数目有___________ 个。
(5)某分子中原子空间位置关系如B图所示,X位于立方体的顶点,Y位于立方体中心,用X,Y表示的化学式为______________ 。
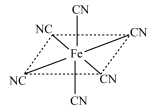
(6)铁元素应用广泛,Fe2+与KCN溶液反应得Fe(CN)2沉淀,当加入过量KCN溶液时沉淀溶解,生成黄血盐,其阴离子结构如图。写出上述沉淀溶解过程的离子方程式为___________________ 。

(2)Cu与O形成的某种化合物X,其晶胞结构如下图所示。O在顶点和体心。已知X晶胞中原子坐标参数:A为(0,0,0),B为(
 ,
, ,
, ),则C原子的坐标参数为
),则C原子的坐标参数为
物质结构用到多种模型,请结合模型完成下列问题:

(3)D图是CaTiO3晶胞模型,同一种微粒位置相同,Ca2+位于立方体的体心,则Ti4+位于
(4)已知A图是CsCl晶胞模型,体心为Cs+,与其紧邻等距离的Cs+数目有
(5)某分子中原子空间位置关系如B图所示,X位于立方体的顶点,Y位于立方体中心,用X,Y表示的化学式为
(6)铁元素应用广泛,Fe2+与KCN溶液反应得Fe(CN)2沉淀,当加入过量KCN溶液时沉淀溶解,生成黄血盐,其阴离子结构如图。写出上述沉淀溶解过程的离子方程式为

您最近一年使用:0次



