关于下列氧化还原反应的说法正确的是( )
| A.在氧化还原反应2H2S+SO2 ═ 3S↓+2H2O中,氧化产物和还原产物的物质的量之比为1:1 |
| B.在氧化还原反应3S+6KOH ═ 2K2S+K2SO3+3H2O中,被氧化和被还原的硫元素质量之比为2:1 |
| C.在氧化还原反应2KMnO4+16HCl(浓)═ 2KCl+2MnCl2+5Cl2↑+8H2O中,氧化剂和还原剂物质的量之比为1:8 |
| D.在氧化还原反应5NH4NO3 ═ 4N2↑+2HNO3+9H2O中,反应中发生氧化反应和发生还原反应的氮原子物质的量之比为5:3 |
更新时间:2017-04-13 20:26:37
|
相似题推荐
单选题
|
较难
(0.4)
解题方法
【推荐1】氮及其化合物在工业生产与生活中应用广泛。合成NH3实现了氮的人工固定,NH3在强碱条件下能被NaClO氧化生成N2H4,N2H4可被NaClO继续氧化生成N2,也可被HNO2氧化生成HN3,HN3是一种弱酸,酸性与醋酸相当。下列有关含氮化合物的性质与制备说法不正确 的是
| A.分析结构可推得,N2H4可溶于水 |
| B.N2H4被NaClO氧化生成N2时,还原剂与氧化剂物质的量之比为1:2 |
| C.制备N2H4时应将NH3缓慢通入NaClO溶液中 |
| D.相同条件下溶液的碱性:NaHCO3强于NaN3 |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】在一定温度和催化剂作用下,NO跟NH3可以发生反应生成N2和H2O。现有NO和NH3的混合物1mol,充分反应后所得产物中,经还原得到的N2比经氧化得到的N2多1.4g。已知反应的化学方程式:4NH3+6NO 5N2+6H2O,则下列说法正确的是
5N2+6H2O,则下列说法正确的是
 5N2+6H2O,则下列说法正确的是
5N2+6H2O,则下列说法正确的是| A.当转移的电子数约为3.612×1023时,则标况下有4.48L氨气被还原 |
| B.氧化产物和还原产物的物质的量比为3:2 |
| C.若以上反应进行完全,原混合物中NO与NH3的物质的量之比为可能为3:7 |
| D.若有混合物中有0.2molNH3,则参与反应的NO为0.8mol |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】如图所示,两圆圈相交的阴影部分表示圆圈内物质相互发生的反应。钠及其氧化物的物质的量 均为0.1 mol,水的质量为100 g。下列说法正确的是
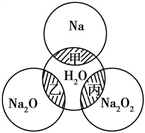

| A.甲、乙、丙都属于氧化还原反应 |
B.甲反应的离子方程式为Na+2H2O Na++2OH-+H2↑ Na++2OH-+H2↑ |
| C.丙充分反应,能产生0.05 mol O2,转移电子0.1 mol |
| D.甲、乙、丙充分反应后所得溶液的质量分数分别为w1、w2、w3,则2w1=w2=w3 |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】对于反应:KClO3 + 6HCl → KCl +3Cl2↑ + 3H2O,若有0.1molKClO3参加反应,下列说法正确的是
| A.被氧化的HCl为0.6mol |
| B.转移电子1.806×1023个 |
| C.产生气体为6.72L |
| D.还原剂占参加反应HCl的5/6 |
您最近半年使用:0次
【推荐3】向FeI2,FeBr2的混合溶液中通入适量氯气,溶液中某些离子的物质的量变化如图所示。已知:2Fe2++Br2===2Fe3++2Br-,2Fe3++2I-===2Fe2++I2。则下列有关说法中,不正确的是。
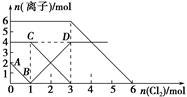

| A.线段BD表示Fe3+物质的量的变化 |
| B.原混合溶液中FeI2的物质的量为1mol |
| C.当通入2 mol Cl2时,溶液中已发生的离子反应可表示为2Fe2++2I-+2Cl2===2Fe3++I2+4Cl- |
| D.原溶液中:n(Fe2+)∶n(I-)∶n(Br-)=2∶3∶1 |
您最近半年使用:0次



