下表是元素周期表的一部分:
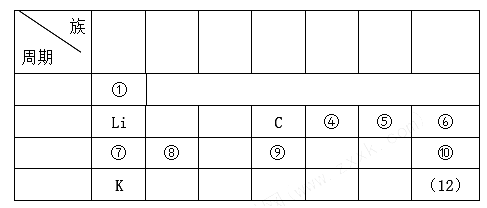
(1)表中元素______ 的非金属性最强(填写元素符号,下同);元素______ 的单质室温下呈液态,它的原子序数是_________ 。
(2)表中元素⑤和⑦、①和⑤均可以组成原子比例为1:1的物质,这两种物质内所含有相同的化学键是__________ (填写“离子键”、“极性共价键”或“非极性共价键”)。
(3)表中元素⑥⑩(12)氢化物的稳定性由大到小的顺序为:_________ (填写化学式,下同)。
(4)表中有一种元素的单质可作为半导体材料,它在元素周期表中的位置是_____ 。
(5)用电子式表示表中⑧⑩两元素形成化合物的过程__________________ 。

(1)表中元素
(2)表中元素⑤和⑦、①和⑤均可以组成原子比例为1:1的物质,这两种物质内所含有相同的化学键是
(3)表中元素⑥⑩(12)氢化物的稳定性由大到小的顺序为:
(4)表中有一种元素的单质可作为半导体材料,它在元素周期表中的位置是
(5)用电子式表示表中⑧⑩两元素形成化合物的过程
更新时间:2017-06-14 20:10:10
|
相似题推荐
解答题-无机推断题
|
较难
(0.4)
【推荐1】填写空格。
(1)写出下列物质的电子式:
_______ ,
_______ :
(2)写出下列物质的结构式:
_______ :
_______ 。
(3)与 原子电子层结构相同的
原子电子层结构相同的 价阴离子的离子结构示意图
价阴离子的离子结构示意图_______ 。
(4)在1~18号元素组成的化合物中具有三核10个电子的共价化合物是_______ :具有三核20个电子的离子化合物是_______ :具有四核18个电子的两种化合物分别是_______ 、_______ :既具有离子键又有非极性键和极性键的化合物是_______ 。
(5)下列叙述中所涉及元素是氧元素的有_______
a.质量数为18,原子核中有10个中子核素
b.核电荷数等于最外层电子数的离子
c.质子数等于短周期同族元素原子序数一半的元素
d.原子的最外层电子数是内层电子数3倍的元素
e.能与H、C、N、 、S、
、S、 等元素形成两种或两种以上的化合物的元素
等元素形成两种或两种以上的化合物的元素
f.形成化合物的种类最多的元素
g.Y和Z均由元素R组成,反应 ,其中的R元素
,其中的R元素
(1)写出下列物质的电子式:


(2)写出下列物质的结构式:


(3)与
 原子电子层结构相同的
原子电子层结构相同的 价阴离子的离子结构示意图
价阴离子的离子结构示意图(4)在1~18号元素组成的化合物中具有三核10个电子的共价化合物是
(5)下列叙述中所涉及元素是氧元素的有
a.质量数为18,原子核中有10个中子核素
b.核电荷数等于最外层电子数的离子
c.质子数等于短周期同族元素原子序数一半的元素
d.原子的最外层电子数是内层电子数3倍的元素
e.能与H、C、N、
 、S、
、S、 等元素形成两种或两种以上的化合物的元素
等元素形成两种或两种以上的化合物的元素f.形成化合物的种类最多的元素
g.Y和Z均由元素R组成,反应
 ,其中的R元素
,其中的R元素
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐2】氮和碳一样也存在一系列氢化物,如NH3、N2H4、N3H5、N4H6等。
请回答下列问题
(1)上述氮的系列氢化物的通式为______________ ;N3H5的电子式为_____________________ 。
(2)已知:①4NH3(g)+5O2(g)==4NO(g)+6H2O(g) △H1= a kJ·mol-1 K1
②4NH3(g)+3O2(g)==2N2(g)+6H2O(g) △H2= b kJ·mol-1 K2
写出N2 与O2反应生成1mol NO气体的热化学方程式:________________________________ ;该反应式的平衡常数表达式K=__________________ (用含有K1、K2的代数式表示)。
(3)已知NH3·H2O为一元弱碱,N2H4·H2O 为二元弱碱,N2H4·H2O在水溶液中的一级电离方程式为N2H4·H2O+H2O N2H5·H2O++ OH-,则可溶性盐盐酸肼(N2H6Cl2)
N2H5·H2O++ OH-,则可溶性盐盐酸肼(N2H6Cl2)
第一步水解的离子方程式为_________________________________________________ ;溶液中离子浓度由大到小的顺序为________________________________________________ 。
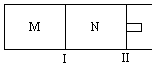
(4)如图所示,隔板I固定不动,活塞II可自由移动,M、N 两个容器中均发生反应:N2(g)+ 3H2(g) 2NH3(g)。向M、N 中均通入lmol N2 和2.3 mol H2。初始时M、N 容积相同,并保持温度不变,则达到平衡时H2 的转化率aM(H2)
2NH3(g)。向M、N 中均通入lmol N2 和2.3 mol H2。初始时M、N 容积相同,并保持温度不变,则达到平衡时H2 的转化率aM(H2)_____ aN(H2)(填“>”“=”“或”)。达到平衡时测得容器N 的容积为2.0 L,其中含有0.2 mol NH3,则此条件下该反应的平衡常数K=______________ 。
请回答下列问题
(1)上述氮的系列氢化物的通式为
(2)已知:①4NH3(g)+5O2(g)==4NO(g)+6H2O(g) △H1= a kJ·mol-1 K1
②4NH3(g)+3O2(g)==2N2(g)+6H2O(g) △H2= b kJ·mol-1 K2
写出N2 与O2反应生成1mol NO气体的热化学方程式:
(3)已知NH3·H2O为一元弱碱,N2H4·H2O 为二元弱碱,N2H4·H2O在水溶液中的一级电离方程式为N2H4·H2O+H2O
 N2H5·H2O++ OH-,则可溶性盐盐酸肼(N2H6Cl2)
N2H5·H2O++ OH-,则可溶性盐盐酸肼(N2H6Cl2)第一步水解的离子方程式为
(4)如图所示,隔板I固定不动,活塞II可自由移动,M、N 两个容器中均发生反应:N2(g)+ 3H2(g)
 2NH3(g)。向M、N 中均通入lmol N2 和2.3 mol H2。初始时M、N 容积相同,并保持温度不变,则达到平衡时H2 的转化率aM(H2)
2NH3(g)。向M、N 中均通入lmol N2 和2.3 mol H2。初始时M、N 容积相同,并保持温度不变,则达到平衡时H2 的转化率aM(H2)
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
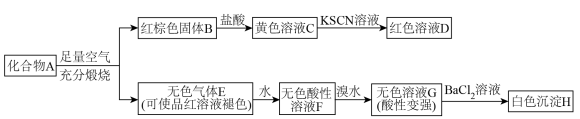
【推荐3】A是由两种元素组成的化合物,具有磁性,某研究小组按如图流程探究其组成:
回答下列问题:
(1)组成A的两种元素分别为_______ 、_____ (填元素符号);实验室中煅烧A时,盛装A的仪器名称为_____________ 。
(2)A可被氢气还原为金属单质,同时生成—种气态氢化物X,X的密度是相同条件下氢气密度的17倍,X的电子式为_______________ 。
(3)若将无色气体E通入黄色溶液C中,溶液最终变成浅绿色,反应的离子方程式为________________ ;
无色酸性溶液F和溴水反应的化学方程式为_____________ 。
(4)取无色溶液G与过量BaCl2溶液反应后上层清液于另一支试管中,滴加H2O2溶液,若产生白色沉淀,说明G溶液中含有____________ (填化学式)。
(5)称取5.920g A在空气中充分煅烧,生成4.800g红棕色固体B,可计算推知A的化学式为____________ ;A能与稀硫酸反应,生成一种淡黄色不溶物和气态氢化物X,反应的离子方程式为________________ 。

回答下列问题:
(1)组成A的两种元素分别为
(2)A可被氢气还原为金属单质,同时生成—种气态氢化物X,X的密度是相同条件下氢气密度的17倍,X的电子式为
(3)若将无色气体E通入黄色溶液C中,溶液最终变成浅绿色,反应的离子方程式为
无色酸性溶液F和溴水反应的化学方程式为
(4)取无色溶液G与过量BaCl2溶液反应后上层清液于另一支试管中,滴加H2O2溶液,若产生白色沉淀,说明G溶液中含有
(5)称取5.920g A在空气中充分煅烧,生成4.800g红棕色固体B,可计算推知A的化学式为
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐1】如图是元素周期表中的前四周期,①~⑨为相应的元素,请从中选择合适的元素回答问题:
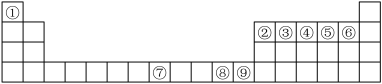
(1)根据元素原子的外围电子排布特征,元素周期表可划分为五个区域,⑨元素位于周期表的________ 区。
(2)④、⑥两元素形成的化合物的立体构型为________ ,其中心原子的杂化轨道类型为________ 。
(3)元素⑧的离子的氢氧化物不溶于水,但可溶于氨水中,该离子与NH3间结合的作用力为________ 。
(4)在周期表给出的9种元素中,电负性最大的元素基态原子的电子排布式为___________ 。
(5)在①与④形成的相对分子质量最小的化合物A中,元素④的杂化类型是____ ,写出与化合物A互为等电子体的一种阳离子______ (填离子符号)。
(6)关于元素①与元素⑤形成的1︰1的化合物,下列说法正确的是______ (填字母序号)。
A.该化合物中的所有原子都满足最外层8电子稳定结构
B.该化合物分子中σ键和π键数目比为1︰1
C.该化合物是由极性键和非极性键形成的极性分子
D.该化合物分子的空间构型为直线形
(7)元素⑦与CO可形成X(CO)5型化合物,该化合物常温下呈液态,熔点为-20.5 ℃,沸点为103 ℃,易溶于非极性溶剂,据此可判断该化合物晶体属于________ 晶体(填晶体类型),化合物中⑦的化合价为:_______ 。根据等电子体理论,该化合物的配体的结构式为:_______ ,CaC2中,阴离子的电子式为: ____________________ 。

(1)根据元素原子的外围电子排布特征,元素周期表可划分为五个区域,⑨元素位于周期表的
(2)④、⑥两元素形成的化合物的立体构型为
(3)元素⑧的离子的氢氧化物不溶于水,但可溶于氨水中,该离子与NH3间结合的作用力为
(4)在周期表给出的9种元素中,电负性最大的元素基态原子的电子排布式为
(5)在①与④形成的相对分子质量最小的化合物A中,元素④的杂化类型是
(6)关于元素①与元素⑤形成的1︰1的化合物,下列说法正确的是
A.该化合物中的所有原子都满足最外层8电子稳定结构
B.该化合物分子中σ键和π键数目比为1︰1
C.该化合物是由极性键和非极性键形成的极性分子
D.该化合物分子的空间构型为直线形
(7)元素⑦与CO可形成X(CO)5型化合物,该化合物常温下呈液态,熔点为-20.5 ℃,沸点为103 ℃,易溶于非极性溶剂,据此可判断该化合物晶体属于
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
【推荐2】如表为元素周期表的一部分,用化学用语回答下列问题:
(1)⑧的原子结构示意图为________ 。
(2)③⑧⑩的最高价氧化物对应的水化物,酸性最强的是________ (填化学式)。
(3)③的气态氢化物与③的最高价氧化物对应的水化物反应生成的盐是________ (填化学式)。
(4)①④⑩三种元素的原子能形成原子数目比为1:1:1的共价化合物,它的电子式为________ 。②④两种元素形成的原子数目比为1:2的共价化合物的结构式为________ 。
(5)⑤的最高价氧化物的水化物与⑦的最高价氧化物反应的离子方程式为________ 。
主族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA |
| 一 | ① | ||||||
| 二 | ② | ③ | ④ | ||||
| 三 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
(1)⑧的原子结构示意图为
(2)③⑧⑩的最高价氧化物对应的水化物,酸性最强的是
(3)③的气态氢化物与③的最高价氧化物对应的水化物反应生成的盐是
(4)①④⑩三种元素的原子能形成原子数目比为1:1:1的共价化合物,它的电子式为
(5)⑤的最高价氧化物的水化物与⑦的最高价氧化物反应的离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
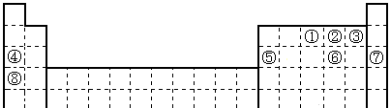
【推荐3】元素①~⑧在元素周期表中的位置如下,回答有关问题:
(1)某元素是①~⑧外的元素,其最外层电子数是次外层电子数的 ,在地壳中含量仅次于氧元素,则该元素在周期表的位置
,在地壳中含量仅次于氧元素,则该元素在周期表的位置_______________ ;
(2)元素①~⑧化学性质最稳定的元素是________ (填数字), 写出该元素含有22个中子的核素的化学符号________
(3)在②、③、④、⑤四种元素中,其离子半径按由大到小的排列顺序为_______________ (用化学式表示,下同),②③⑥元素氢化物的稳定性最强的是________ (填化学式)。
(4)比较④_________ ⑧的金属性(填“>”或“<”),能说明这一结论的依据有________
A.单质的熔点大小 B.最高价氧化物水化物的碱性强弱
C.单质的密度大小 D.单质与水反应的剧烈程度
(5)能体现②⑥元素非金属性强弱的化学方程式_______________________________ 。
(1)某元素是①~⑧外的元素,其最外层电子数是次外层电子数的
 ,在地壳中含量仅次于氧元素,则该元素在周期表的位置
,在地壳中含量仅次于氧元素,则该元素在周期表的位置(2)元素①~⑧化学性质最稳定的元素是
(3)在②、③、④、⑤四种元素中,其离子半径按由大到小的排列顺序为
(4)比较④
A.单质的熔点大小 B.最高价氧化物水化物的碱性强弱
C.单质的密度大小 D.单质与水反应的剧烈程度
(5)能体现②⑥元素非金属性强弱的化学方程式
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
【推荐1】几种短周期元素的原子半径及化合价见下表:
分析上表中有关数据,结合已学过的知识,回答以下问题。
涉及上述元素的答案,请用元素符号表示。
(1)E元素在周期表中的位置是___________ 。
(2)A、H、J对应的离子半径由大到小的顺序是(填写离子符号)____________ 。
(3)用电子式表示A与I所形成化合物的形成过程__________________ 。
(4)B与H所形成的化合物与J的最高价氧化物的水化物X的溶液发生反应的离子方程式为__________________ ;
(5)用B与D所形成的化合物的化学式为__________________ ,属于___________ 晶体。
元素代号 | A | B | D | E | G | H | I | J |
化合价 | -1 | -2 | +4、-4 | +6、-2 | +5、-3 | +3 | +2 | +1 |
原子半径/nm | 0.071 | 0.074 | 0.130 | 0.102 | 0.110 | 0.143 | 0.160 | 0.186 |
涉及上述元素的答案,请用元素符号表示。
(1)E元素在周期表中的位置是
(2)A、H、J对应的离子半径由大到小的顺序是(填写离子符号)
(3)用电子式表示A与I所形成化合物的形成过程
(4)B与H所形成的化合物与J的最高价氧化物的水化物X的溶液发生反应的离子方程式为
(5)用B与D所形成的化合物的化学式为
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
【推荐2】有A、B、C、D、E、F、G7种元素,试按下述所给的条件推断:
①A、B、C是同一周期的金属元素,已知原子核外均有3个电子层,A的原子半径在所属周期中最大且原子半径A>B>C;
②D、E是非金属元素,它们跟氢化合可生成气态氢化物HD和HE,在室温时,D的单质是液体,E的单质是固体;
③F的单质在常温下是气体,性质很稳定,是除氢外最轻的气体;
④G是除氢外原子半径最小的主族元素
(1)A的名称是____ ,B位于周期表中第____ 周期____ 族,C的原子结构示意图是________________ 。
(2)E的单质颜色是_______ 。
(3)A元素与D元素形成的化合物的电子式是_________ 。
(4)G的单质与水反应的化学方程式是________ 。
(5)F的元素符号是__________ 。
(6)在上述七种元素中,最高价氧化物对应的水化物碱性最强的是_____ (填化学式,下同),酸性最强的是_______ ,气态氢化物最稳定的是__________ 。
(7)将C的氧化物对应的水化物投入到A的氧化物对应的水化物中反应的离子方程式是_______________ 。
①A、B、C是同一周期的金属元素,已知原子核外均有3个电子层,A的原子半径在所属周期中最大且原子半径A>B>C;
②D、E是非金属元素,它们跟氢化合可生成气态氢化物HD和HE,在室温时,D的单质是液体,E的单质是固体;
③F的单质在常温下是气体,性质很稳定,是除氢外最轻的气体;
④G是除氢外原子半径最小的主族元素
(1)A的名称是
(2)E的单质颜色是
(3)A元素与D元素形成的化合物的电子式是
(4)G的单质与水反应的化学方程式是
(5)F的元素符号是
(6)在上述七种元素中,最高价氧化物对应的水化物碱性最强的是
(7)将C的氧化物对应的水化物投入到A的氧化物对应的水化物中反应的离子方程式是
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐3】下表为元素周期表的一部分,请参照元素①-⑧在表中的位置,用化学用语 回答下列问题:
(1)④、⑤、⑥的原子半径由大到小的顺序为______ 。③、④、⑤、⑥简单离子半径由小到大的顺序为______ 。
(2)②、⑧、⑦的最高价含氧酸的酸性由强到弱的顺序是______ 。
(3)①、④、⑤、⑧中的某些元素可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的电子式:______ 。
(4)由表中两种元素的原子按1:1组成的常见液态化合物易被催化分解,可使用的催化剂为__________ 。
a.MnO2 b.FeCl3 c.CuSO4 d.KMnO4
(5)由表中元素形成的常见物质X、Y、Z、M、N可发生以下反应:
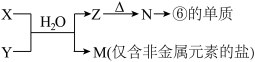
a) X溶液与Y溶液反应的离子方程式为_________ ,
b) N→⑥的单质的化学方程式为________________ 。
族 周期 | IA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
(1)④、⑤、⑥的原子半径由大到小的顺序为
(2)②、⑧、⑦的最高价含氧酸的酸性由强到弱的顺序是
(3)①、④、⑤、⑧中的某些元素可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的电子式:
(4)由表中两种元素的原子按1:1组成的常见液态化合物易被催化分解,可使用的催化剂为
a.MnO2 b.FeCl3 c.CuSO4 d.KMnO4
(5)由表中元素形成的常见物质X、Y、Z、M、N可发生以下反应:

a) X溶液与Y溶液反应的离子方程式为
b) N→⑥的单质的化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐1】五种短周期元素A、B、C、D、E,原子序数依次增大,其中A、B同周期,且A、B原子核外均有两个未成对电子;A、D同主族,B、E同主族,且C的最外层电子比E的最外层电子少5个。根据以上信息,完成下列各题。
(1)写出下列化学用语:A:_____ B:_____ C:_____ D:_______ E:_______
(2)A的最高价氧化物的熔点_________ D的最高价氧化物的熔点(填“>”或“<”),原因是_______________________ ;B氢化物的沸点______ E氢化物的沸点(填“>”或“<”),原因是______________ 。
(3)选取上述五种元素,完成下列问题
①构成的原子晶体有___________________ ;
②含有非极性键的离子化合物__________________ (用电子式表示)
③含有极性键的非极性分子_______________ (用电子式表示)
(1)写出下列化学用语:A:
(2)A的最高价氧化物的熔点
(3)选取上述五种元素,完成下列问题
①构成的原子晶体有
②含有非极性键的离子化合物
③含有极性键的非极性分子
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐2】硫及其化合物有许多用途,相关物质的物理常数如下表所示:

回答下列问题:
(1)基态S原子电子占据最高能级的电子云轮廓图为__________ 形。
(2)图(a)为S8的结构,其熔点和沸点要比二氧化硫的熔点和沸点高很多,主要原因为________ 。
(3)气态三氧化硫以单分子形式存在,其分子的立体构型为__________ 形,其中共价键的类型有__________ 种;固体三氧化硫中存在如图(b)所示的三聚分子,该分子中S原子的杂化轨道类型为__________ 。
(4)根据价层电子对互斥理论,H2S、SO2、SO3的气态分子中,中心原子价层电子对数不同于其他分子的是__________ 。
(5)FeS2晶体的晶胞如图(c)所示。晶胞边长为a nm、FeS2相对式量为M,阿伏加 德罗常数的值为NA,其晶体密度的计算表达式为____________ g/cm3;晶胞中Fe2+位于 所形成的正八面体的体心,该正八面体的边长为
所形成的正八面体的体心,该正八面体的边长为__________ nm。
晶胞有两个基本要素:
(6)晶胞的一个基本要素:原子坐标参数,表示晶胞内部各原子的相对位置,下图为Ge单晶的晶胞,其中原子坐标参数A为(0,0,0);B为( ,0,
,0, );C为(
);C为( ,
, ,0)。则D原子的坐标参数为
,0)。则D原子的坐标参数为__________ 。

| H2S | S8 | FeS2 | SO2 | SO3 | H2SO4 | |
| 熔点/℃ | -85.5 | 115.2 | >600(分解) | -75.5 | 16.8 | 10.3 |
| 沸点/℃ | -60.3 | 444.6 | -10.0 | 45.0 | 337.0 |

回答下列问题:
(1)基态S原子电子占据最高能级的电子云轮廓图为
(2)图(a)为S8的结构,其熔点和沸点要比二氧化硫的熔点和沸点高很多,主要原因为
(3)气态三氧化硫以单分子形式存在,其分子的立体构型为
(4)根据价层电子对互斥理论,H2S、SO2、SO3的气态分子中,中心原子价层电子对数不同于其他分子的是
(5)FeS2晶体的晶胞如图(c)所示。晶胞边长为a nm、FeS2相对式量为M,阿伏加 德罗常数的值为NA,其晶体密度的计算表达式为
 所形成的正八面体的体心,该正八面体的边长为
所形成的正八面体的体心,该正八面体的边长为晶胞有两个基本要素:
(6)晶胞的一个基本要素:原子坐标参数,表示晶胞内部各原子的相对位置,下图为Ge单晶的晶胞,其中原子坐标参数A为(0,0,0);B为(
 ,0,
,0, );C为(
);C为( ,
, ,0)。则D原子的坐标参数为
,0)。则D原子的坐标参数为
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
【推荐3】某强酸性溶液X中可能含有Fe2+、Fe3+、Al3+、Ba2+、NH4+、CO32-、NO3-、SO42-、SiO32-中的若干种,现取X溶液进行连续实验,实验过程及产物如图所示。实验过程中有一种气体为红棕色。
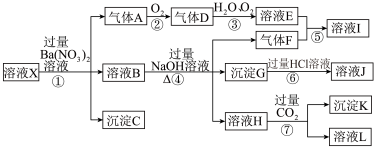
根据以上信息,回答下列问题:
(1)由强酸性条件即可判断X溶液中肯定不存在的离子有________
(2)溶液X中关于硝酸根离子的判断,正确的是______ (填编号,下同)。
a.一定含有 b.一定不含有 c.可能含有
(3)化合物I中含有的化学键类型有____________
(4)转化⑦的离子方程式为____________
(5)对不能确定是否存在的离子,可以另取X溶液,加入下列溶液中的一种,根据现象即可判断,该试剂最好是________ 。
①NaOH溶液 ②KSCN溶液 ③氯水和KSCN的混合溶液 ④pH试纸 ⑤KMnO4溶液

根据以上信息,回答下列问题:
(1)由强酸性条件即可判断X溶液中肯定不存在的离子有
(2)溶液X中关于硝酸根离子的判断,正确的是
a.一定含有 b.一定不含有 c.可能含有
(3)化合物I中含有的化学键类型有
(4)转化⑦的离子方程式为
(5)对不能确定是否存在的离子,可以另取X溶液,加入下列溶液中的一种,根据现象即可判断,该试剂最好是
①NaOH溶液 ②KSCN溶液 ③氯水和KSCN的混合溶液 ④pH试纸 ⑤KMnO4溶液
您最近一年使用:0次



