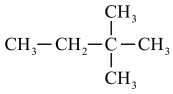
足量锌与浓H2SO4充分在加热下反应生成会SO2和H2的混合气体;锌和稀硫酸反应只有H2生成。现有甲乙两研究小组分别实验探究:
(1)甲研究小组按下图实验验证锌与浓硫酸反应生成物中SO2和H2,取少量的Zn置于b中,向a中加入100mL18.5mol·L-1的浓硫酸,经过一段时间反应,Zn完全溶解
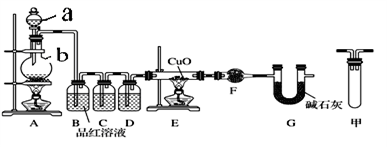
①填写仪器名称:a_____________ 、b_________ 。
②写出装置A中生成能使品红溶液褪色的化学反应方程式:_________________ 。
③装置D中加入的试剂是__________ 。
④U形管G的作用为______________ 。
⑤有同学认为A、B间应增加图中的甲装置,该装置的作用为__________ 。
⑥证明反应生成SO2和H2的实验现象是_________________ 。
⑦若A中生成标准状况下的气体33.6L,将A反应后的溶液稀释到1L,测得溶液中H+的浓度为0.1 mol·L-1,则稀释液中SO42-的物质的量浓度是_________ mol·L-1。
(2)乙研究小组为了探究锌与稀硫酸反应过程中的速率及能量的变化,进行以下实验,分析影响反应速率的因素。

实验时,从断开K开始 ,每间隔1分钟,交替断开或闭合K,并连续计数每1 分钟内从a管流出的水滴数,得到的水滴数如下表所示:
分析反应过程中的水滴数,请回答:
① 由水滴数58>34、81>59,说明在反应初期,闭合K时比断开K时的反应速率快,主要原因是形成原电池反应速度快。
② 由水滴数102>78,说明在反应后期,断开K时的反应速率快于闭合K时的反应速率,主要原因是_____________________________________ 。
③ 从能量转换形式不同的角度,分析水滴数86>81、117>112的主要原因是:_______ 。
(1)甲研究小组按下图实验验证锌与浓硫酸反应生成物中SO2和H2,取少量的Zn置于b中,向a中加入100mL18.5mol·L-1的浓硫酸,经过一段时间反应,Zn完全溶解

①填写仪器名称:a
②写出装置A中生成能使品红溶液褪色的化学反应方程式:
③装置D中加入的试剂是
④U形管G的作用为
⑤有同学认为A、B间应增加图中的甲装置,该装置的作用为
⑥证明反应生成SO2和H2的实验现象是
⑦若A中生成标准状况下的气体33.6L,将A反应后的溶液稀释到1L,测得溶液中H+的浓度为0.1 mol·L-1,则稀释液中SO42-的物质的量浓度是
(2)乙研究小组为了探究锌与稀硫酸反应过程中的速率及能量的变化,进行以下实验,分析影响反应速率的因素。

实验时,
| 1分钟水滴数(断开K) | 34 | 59 | 86 | 117 | … | 102 |
| 1分钟水滴数(闭合K) | 58 | 81 | 112 | 139 | … | 78 |
分析反应过程中的水滴数,请回答:
① 由水滴数58>34、81>59,说明在反应初期,闭合K时比断开K时的反应速率快,主要原因是形成原电池反应速度快。
② 由水滴数102>78,说明在反应后期,断开K时的反应速率快于闭合K时的反应速率,主要原因是
③ 从能量转换形式不同的角度,分析水滴数86>81、117>112的主要原因是:
更新时间:2017-07-01 11:52:47
|
相似题推荐
填空题
|
较难
(0.4)
解题方法
【推荐1】NaClO2是一种重要的杀菌消毒剂,也常用来漂白织物等,其中一种生产工艺如下:步骤一,利用NaClO3在硫酸作用下与SO2反应生成 ClO2和一种酸式盐。步骤二,将ClO2在NaOH溶液中与H2O2反应即可生成NaClO2
回答下列问题:
(1)NaClO2中Cl的化合价为_____________ 。
(2)写出步骤一中生成ClO2的化学方程式____________________
(3) 步骤二反应中氧化剂与还原剂的物质的量之比为_________________ ,该反应中氧化产物是____________________ 。
(4)亚氯酸钠(NaClO2)在常温与黑暗处可保存一年。亚氯酸不稳定可分解,反应的离子方程式为HClO2―→ClO2↑+H++Cl-+H2O(未配平)。在该反应中,当有1 mol ClO2生成时转移的电子个数约为______________ 。
(5)Cl2、H2O2、ClO2(还原产物为Cl-)、O3(1 mol O3转化为1 mol O2和1 mol H2O)等物质常被用作消毒剂。等物质的量的上述物质消毒效率最高的是________ (填序号)。
(6)H2O2有时可作为矿业废液消毒剂,有“绿色氧化剂”的美称。如消除采矿业胶液中的氰化物(如KCN),经以下反应实现:KCN+H2O2+H2O=A+NH3↑,则生成物A的化学式为________ ,H2O2被称为“绿色氧化剂”的理由是___________________ 。
回答下列问题:
(1)NaClO2中Cl的化合价为
(2)写出步骤一中生成ClO2的化学方程式
(3) 步骤二反应中氧化剂与还原剂的物质的量之比为
(4)亚氯酸钠(NaClO2)在常温与黑暗处可保存一年。亚氯酸不稳定可分解,反应的离子方程式为HClO2―→ClO2↑+H++Cl-+H2O(未配平)。在该反应中,当有1 mol ClO2生成时转移的电子个数约为
(5)Cl2、H2O2、ClO2(还原产物为Cl-)、O3(1 mol O3转化为1 mol O2和1 mol H2O)等物质常被用作消毒剂。等物质的量的上述物质消毒效率最高的是
| A.Cl2 | B.H2O2 | C.ClO2 | D.O3 |
(6)H2O2有时可作为矿业废液消毒剂,有“绿色氧化剂”的美称。如消除采矿业胶液中的氰化物(如KCN),经以下反应实现:KCN+H2O2+H2O=A+NH3↑,则生成物A的化学式为
您最近一年使用:0次
【推荐2】阅读下面科普信息,回答问题:
一个体重 的健康人含铁2g,这2g铁在人体中以
的健康人含铁2g,这2g铁在人体中以 和
和 的形式存在。亚铁离子易被吸收,给贫血者补充铁时,应给予含亚铁离子的亚铁盐,如硫酸亚铁。服用维生素C,可使食物中的铁离子还原成亚铁离子,有利于铁的吸收。
的形式存在。亚铁离子易被吸收,给贫血者补充铁时,应给予含亚铁离子的亚铁盐,如硫酸亚铁。服用维生素C,可使食物中的铁离子还原成亚铁离子,有利于铁的吸收。
(1)以下为常见的铁元素的几种微粒,其中既有氧化性又有还原性的是_______ (填字母)。
A. B.
B. C.
C.
(2)工业盐的主要成分是 ,曾多次发生过因误食
,曾多次发生过因误食 而中毒的事件,其原因是
而中毒的事件,其原因是 把人体内的
把人体内的 转化为
转化为 而失去与
而失去与 结合的能力,这说明
结合的能力,这说明 具有
具有_______ 性。
(3)为了防止钢铁零件生锈,常用 进行化学处理方法使钢铁零件表面生成
进行化学处理方法使钢铁零件表面生成 的致密保护层——“发蓝”。化学处理过程中其中一步的反应为
的致密保护层——“发蓝”。化学处理过程中其中一步的反应为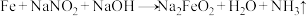 (未配平),上述反应中氧化剂与还原剂的化学计量系数之比为
(未配平),上述反应中氧化剂与还原剂的化学计量系数之比为_______ 。
(4)某同学把氯气通入 溶液中,生成
溶液中,生成 和
和 ,请写出该反应的化学方程式:
,请写出该反应的化学方程式:_______ 。
(5)工业废水中的 可用铝粉除去。已知此反应体系中包含
可用铝粉除去。已知此反应体系中包含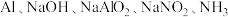 和
和 六种物质,该反应的化学方程式为
六种物质,该反应的化学方程式为_______ 。
一个体重
 的健康人含铁2g,这2g铁在人体中以
的健康人含铁2g,这2g铁在人体中以 和
和 的形式存在。亚铁离子易被吸收,给贫血者补充铁时,应给予含亚铁离子的亚铁盐,如硫酸亚铁。服用维生素C,可使食物中的铁离子还原成亚铁离子,有利于铁的吸收。
的形式存在。亚铁离子易被吸收,给贫血者补充铁时,应给予含亚铁离子的亚铁盐,如硫酸亚铁。服用维生素C,可使食物中的铁离子还原成亚铁离子,有利于铁的吸收。(1)以下为常见的铁元素的几种微粒,其中既有氧化性又有还原性的是
A.
 B.
B. C.
C.
(2)工业盐的主要成分是
 ,曾多次发生过因误食
,曾多次发生过因误食 而中毒的事件,其原因是
而中毒的事件,其原因是 把人体内的
把人体内的 转化为
转化为 而失去与
而失去与 结合的能力,这说明
结合的能力,这说明 具有
具有(3)为了防止钢铁零件生锈,常用
 进行化学处理方法使钢铁零件表面生成
进行化学处理方法使钢铁零件表面生成 的致密保护层——“发蓝”。化学处理过程中其中一步的反应为
的致密保护层——“发蓝”。化学处理过程中其中一步的反应为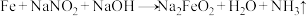 (未配平),上述反应中氧化剂与还原剂的化学计量系数之比为
(未配平),上述反应中氧化剂与还原剂的化学计量系数之比为(4)某同学把氯气通入
 溶液中,生成
溶液中,生成 和
和 ,请写出该反应的化学方程式:
,请写出该反应的化学方程式:(5)工业废水中的
 可用铝粉除去。已知此反应体系中包含
可用铝粉除去。已知此反应体系中包含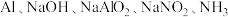 和
和 六种物质,该反应的化学方程式为
六种物质,该反应的化学方程式为
您最近一年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐3】H、C、N、O、Mg、Al、Si、S、Cu是中学化学中常见的元素,请根据题意回答与这些元素有关的问题:
(1)S的原子结构示意图为_______ 。
(2)14C可用于古代文物年代鉴定,其原子核内的中子数为_______ 。
(3)根据元素周期律,碳的非金属性强于硅,请用一个化学反应方程式表示_______ 。
(4)粉末状的Si3N4对空气和水都不稳定,但将粉末状的Si3N4和适量氧化镁在一定条件下的密闭容器中热处理,可以得到对空气、水、和酸都相当稳定的固体材料,同时还可生成对水不稳定的Mg3N2,热处理后除去MgO和Mg3N2的方法是_______ 。
(5)某铜铝合金用足量稀硝酸完全溶解,得到标准状况下NO 11.2 L,再向溶液中加入过量氨水,充分反应后过滤。若沉淀质量为7.8g,则合金的质量为_______ g。
(6)将由NO和NO2组成的混合气体通入如图所示的装置中,用来验证浓硝酸的氧化性比稀硝酸的氧化性强(在通入混合气体之前,已通入一段时间的N2)。

已知:(i)浓硝酸能将NO氧化成NO2,而稀硝酸不能氧化NO。
(ii)NaOH溶液与NO2能发生反应生成两种盐和水,NaOH溶液与NO不反应。
a.装置②、③、④中盛放的药品依次是_______ 、_______ 、_______ 。
b.能够说明实验已成功的现象是_______ 。
(1)S的原子结构示意图为
(2)14C可用于古代文物年代鉴定,其原子核内的中子数为
(3)根据元素周期律,碳的非金属性强于硅,请用一个化学反应方程式表示
(4)粉末状的Si3N4对空气和水都不稳定,但将粉末状的Si3N4和适量氧化镁在一定条件下的密闭容器中热处理,可以得到对空气、水、和酸都相当稳定的固体材料,同时还可生成对水不稳定的Mg3N2,热处理后除去MgO和Mg3N2的方法是
(5)某铜铝合金用足量稀硝酸完全溶解,得到标准状况下NO 11.2 L,再向溶液中加入过量氨水,充分反应后过滤。若沉淀质量为7.8g,则合金的质量为
(6)将由NO和NO2组成的混合气体通入如图所示的装置中,用来验证浓硝酸的氧化性比稀硝酸的氧化性强(在通入混合气体之前,已通入一段时间的N2)。

已知:(i)浓硝酸能将NO氧化成NO2,而稀硝酸不能氧化NO。
(ii)NaOH溶液与NO2能发生反应生成两种盐和水,NaOH溶液与NO不反应。
a.装置②、③、④中盛放的药品依次是
b.能够说明实验已成功的现象是
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐1】硫及其化合物应用广泛,同时也会对环境造成污染。
(1)硫被用来制造黑色火药、火柴等,也是生产橡胶制品的重要原料。有一种硫单质Sx,该单质蒸气对氢气的相对密度为128,则x=___________ 。
(2)H2S有剧毒,可用作有机合成还原剂、农药、医药、催化剂的再生等。一种脱硫技术如下:第一步,用Na2CO3溶液吸收H2S:H2S+Na2CO3=NaHS+NaHCO3;第二步,用NaVO3溶液与NaHS反应生成硫单质,同时还产生Na2V4O9.Na2V4O9中V的平均化合价为___________ ,第二步反应的离子方程式为___________ 。
(3)SO2尾气先用氨水吸收生成(NH4)2SO3, 再被氧化成
再被氧化成 ,最终得到副产物氮肥,变废为宝。两种氧化方案如下:
,最终得到副产物氮肥,变废为宝。两种氧化方案如下:
方案l:2 +O2=2
+O2=2 。
。
方案2:2[Co(NH3)6]2++O2=[(NH3)5Co-O-O-Co(NH3)5]4++2NH3, +H2O+2NH3+[(NH3)5Co-O-O-Co(NH3)5]4+⇌
+H2O+2NH3+[(NH3)5Co-O-O-Co(NH3)5]4+⇌ +2[Co(NH3)6]3++2OH-。
+2[Co(NH3)6]3++2OH-。
①氨水中存在的分子有___________ (填化学式)。
②通过实验可知,[(NH3)5Co-O-O-Co(NH3)5]4+将 氧化为
氧化为 的能力大于O2,可能的原因是
的能力大于O2,可能的原因是___________ 。
(4)连二亚硫酸钠(Na2S2O4)适合作木浆造纸的漂白剂。实验室制法:将甲酸和溶于甲醇和水混合溶剂的NaOH混合反应后,再通入SO2气体即可制得连二亚硫酸钠,同时生成能使澄清石灰水变浑浊的气体,则该制备反应的化学方程式为___________ 。
(1)硫被用来制造黑色火药、火柴等,也是生产橡胶制品的重要原料。有一种硫单质Sx,该单质蒸气对氢气的相对密度为128,则x=
(2)H2S有剧毒,可用作有机合成还原剂、农药、医药、催化剂的再生等。一种脱硫技术如下:第一步,用Na2CO3溶液吸收H2S:H2S+Na2CO3=NaHS+NaHCO3;第二步,用NaVO3溶液与NaHS反应生成硫单质,同时还产生Na2V4O9.Na2V4O9中V的平均化合价为
(3)SO2尾气先用氨水吸收生成(NH4)2SO3,
 再被氧化成
再被氧化成 ,最终得到副产物氮肥,变废为宝。两种氧化方案如下:
,最终得到副产物氮肥,变废为宝。两种氧化方案如下:方案l:2
 +O2=2
+O2=2 。
。方案2:2[Co(NH3)6]2++O2=[(NH3)5Co-O-O-Co(NH3)5]4++2NH3,
 +H2O+2NH3+[(NH3)5Co-O-O-Co(NH3)5]4+⇌
+H2O+2NH3+[(NH3)5Co-O-O-Co(NH3)5]4+⇌ +2[Co(NH3)6]3++2OH-。
+2[Co(NH3)6]3++2OH-。①氨水中存在的分子有
②通过实验可知,[(NH3)5Co-O-O-Co(NH3)5]4+将
 氧化为
氧化为 的能力大于O2,可能的原因是
的能力大于O2,可能的原因是(4)连二亚硫酸钠(Na2S2O4)适合作木浆造纸的漂白剂。实验室制法:将甲酸和溶于甲醇和水混合溶剂的NaOH混合反应后,再通入SO2气体即可制得连二亚硫酸钠,同时生成能使澄清石灰水变浑浊的气体,则该制备反应的化学方程式为
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐2】有下列物质:A.甲醛 B.葡萄糖 C.乙醇 D.乙酸 E.油脂 F.二氧化硫 G.氢氧化铝 (填写序号):
(1)工业上制备肥皂的主要原料是_________ ;
(2)注射时用于皮肤杀菌、消毒的物质主要成分是_________ ;
(3)能用于除去热水瓶胆水垢〔主要成分:CaCO3,Mg(OH)2〕的是_________ ;
(4)既能与强酸反应又能与强碱反应生成盐和水的物质是_________ ;
(5)形成酸雨的主要物质是_________ ;
(6)可用于标本制作的防腐剂的是_________ ;
(7)糖尿病人通常是指病人的尿液中_________ 的含量高。
(1)工业上制备肥皂的主要原料是
(2)注射时用于皮肤杀菌、消毒的物质主要成分是
(3)能用于除去热水瓶胆水垢〔主要成分:CaCO3,Mg(OH)2〕的是
(4)既能与强酸反应又能与强碱反应生成盐和水的物质是
(5)形成酸雨的主要物质是
(6)可用于标本制作的防腐剂的是
(7)糖尿病人通常是指病人的尿液中
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐3】NOx、SO2是主要的大气污染物,能引发雾霾、光化学烟雾及酸雨。
(1)NO2会产生硝酸型酸雨,硝酸型酸雨中主要溶质的化学式为_______________ 。
(2)目前新出厂的汽车均加装尿素[CO(NH2)2]箱,尾气中NO、NO2及尿素以物质的量之比1:1:1加热催化生成无害气体的化学方程式为_____________________________ 。
(3)氨化法同时脱硫脱硝的原理如下(已知NH4NO2在浓度较大时会分解)

①“催化氧化”的目的是________________ 。
②最终得到副产品的主要成分为____________ (填化学式)。
③相同条件下用氨水作吸收剂,NOx的脱除率与pH及 的关系如图所示。
的关系如图所示。

pH及其他条件相同时, 的比值越大,NOx的拖出率也越大,其主要原因是
的比值越大,NOx的拖出率也越大,其主要原因是_________________ 。
(1)NO2会产生硝酸型酸雨,硝酸型酸雨中主要溶质的化学式为
(2)目前新出厂的汽车均加装尿素[CO(NH2)2]箱,尾气中NO、NO2及尿素以物质的量之比1:1:1加热催化生成无害气体的化学方程式为
(3)氨化法同时脱硫脱硝的原理如下(已知NH4NO2在浓度较大时会分解)

①“催化氧化”的目的是
②最终得到副产品的主要成分为
③相同条件下用氨水作吸收剂,NOx的脱除率与pH及
 的关系如图所示。
的关系如图所示。
pH及其他条件相同时,
 的比值越大,NOx的拖出率也越大,其主要原因是
的比值越大,NOx的拖出率也越大,其主要原因是
您最近一年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐1】利用元素的化合价推测物质的性质是化学研究的重要手段。如图是硫元素的常见化合价与部分物质类别的对应关系:
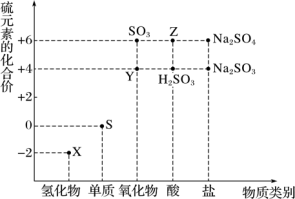
(1)将X与Y混合可生成淡黄色固体,该反应中氧化剂与还原剂的物质的量之比为___________ 。
(2)Z 的浓溶液与铜单质在一定条件下可以发生化学反应,该反应的化学方程式为_______ 。
(3) Na2S2O3是重要的化工原料。从氧化还原反应的角度分析,下列制备 Na2S2O3的方案理论上可行的是_______ (填字母) 。
a.Na2S+S b.Na2SO3+S c.SO2+Na2SO4 d.Na2SO3+Na2SO4
(4)已知 Na2SO3能被 K2Cr2O7氧化为Na2SO4,则 24 mL 0.05 mol·L-1的 Na2SO3溶液与 20 mL 0.02 mol·L-1的K2Cr2O7溶液恰好反应时,Cr 元素在还原产物中的化合价为_______ 。

(1)将X与Y混合可生成淡黄色固体,该反应中氧化剂与还原剂的物质的量之比为
(2)Z 的浓溶液与铜单质在一定条件下可以发生化学反应,该反应的化学方程式为
(3) Na2S2O3是重要的化工原料。从氧化还原反应的角度分析,下列制备 Na2S2O3的方案理论上可行的是
a.Na2S+S b.Na2SO3+S c.SO2+Na2SO4 d.Na2SO3+Na2SO4
(4)已知 Na2SO3能被 K2Cr2O7氧化为Na2SO4,则 24 mL 0.05 mol·L-1的 Na2SO3溶液与 20 mL 0.02 mol·L-1的K2Cr2O7溶液恰好反应时,Cr 元素在还原产物中的化合价为
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐2】某同学利用如下图所示装置完成了浓硫酸和SO2的性质实验(夹持装置已省略)。请回答下列问题
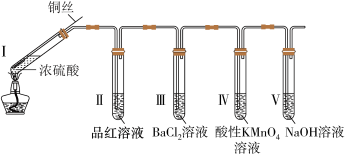
(1)将螺旋状的铜丝伸入浓硫酸中,发生反应的化学方程式为____________ 。
(2)实验中,试管Ⅱ中的品红溶液_____________ (填现象)。
(3)下列说法不正确的是_______ (填字母代号)
A.反应后,将试管I中的液体逐滴加入水中,溶液呈蓝色 B.试管Ⅲ中出现白色浑浊
C.试管Ⅳ中的酸性KMnO4溶液褪色 D.试管V中的NaOH溶液用于吸收尾气
(4)若反应中有0.02 mol H2SO4被还原,则反应产生的气体体积为______ mL(标准状况下)。

(1)将螺旋状的铜丝伸入浓硫酸中,发生反应的化学方程式为
(2)实验中,试管Ⅱ中的品红溶液
(3)下列说法不正确的是
A.反应后,将试管I中的液体逐滴加入水中,溶液呈蓝色 B.试管Ⅲ中出现白色浑浊
C.试管Ⅳ中的酸性KMnO4溶液褪色 D.试管V中的NaOH溶液用于吸收尾气
(4)若反应中有0.02 mol H2SO4被还原,则反应产生的气体体积为
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐1】氢气还原氧化铜反应不完全时,得到的是Cu、Cu2O、CuO的固体混合物。某化学兴趣小组为了探究某次氢气还原CuO实验最终所得的产物的组成,进行了如下实验:
①取一定质量的均匀的上述固体混合物A,将其分成两等份。
②取其中一份用足量的氢气还原,测得反应后固体的质量减小了3.20g
③另一份加入500mL的稀硝酸,固体恰好完全溶解,且同时收集到标准状况下NO气体2.24L。
请回答以下问题:
(1)A中,所含氧元素的物质的量为_________ 。
(2)A中,n(Cu)+n(Cu2O)=_______________ 。
(3)所用稀硝酸的物质的量浓度为_______________ 。
①取一定质量的均匀的上述固体混合物A,将其分成两等份。
②取其中一份用足量的氢气还原,测得反应后固体的质量减小了3.20g
③另一份加入500mL的稀硝酸,固体恰好完全溶解,且同时收集到标准状况下NO气体2.24L。
请回答以下问题:
(1)A中,所含氧元素的物质的量为
(2)A中,n(Cu)+n(Cu2O)=
(3)所用稀硝酸的物质的量浓度为
您最近一年使用:0次