实验室制取氯气时,为了除去Cl2中的HCl气体,可使气体通过下列溶液中的_________ ,为了干燥Cl2,可使气体通过下列溶液中的____________ 。①NaOH溶液 ②饱和食盐水 ③AgNO3溶液 ④浓H2SO4,当氯气通过浸有淀粉KI溶液的棉花球时,现象是棉花球表面变成__________ 。反应的离子方程式是______________________ 。
更新时间:2017-07-13 14:59:07
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】双氧水和84消毒液是生活中常用的两种消毒剂,了解物质的性质是科学合理使用化学品的基础和前提。请回答下列问题:
(1)某同学设计如下实验研究H2O2的性质
① 从理论上看H2O2既有氧化性又有还原性,具有还原性的原因是___________ 。
② 能证明H2O2具有还原性的实验是___________ (填序号),可作为证据的实验现象是___________ (填字母序号)。
(2)84消毒液的有效成分为NaClO。
①实验室制备氯气的化学方程式是___________ 。
②将Cl2通入NaOH溶液中可制得84消毒液,化学反应方程式为___________ 。
③84消毒液不能用于钢制器具的消毒,原因是NaClO具有___________ 性。
④84消毒液的溶液在浸泡餐具过程中,因吸收空气中CO2消毒杀菌能力增强,用化学用语解释___________ 。(已知:酸性H2CO3>HClO>HCO )
)
(3)2016年巴西奥运会期间,由于工作人员将84消毒液与双氧水两种消毒剂混用,导致游泳池藻类快速生长,池水变绿。一种可能的原因是NaClO与H2O2反应产生O2促进藻类快速生长。
①该反应说明氧化性:NaClO___________ H2O2的(填“>”或“<”)。
②当有0.1mol O2生成时,转移电子___________ mol。
(1)某同学设计如下实验研究H2O2的性质
| 序号 | 实验 | 实验现象 |
| ⅰ | 向5%H2O2溶液中滴加酸性KMnO4溶液 | a. 溶液紫色褪去 b. 有大量气泡产生 |
| ⅱ | 向5%H2O2溶液中滴加淀粉碘化钾溶液 | c. 溶液变蓝 |
② 能证明H2O2具有还原性的实验是
(2)84消毒液的有效成分为NaClO。
①实验室制备氯气的化学方程式是
②将Cl2通入NaOH溶液中可制得84消毒液,化学反应方程式为
③84消毒液不能用于钢制器具的消毒,原因是NaClO具有
④84消毒液的溶液在浸泡餐具过程中,因吸收空气中CO2消毒杀菌能力增强,用化学用语解释
 )
)(3)2016年巴西奥运会期间,由于工作人员将84消毒液与双氧水两种消毒剂混用,导致游泳池藻类快速生长,池水变绿。一种可能的原因是NaClO与H2O2反应产生O2促进藻类快速生长。
①该反应说明氧化性:NaClO
②当有0.1mol O2生成时,转移电子
您最近一年使用:0次
【推荐2】重铬酸钾 和浓盐酸在一定温度下反应可制备黄绿色的氯气,其化学方程式为
和浓盐酸在一定温度下反应可制备黄绿色的氯气,其化学方程式为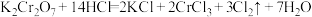 。
。
(1)浓盐酸在反应中表现出来的性质是_______ (填写编号)
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
(2) 是
是_______ (“氧化”或“还原”)产物;产生 ,则转移电子的物质的量为
,则转移电子的物质的量为____ mol。
(3)从铬元素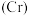 的化合价态上判断,
的化合价态上判断,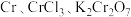 三种物质中的铬元素既表现氧化性又表现还原性的是
三种物质中的铬元素既表现氧化性又表现还原性的是_____________ (写化学式,下同)。
(4)已知氯气有毒,与水反应生成两种酸。实验室制备氯气可选用__________ 溶液进行尾气处理。
 和浓盐酸在一定温度下反应可制备黄绿色的氯气,其化学方程式为
和浓盐酸在一定温度下反应可制备黄绿色的氯气,其化学方程式为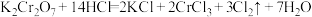 。
。(1)浓盐酸在反应中表现出来的性质是
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
(2)
 是
是 ,则转移电子的物质的量为
,则转移电子的物质的量为(3)从铬元素
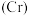 的化合价态上判断,
的化合价态上判断,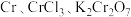 三种物质中的铬元素既表现氧化性又表现还原性的是
三种物质中的铬元素既表现氧化性又表现还原性的是(4)已知氯气有毒,与水反应生成两种酸。实验室制备氯气可选用
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】氧化还原反应是一类重要的反应,在工农业生产、实验室、日常生活中都有广泛的用途。
(1)广西南宁隆安县是全国知名的火龙果种植基地,火龙果富含的花肝素能够消耗活性氧,说明花青素可以作为___________ 剂(填“氧化”或“还原”)。
(2)治理汽车尾气的一种方法是在汽车的排气管上装一个催化转化装置。在催化转化器中,汽车尾气中的CO和NO在催化剂、高温条件下发生反应,生成两种无毒气体。请写出该反应的化学方程式___________ 。
(3) 可在呼吸面具和潜水艇中作为氧气的来源,请写出
可在呼吸面具和潜水艇中作为氧气的来源,请写出 和
和 反应的化学方程式
反应的化学方程式___________ ,其中 在该反应中
在该反应中___________ (填标号)。
A.作氧化剂B.作还原剂
C.既是氧化剂又是还原剂D.既不是氧化剂也不是还原剂
(4)《天工开物》记载“凡火药以硝石、硫磺为主,草木灰为辅……魂散惊而魄齑粉”,其中涉及的主要反应为: ,该反应过程中转移6mol电子时,产生的
,该反应过程中转移6mol电子时,产生的 在标况下体积为
在标况下体积为___________ L。
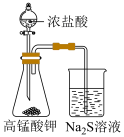
(5)实验室可以用高锰酸钾和浓盐酸反应制备氯气,请写出该反应的离子方程式:__________ 。现采用如图所示的装置探究物质氧化性强弱,若观察到右侧烧杯出现淡黄色沉淀,则说明 、
、 和S的氧化性由强到弱的顺序为:
和S的氧化性由强到弱的顺序为:___________ 。
(1)广西南宁隆安县是全国知名的火龙果种植基地,火龙果富含的花肝素能够消耗活性氧,说明花青素可以作为
(2)治理汽车尾气的一种方法是在汽车的排气管上装一个催化转化装置。在催化转化器中,汽车尾气中的CO和NO在催化剂、高温条件下发生反应,生成两种无毒气体。请写出该反应的化学方程式
(3)
 可在呼吸面具和潜水艇中作为氧气的来源,请写出
可在呼吸面具和潜水艇中作为氧气的来源,请写出 和
和 反应的化学方程式
反应的化学方程式 在该反应中
在该反应中A.作氧化剂B.作还原剂
C.既是氧化剂又是还原剂D.既不是氧化剂也不是还原剂
(4)《天工开物》记载“凡火药以硝石、硫磺为主,草木灰为辅……魂散惊而魄齑粉”,其中涉及的主要反应为:
 ,该反应过程中转移6mol电子时,产生的
,该反应过程中转移6mol电子时,产生的 在标况下体积为
在标况下体积为(5)实验室可以用高锰酸钾和浓盐酸反应制备氯气,请写出该反应的离子方程式:
 、
、 和S的氧化性由强到弱的顺序为:
和S的氧化性由强到弱的顺序为:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】以Cl2、NaOH、(NH2)2CO(尿素)和SO2为原料可制备N2H4·H2O(水合肼)和无水Na2SO3,其主要实验流程如下:
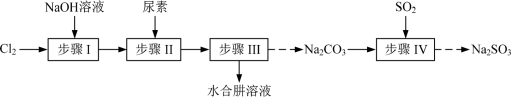
已知:①Cl2+2OH−=ClO−+Cl−+H2O是放热反应。
②N2H4·H2O沸点约118℃,具有强还原性,能与NaClO剧烈反应生成N2。
步骤I制备NaClO溶液时,若温度超过40℃,Cl2与NaOH溶液反应生成NaClO3和NaCl,其离子方程式为_______ ;实验中控制温度除用冰水浴外,还需采取的措施是_______ 。

已知:①Cl2+2OH−=ClO−+Cl−+H2O是放热反应。
②N2H4·H2O沸点约118℃,具有强还原性,能与NaClO剧烈反应生成N2。
步骤I制备NaClO溶液时,若温度超过40℃,Cl2与NaOH溶液反应生成NaClO3和NaCl,其离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】化学与资源利用、材料研制、环境保护等密切相关。
(1)海水中蕴含的元素有80多种,它是一个巨大的宝藏。
①海水中镁的总储量约为1.8×1015 t,海水里镁的存在形式主要是_________ 。(填“游离态”或“化合态”)
②下列物质不经过化学变化就能从海水中获得的是______ 。(填字母)
A.单质钠 B.单质钾 C.氯化钠
③目前化学工业的主要支柱之一是氯碱工业,它是以电解_______ 为基础制取氯气等产品的工业。
(2)材料是人类生存和发展的物质基础,合理使用材料可以改善人类生活。
①工业上制造光导纤维的基本原料是_______ 。
②下列物质中,不能用来制造耐火材料的是_______ 。(填字母)
A.氧化镁 B.三氧化二铝 C.过氧化钠
③在生铁和钢这2种金属材料中,含碳量较高的是_______ 。
(3)保持洁净安全的生存环境已成为全人类的共识。
①pH<_______ 的雨水称为酸雨。
②下列物质中,会破坏臭氧层的是_______ 。(填字母)
A.氮气 B.一氧化碳 C.氟氯烃
③在生产中,人们曾用浓氨水来检验氯气管道是否漏气,已知能发生的反应为(在有水蒸气存在时):2NH3 +3Cl2=6HCl + N2,则如果氯气管道某处漏气,用该方法检查时的现象是______ 。
(1)海水中蕴含的元素有80多种,它是一个巨大的宝藏。
①海水中镁的总储量约为1.8×1015 t,海水里镁的存在形式主要是
②下列物质不经过化学变化就能从海水中获得的是
A.单质钠 B.单质钾 C.氯化钠
③目前化学工业的主要支柱之一是氯碱工业,它是以电解
(2)材料是人类生存和发展的物质基础,合理使用材料可以改善人类生活。
①工业上制造光导纤维的基本原料是
②下列物质中,不能用来制造耐火材料的是
A.氧化镁 B.三氧化二铝 C.过氧化钠
③在生铁和钢这2种金属材料中,含碳量较高的是
(3)保持洁净安全的生存环境已成为全人类的共识。
①pH<
②下列物质中,会破坏臭氧层的是
A.氮气 B.一氧化碳 C.氟氯烃
③在生产中,人们曾用浓氨水来检验氯气管道是否漏气,已知能发生的反应为(在有水蒸气存在时):2NH3 +3Cl2=6HCl + N2,则如果氯气管道某处漏气,用该方法检查时的现象是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】含氧化合物具有广泛的应用,请回答下列问题。
(1) 中含有的电子数目为
中含有的电子数目为___________ 。
(2)将氯气持续通入紫色石蕊试液中,溶液颜色如图变化:

溶液中导致变色的微粒Ⅰ是___________ (填微粒符号,下同),Ⅱ是___________ ,Ⅲ是___________ 。
(3)氯气和氢氧化钠溶液反应可制备“84消毒液”,其化学方程式为___________ 。
(4)漂白粉漂白时,通入 可增加漂白效果,其化学方程式为
可增加漂白效果,其化学方程式为___________ 。
(5)用坩埚钳夹住一束铁丝,灼烧后立刻放入充满氯气的集气瓶中,反应的现象为___________ 。
(6) 是酸性氧化物,
是酸性氧化物, 和碱反应生成
和碱反应生成 的化学方程式为
的化学方程式为___________ 。
(1)
 中含有的电子数目为
中含有的电子数目为(2)将氯气持续通入紫色石蕊试液中,溶液颜色如图变化:

溶液中导致变色的微粒Ⅰ是
(3)氯气和氢氧化钠溶液反应可制备“84消毒液”,其化学方程式为
(4)漂白粉漂白时,通入
 可增加漂白效果,其化学方程式为
可增加漂白效果,其化学方程式为(5)用坩埚钳夹住一束铁丝,灼烧后立刻放入充满氯气的集气瓶中,反应的现象为
(6)
 是酸性氧化物,
是酸性氧化物, 和碱反应生成
和碱反应生成 的化学方程式为
的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】尾气处理装置(见下图a、b、c)
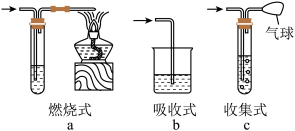
(1)制取Cl2时,尾气的处理可采用________ 装置。
(2)制取CO时,尾气处理可采用________ 装置。
(3)制取H2时,尾气处理可采用________ 装置。

(1)制取Cl2时,尾气的处理可采用
(2)制取CO时,尾气处理可采用
(3)制取H2时,尾气处理可采用
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】据报道,日常生活中,将洁厕液与84消毒液混合使用会发生中毒的事故。
1.两种日化产品主要成分中都含有氯元素,该元素在元素周期表中位置是_______ ,写出氯原子最外层电子排布的轨道表示式_____________ 。
2.84消毒液的主要成分是次氯酸钠,写出次氯酸钠的电子式______ .若将84消毒液长期露置于空气中,溶液中的主要成分将变为________ 。(填化学式)
3.洁厕灵的主要成分是HCl。下列关于卤化氢的性质比较中错误的是____
A. 酸性:HF>HCl>HBr>HI
B. 键能:H—F>H—Cl>H—Br>H—I
C. 熔点:HF<HCl<HBr<HI
D. 还原性:HF<HCl<HBr<HI
4.洁厕液与84消毒液混合后会发生氧化还原反应,生成有毒的氯气。写出该反应的离子方程式____ 。
5.下列氧化还原反应中,与上述反应类型不同的是____
A. Na2S2O3+ H2SO4 → Na2SO4+ S + SO2+ H2O
B. 2FeCl3+ Fe → 2FeCl2
C. S + 2H2SO4(浓) 3SO2+ 2H2O
3SO2+ 2H2O
D. KClO3+ 5KCl + 3H2SO4 → 3K2SO4 + 3Cl2 + 3H2O
6.若以物质单位质量得到的电子数衡量物质的消毒效率,则下列常用的消毒剂中,消毒效率最高的是____
A. NaClO B. ClO2 C. Cl2 D. Ca(ClO)2
1.两种日化产品主要成分中都含有氯元素,该元素在元素周期表中位置是
2.84消毒液的主要成分是次氯酸钠,写出次氯酸钠的电子式
3.洁厕灵的主要成分是HCl。下列关于卤化氢的性质比较中错误的是
A. 酸性:HF>HCl>HBr>HI
B. 键能:H—F>H—Cl>H—Br>H—I
C. 熔点:HF<HCl<HBr<HI
D. 还原性:HF<HCl<HBr<HI
4.洁厕液与84消毒液混合后会发生氧化还原反应,生成有毒的氯气。写出该反应的离子方程式
5.下列氧化还原反应中,与上述反应类型不同的是
A. Na2S2O3+ H2SO4 → Na2SO4+ S + SO2+ H2O
B. 2FeCl3+ Fe → 2FeCl2
C. S + 2H2SO4(浓)
 3SO2+ 2H2O
3SO2+ 2H2OD. KClO3+ 5KCl + 3H2SO4 → 3K2SO4 + 3Cl2 + 3H2O
6.若以物质单位质量得到的电子数衡量物质的消毒效率,则下列常用的消毒剂中,消毒效率最高的是
A. NaClO B. ClO2 C. Cl2 D. Ca(ClO)2
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】下列七种有机物中:
A.CH4 B.CH2=CH2 C. D.CH3COOH E.淀粉 F.葡萄糖 G.蛋白质
D.CH3COOH E.淀粉 F.葡萄糖 G.蛋白质
(1)酸性比碳酸强的是___________ (填字母编号,下同)。
(2)易发生银镜反应的是___________ 。
(3)具有正四面体结构的是___________ 。
(4)通常用于检验碘单质的是___________ 。
(5)可用于合成聚乙烯塑料的是___________ 。
(6)可与浓硝酸发生颜色反应的是___________ 。
(7)在空气中燃烧产生带浓烟火焰的是___________ 。
A.CH4 B.CH2=CH2 C.
 D.CH3COOH E.淀粉 F.葡萄糖 G.蛋白质
D.CH3COOH E.淀粉 F.葡萄糖 G.蛋白质(1)酸性比碳酸强的是
(2)易发生银镜反应的是
(3)具有正四面体结构的是
(4)通常用于检验碘单质的是
(5)可用于合成聚乙烯塑料的是
(6)可与浓硝酸发生颜色反应的是
(7)在空气中燃烧产生带浓烟火焰的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】亚硝酸钠可使肉制品色泽粉红,外观上好看诱人,大量食用会致癌。
(1)NaNO2 俗称“工业盐”,外观与食盐相似,误食会中毒,可通过化学实验加以鉴别。如 向 NaNO2 的酸性溶液中加入 KI 固体,析出的碘单质可以使淀粉溶液变蓝色,据此检验 NO2 。
①该反应中被氧化的元素是_______ (填符号)。
②完成下列反应的化学方程式并配平。
____ NaNO2+____ KI+____ H2SO4=____ +_____ +____ I2+____ NO↑+____
③标准状况下,该反应中每转移 1 mol e-,生成气体的体积是_______ 。
(2)硝酸工业生产中的尾气可用纯碱溶液吸收,有关的化学反应为: 2NO2+Na2CO3=NaNO2+NaNO3+CO2↑氧化剂与还原剂的物质的量之比为_______ 。每产生 33.6 L(标准状况下)CO2,吸收液质量将增加 _______ g。
(3)某同学把 NaNO2 加到硫酸酸化的 KMnO4 溶液中,观察到 KMnO4 溶液褪色且无沉 淀生成,同时生成 KNO3 和 MnSO4,写出该反应的离子方程式:_______
(1)NaNO2 俗称“工业盐”,外观与食盐相似,误食会中毒,可通过化学实验加以鉴别。如 向 NaNO2 的酸性溶液中加入 KI 固体,析出的碘单质可以使淀粉溶液变蓝色,据此检验 NO2 。
①该反应中被氧化的元素是
②完成下列反应的化学方程式并配平。
③标准状况下,该反应中每转移 1 mol e-,生成气体的体积是
(2)硝酸工业生产中的尾气可用纯碱溶液吸收,有关的化学反应为: 2NO2+Na2CO3=NaNO2+NaNO3+CO2↑氧化剂与还原剂的物质的量之比为
(3)某同学把 NaNO2 加到硫酸酸化的 KMnO4 溶液中,观察到 KMnO4 溶液褪色且无沉 淀生成,同时生成 KNO3 和 MnSO4,写出该反应的离子方程式:
您最近一年使用:0次



