Ⅰ.目前合成的储氢纳米碳管常伴有大量的碳纳米颗粒(杂质),这种颗粒可用氧化气化法提纯,其反应式为:
___C+ K2Cr2O7+___H2SO4===___CO2↑+___Cr2(SO4)3+___K2SO4+___H2O
(1)配平上述化学反应方程式(请将配平的计量数依次填入上式)_____________ 。
(2)该反应的氧化剂是______________ ,氧化产物的电子式为__________________ 。
(3)H2SO4在上述反应中表现出来的性质是________ (填选项编号)。
A.酸性 B.氧化性 C.吸水性 D.脱水性
(4)上述反应中若产生0.2 mol CO2 ,则转移电子的物质的量是_________ mol。
Ⅱ.三氟化氮(NF3)是一种无色无味的气体,可由氟与氨在一定条件下反应制得。
(1)写出该反应化学方程式并标明电子转移的方向和数目____________________________ 。
(2)27.0 mL NF3和水充分反应,生成 18.0 mL NO(同温、同压下),写出反应的化学方程式:______________________________________________________________________ 。
(3)NF3是一种无色无味的气体,但一旦NF3在空气中泄漏,还是易于发现的。该气体泄漏时的现象是_________________________________________________________________ 。
___C+ K2Cr2O7+___H2SO4===___CO2↑+___Cr2(SO4)3+___K2SO4+___H2O
(1)配平上述化学反应方程式(请将配平的计量数依次填入上式)
(2)该反应的氧化剂是
(3)H2SO4在上述反应中表现出来的性质是
A.酸性 B.氧化性 C.吸水性 D.脱水性
(4)上述反应中若产生0.2 mol CO2 ,则转移电子的物质的量是
Ⅱ.三氟化氮(NF3)是一种无色无味的气体,可由氟与氨在一定条件下反应制得。
(1)写出该反应化学方程式并标明电子转移的方向和数目
(2)27.0 mL NF3和水充分反应,生成 18.0 mL NO(同温、同压下),写出反应的化学方程式:
(3)NF3是一种无色无味的气体,但一旦NF3在空气中泄漏,还是易于发现的。该气体泄漏时的现象是
更新时间:2017-08-04 09:56:15
|
相似题推荐
计算题
|
适中
(0.65)
解题方法
【推荐1】(1)4.9 g H2SO4含________ 个H2SO4分子,能和________ mol NaOH完全反应。
(2)含有相同碳原子数的CO和CO2,其质量比为_____________ 。
(3)在同温同压下,等质量的CO和CO2,其体积之比为___________ 。
(4)在一定的温度和压强下,1体积气体X2跟3体积气体Y2化合生成2体积化合物C,则该化合物的化学式是____________ 。
(5)某盐混合溶液中含有离子:Na+、Mg2+、Cl-、 ,测得Na+、Mg2+和Cl-的物质的量浓度依次为0.2 mol·L-1、0.25 mol·L-1、0.4 mol·L-1,则c(
,测得Na+、Mg2+和Cl-的物质的量浓度依次为0.2 mol·L-1、0.25 mol·L-1、0.4 mol·L-1,则c( )=
)=________ 。
(2)含有相同碳原子数的CO和CO2,其质量比为
(3)在同温同压下,等质量的CO和CO2,其体积之比为
(4)在一定的温度和压强下,1体积气体X2跟3体积气体Y2化合生成2体积化合物C,则该化合物的化学式是
(5)某盐混合溶液中含有离子:Na+、Mg2+、Cl-、
 ,测得Na+、Mg2+和Cl-的物质的量浓度依次为0.2 mol·L-1、0.25 mol·L-1、0.4 mol·L-1,则c(
,测得Na+、Mg2+和Cl-的物质的量浓度依次为0.2 mol·L-1、0.25 mol·L-1、0.4 mol·L-1,则c( )=
)=
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】含有相同氧原子数的CO和CO2两份气体
(1)其质量之比为_______ 。
(2)同温同压时,其体积之比为______ ,密度之比为______ 。
(3)同温同体积时,其压强之比为_____ ,密度之比为______ 。
(1)其质量之比为
(2)同温同压时,其体积之比为
(3)同温同体积时,其压强之比为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】回答下列问题
(1)已知:3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O。
①NO是___________ 产物(填“氧化”或“还原”)
②若反应中有64g铜溶解,则被还原的HNO3的质量为___________ 。
(2)智利硝石矿层中含有碘酸钠,可用亚硫酸氢钠与其反应来制备单质碘,其化学方程式为:2NaIO3+5NaHSO3=3NaHSO4+2Na2SO4+I2+H2O
①氧化剂是___________ 。
②用单线桥标出电子转移方向和数目:_________
2NaIO3+5NaHSO3=3NaHSO4+2Na2SO4+I2+H2O
(3)已知:2H2S+SO2=3S+2H2O
①若有4个H2S分子参加反应,电子转移的数目为___________ 。
②氧化产物与还原产物的质量比为___________ 。
(1)已知:3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O。
①NO是
②若反应中有64g铜溶解,则被还原的HNO3的质量为
(2)智利硝石矿层中含有碘酸钠,可用亚硫酸氢钠与其反应来制备单质碘,其化学方程式为:2NaIO3+5NaHSO3=3NaHSO4+2Na2SO4+I2+H2O
①氧化剂是
②用单线桥标出电子转移方向和数目:
2NaIO3+5NaHSO3=3NaHSO4+2Na2SO4+I2+H2O
(3)已知:2H2S+SO2=3S+2H2O
①若有4个H2S分子参加反应,电子转移的数目为
②氧化产物与还原产物的质量比为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐2】氯气的实验室制法有多种,其中一种可以用重铬酸钾和浓盐酸制取。其变化可表述为:K2Cr2O7+14HCl (浓)=2KCl+2CrCl3+3Cl2 ↑+7H2O。
(1)请标出上述方程式的电子转移方向和数目__________ 。
(2)上述反应中被还原的元素为________ 。
(3)氧化产物与还原产物的物质的量之比为___________ 。
(4)浓盐酸在反应中显示出来的性质是________________ 。
(5)若有14.7g K2Cr2O7 发生上述反应,则转移的电子数为_____ 个, 产生的气体在标准状况下的体积为________ L。
(1)请标出上述方程式的电子转移方向和数目
(2)上述反应中被还原的元素为
(3)氧化产物与还原产物的物质的量之比为
(4)浓盐酸在反应中显示出来的性质是
(5)若有14.7g K2Cr2O7 发生上述反应,则转移的电子数为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐3】无机化合物 A 和 NaH 都是重要的还原剂,遇水都强烈反应。一定条件下,2.4g NaH 与气体 B 反应生成 3.9g 化合物 A 和 2.24L(已折算成标准状况)的 H2。已知气体 B 可使湿润红色石蕊试纸变蓝。请回答下列问题:
(1)B 的化学式是_____ 。
(2)NaH 与气体 B 反应生成化合物 A 的化学方程式_____ 。该反应中 A 是_____ 。
A.氧化产物 B.还原产物 C.既不是氧化产物也不是还原产物
(3)0.1molA 与足量盐酸发生非氧化还原反应最多消耗 HCl_____ mol
(4)在高温下氢化钠(NaH)可将四氯化钛(TiC14)还原成金属钛,同时得到混合气体, 测得其平均摩尔质量为 25 g/mol,写出该反应的化学方程式_____ 。
(1)B 的化学式是
(2)NaH 与气体 B 反应生成化合物 A 的化学方程式
A.氧化产物 B.还原产物 C.既不是氧化产物也不是还原产物
(3)0.1molA 与足量盐酸发生非氧化还原反应最多消耗 HCl
(4)在高温下氢化钠(NaH)可将四氯化钛(TiC14)还原成金属钛,同时得到混合气体, 测得其平均摩尔质量为 25 g/mol,写出该反应的化学方程式
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】计算
(1)已知酸性条件下, 可将
可将 还原为
还原为 。将标准状况下
。将标准状况下 的
的 气体通入足量酸性
气体通入足量酸性 溶液中,
溶液中,
①写出该反应的离子方程式______ 。
②被还原的 的质量为
的质量为______ 。
(2)为了检验某含有 杂质的
杂质的 样品的纯度,现将
样品的纯度,现将 样品充分加热,当固体质量不再变化时,再次称量固体质量为
样品充分加热,当固体质量不再变化时,再次称量固体质量为 ,则该样品的纯度(质量分数)为
,则该样品的纯度(质量分数)为______ (用含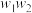 的代数式来表示)。
的代数式来表示)。
(3)有一块表面氧化成氧化钠的金属钠,总质量为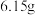 ,投入到足量水中,待充分反应后收集到氢气
,投入到足量水中,待充分反应后收集到氢气 (标准状况下),求未被氧化前金属钠质量是多少?写出计算过程
(标准状况下),求未被氧化前金属钠质量是多少?写出计算过程_____ 。
(1)已知酸性条件下,
 可将
可将 还原为
还原为 。将标准状况下
。将标准状况下 的
的 气体通入足量酸性
气体通入足量酸性 溶液中,
溶液中,①写出该反应的离子方程式
②被还原的
 的质量为
的质量为(2)为了检验某含有
 杂质的
杂质的 样品的纯度,现将
样品的纯度,现将 样品充分加热,当固体质量不再变化时,再次称量固体质量为
样品充分加热,当固体质量不再变化时,再次称量固体质量为 ,则该样品的纯度(质量分数)为
,则该样品的纯度(质量分数)为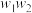 的代数式来表示)。
的代数式来表示)。(3)有一块表面氧化成氧化钠的金属钠,总质量为
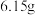 ,投入到足量水中,待充分反应后收集到氢气
,投入到足量水中,待充分反应后收集到氢气 (标准状况下),求未被氧化前金属钠质量是多少?写出计算过程
(标准状况下),求未被氧化前金属钠质量是多少?写出计算过程
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】双氧水是一种重要的氧化剂、漂白剂和消毒剂。生产双氧水常采用蒽醌法。双氧水浓度可在酸性条件下用KMnO4溶液测定,该反应的离子方程式为_________________________ ,双氧水的质量分数为27.5%(密度为1.10 g·cm-3),其浓度为________ 。
您最近一年使用:0次
【推荐3】通过下列步骤可以测定金属锡样品的纯度:
步骤1:将样品溶于盐酸中,将Sn全部转化为SnCl2;
步骤2:加入过量的FeCl3溶液,将SnCl2全部转化为SnCl4;
步骤3:用已知浓度的K2Cr2O7溶液滴定生成的Fe2+,发生的反应为6FeCl2+K2Cr2O7+14HCl=6FeCl3+2KCl+2CrCl3+7H2O。
现有金属锡样品0.613 g,经上述各步反应后,共用去0.100 mol•L-1K2Cr2O7溶液16.00 mL。
(1)步骤2中发生反应的化学方程式为_____ 。
(2)求样品中锡的质量分数_____ (假定杂质不参加反应)。
步骤1:将样品溶于盐酸中,将Sn全部转化为SnCl2;
步骤2:加入过量的FeCl3溶液,将SnCl2全部转化为SnCl4;
步骤3:用已知浓度的K2Cr2O7溶液滴定生成的Fe2+,发生的反应为6FeCl2+K2Cr2O7+14HCl=6FeCl3+2KCl+2CrCl3+7H2O。
现有金属锡样品0.613 g,经上述各步反应后,共用去0.100 mol•L-1K2Cr2O7溶液16.00 mL。
(1)步骤2中发生反应的化学方程式为
(2)求样品中锡的质量分数
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】化学需氧量(COD)是衡量水质的重要指标之一。COD 是指在特定条件下用一种强氧化 剂(如 KMnO4)定量地氧化水体中的还原性物质所消耗的氧化剂的量(折算为氧化能力相当的O2 质量,单位:mg·L-1)。其测定过程如下: 取 100.0mL 水样,用硫酸酸化,加入 10.0 mL 0.002000mol·L-1 KMnO4溶液,充分作用后,再加入 10.0mL 0.005000mol·L-1 溶液。用 0.002000mol·L-1 KMnO4溶液滴定,滴定终点时消耗 6.50mL。
溶液。用 0.002000mol·L-1 KMnO4溶液滴定,滴定终点时消耗 6.50mL。
已知:2MnO +5
+5 +16H+=2Mn2++10CO2↑+8H2O
+16H+=2Mn2++10CO2↑+8H2O
(1)1 mol KMnO4 的氧化能力与_____ g O2 的氧化能力相当(作氧化剂时转移的电子数相同)。
(2)该水样的 COD 值是_____ mg·L-1 (保留小数点后一位)。
 溶液。用 0.002000mol·L-1 KMnO4溶液滴定,滴定终点时消耗 6.50mL。
溶液。用 0.002000mol·L-1 KMnO4溶液滴定,滴定终点时消耗 6.50mL。已知:2MnO
 +5
+5 +16H+=2Mn2++10CO2↑+8H2O
+16H+=2Mn2++10CO2↑+8H2O(1)1 mol KMnO4 的氧化能力与
(2)该水样的 COD 值是
您最近一年使用:0次
【推荐2】高锰酸钾是一种典型的强氧化剂。
(1)在用 KMnO4 酸性溶液处理固体 Cu2S 时,发生的反应如下:8MnO4-+5Cu2S+44H+=10Cu2++5SO2↑+8Mn2++22H2O
①还原产物为_____ 。
②被氧化的元素是_____
③氧化剂与还原剂的物质的量之比为_____
④每生成 2.24 L(标况下)SO2,转移电子数目是_____
(2)用 KMnO4 酸性溶液处理固体 CuS 时,也可将 CuS 反应成 Cu2+和 SO2。写出该离子反应方程式_____
(3)15.8g KMnO4,加热分解后剩余固体 15.0 g。该剩余固体与足量的浓盐酸在加热条件下充分反应,生成单质气体 A,产物中锰元素以 Mn2+存在,则气体 A 的物质的量为_____ mol。
(1)在用 KMnO4 酸性溶液处理固体 Cu2S 时,发生的反应如下:8MnO4-+5Cu2S+44H+=10Cu2++5SO2↑+8Mn2++22H2O
①还原产物为
②被氧化的元素是
③氧化剂与还原剂的物质的量之比为
④每生成 2.24 L(标况下)SO2,转移电子数目是
(2)用 KMnO4 酸性溶液处理固体 CuS 时,也可将 CuS 反应成 Cu2+和 SO2。写出该离子反应方程式
(3)15.8g KMnO4,加热分解后剩余固体 15.0 g。该剩余固体与足量的浓盐酸在加热条件下充分反应,生成单质气体 A,产物中锰元素以 Mn2+存在,则气体 A 的物质的量为
您最近一年使用:0次

 和
和 ,二者体积比为
,二者体积比为

