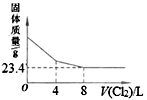
将某NaBr和NaI固体混合物溶于水配成的400mL溶液并等分成二份。取一份,在其中滴加250mLAgNO3溶液时,恰好完全转化为沉淀。另一份中通入Cl2,充分反应后将所得的溶液蒸干、灼烧、冷却、称量。称量固体的质量与通入Cl2的体积关系如图所示。
请计算:
(1)硝酸银溶液的浓度c(AgNO3)=____ mol·L-1。
(2)原混合物中m(NaBr):m(NaI)=____ 。

请计算:
(1)硝酸银溶液的浓度c(AgNO3)=
(2)原混合物中m(NaBr):m(NaI)=
更新时间:2017-08-17 23:54:18
|
相似题推荐
计算题
|
适中
(0.65)
名校
【推荐1】现有一由铝、铁混合而成的金属粉末,与足量的稀硫酸充分反应后生成氢气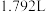 (标准状况下),若该混合粉末与足量的氯气充分反应后得到固体物
(标准状况下),若该混合粉末与足量的氯气充分反应后得到固体物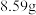 (已知铝、铁与氯气反应生成
(已知铝、铁与氯气反应生成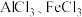 )。计算该混合粉末中铝、铁的质量分别是
)。计算该混合粉末中铝、铁的质量分别是_______ 、_______ 。
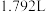 (标准状况下),若该混合粉末与足量的氯气充分反应后得到固体物
(标准状况下),若该混合粉末与足量的氯气充分反应后得到固体物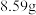 (已知铝、铁与氯气反应生成
(已知铝、铁与氯气反应生成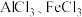 )。计算该混合粉末中铝、铁的质量分别是
)。计算该混合粉末中铝、铁的质量分别是
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐2】氯及其化合物是中学化学中的重要研究对象。
(1)写出实验室中制取氯气的离子方程式___ ;
(2)实验室也可以利用如下反应制取氯气:KClO3+6HCl(浓)→KCl+3Cl2↑+3H2O。若制取标准状况下6.72L氯气,反应过程中转移电子的物质的量为___ ;
(3)某同学用排空气法收集一瓶氯气并进行氯气与铁反应的实验:取一根细铁丝,用砂纸将铁丝擦至光亮,用坩埚钳夹住,在酒精灯上烧至红热,铁丝保持红热,然后立即伸入充满氯气的集气瓶中,观察到的现象是___ 。向反应后的集气瓶中加入适量的蒸馏水,振荡,观察到的现象是___ 。
(1)写出实验室中制取氯气的离子方程式
(2)实验室也可以利用如下反应制取氯气:KClO3+6HCl(浓)→KCl+3Cl2↑+3H2O。若制取标准状况下6.72L氯气,反应过程中转移电子的物质的量为
(3)某同学用排空气法收集一瓶氯气并进行氯气与铁反应的实验:取一根细铁丝,用砂纸将铁丝擦至光亮,用坩埚钳夹住,在酒精灯上烧至红热,铁丝保持红热,然后立即伸入充满氯气的集气瓶中,观察到的现象是
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐1】市售铁强化盐中铁含量测定。
已知:①铁强化盐中含有NaCl、KIO3、NaFeY,其中n(KIO3):n(NaFeY)=1:50,
②I2+2S2O =2I-+S4O
=2I-+S4O
称取m g样品,加稀硫酸溶解后配成100 mL溶液。取出10 mL,加入稍过量的KI溶液,充分反应后,滴入淀粉溶液,用c mol/L Na2S2O3标准溶液滴定,重复操作2~3次,消耗Na2S2O3标准溶液平均值为V mL。
(1)I-除了与Fe3+反应外,还可发生的反应的离子方程式为___________ 。
(2)样品中铁元素的质量分数为___________ (列出式子即可)。
已知:①铁强化盐中含有NaCl、KIO3、NaFeY,其中n(KIO3):n(NaFeY)=1:50,
②I2+2S2O
 =2I-+S4O
=2I-+S4O
称取m g样品,加稀硫酸溶解后配成100 mL溶液。取出10 mL,加入稍过量的KI溶液,充分反应后,滴入淀粉溶液,用c mol/L Na2S2O3标准溶液滴定,重复操作2~3次,消耗Na2S2O3标准溶液平均值为V mL。
(1)I-除了与Fe3+反应外,还可发生的反应的离子方程式为
(2)样品中铁元素的质量分数为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】已知HCN有剧毒;HCN、HOCN中N元素的化合价相同。
a.碳与镁形成的1mol化合物Q与水反应,生成2molMg(OH)2和1mol烃,该烃分子中碳氢质量比为9:1, Q与水反应的化学方程式为__________ 。
b.NaCN超标的电镀废水可用两段氧化法处理:
①.NaCN与NaClO反应,生成NaOCN和NaCl
②.NaOCN与NaClO反应,生成Na2CO3、CO2、NaCl和N2
完成下列填空:
①写出第二次氧化时发生反应的离子方程式__________________________
②(CN)2与Cl2的化学性质相似。(CN)2与NaOH溶液反应生成_________ 和H2O。
③处理200 m3含NaCN 10.3 mg/L的废水,实际至少需NaClO___ g(实际用量应为理论值的4倍),才能使NaCN含量低于0.5 mg/L,达到排放标准。
a.碳与镁形成的1mol化合物Q与水反应,生成2molMg(OH)2和1mol烃,该烃分子中碳氢质量比为9:1, Q与水反应的化学方程式为
b.NaCN超标的电镀废水可用两段氧化法处理:
①.NaCN与NaClO反应,生成NaOCN和NaCl
②.NaOCN与NaClO反应,生成Na2CO3、CO2、NaCl和N2
完成下列填空:
①写出第二次氧化时发生反应的离子方程式
②(CN)2与Cl2的化学性质相似。(CN)2与NaOH溶液反应生成
③处理200 m3含NaCN 10.3 mg/L的废水,实际至少需NaClO
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐3】下表是某食用碘盐包装袋上的部分说明:
请回答下列问题:
(1)下列说法正确的是___________ 。
A.碘酸钾易挥发 B.高温会导致碘的损失
C.用淀粉就能直接检验碘盐中的碘酸钾 D.碘酸钾可氧化氯化钠
(2)碘酸钾与碘化钾在酸性条件下发生如下反应:KIO3+KI+H2SO4→K2SO4+I2+H2O(未配平),该化学方程式配平后系数依次为___________________ 。
w.该反应的还原剂为_____ ;1mol KIO3完全反应转移的电子总数为______ 。
(3)碘不能多也不能少。已知:I2+2S2O32-=2I-+S4O62-,我校化学兴趣小组测定某食用碘盐中碘的含量。其步骤为:
①准确称取w g食盐,加适量蒸馏水使其完全溶解;②用稀硫酸酸化所得溶液,加入足量KI溶液,使KIO3与KI反应完全;③以淀粉为指示剂,逐滴加入物质的量浓度为1.0×10-3mol·L-1的Na2S2O3溶液20.0mL,恰好反应完全。则所测盐中碘的含量是(以含w的代数式表示)_________ mg/kg。
| 配 料 | 食盐、碘酸钾、抗结剂 |
| 碘含量 | 35±15mg/kg |
| 储藏方法 | 密封、避光、防潮 |
| 食用方法 | 烹饪时,待食品熟后加入碘盐 |
(1)下列说法正确的是
A.碘酸钾易挥发 B.高温会导致碘的损失
C.用淀粉就能直接检验碘盐中的碘酸钾 D.碘酸钾可氧化氯化钠
(2)碘酸钾与碘化钾在酸性条件下发生如下反应:KIO3+KI+H2SO4→K2SO4+I2+H2O(未配平),该化学方程式配平后系数依次为
w.该反应的还原剂为
(3)碘不能多也不能少。已知:I2+2S2O32-=2I-+S4O62-,我校化学兴趣小组测定某食用碘盐中碘的含量。其步骤为:
①准确称取w g食盐,加适量蒸馏水使其完全溶解;②用稀硫酸酸化所得溶液,加入足量KI溶液,使KIO3与KI反应完全;③以淀粉为指示剂,逐滴加入物质的量浓度为1.0×10-3mol·L-1的Na2S2O3溶液20.0mL,恰好反应完全。则所测盐中碘的含量是(以含w的代数式表示)
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】碱式碳酸铝镁[MgaAlb(OH)c(CO3)d·xH2O]常用作塑料阻燃剂。
(2)MgaAlb(OH)c(CO3)d·xH2O中a、b、c、d的代数关系式为___________________________ 。
(3)为确定碱式碳酸铝镁的组成,进行如下实验:
①准确称取3.390 g样品与足量稀盐酸充分反应,生成CO2 0.560 L(已换算成标准状况下)。
②另取一定量样品在空气中加热,样品的固体残留率[(固体样品的剩余质量/固体样品的起始质量)×100%]随温度的变化如下图所示(样品在270 ℃时已完全失去结晶水,600 ℃以上残留固体为金属氧化物的混合物)。
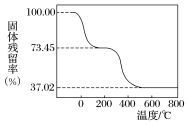
根据以上实验数据计算碱式碳酸铝镁样品中的n(OH-)∶n(CO )(写出计算过程)
)(写出计算过程) ____________ 。
(2)MgaAlb(OH)c(CO3)d·xH2O中a、b、c、d的代数关系式为
(3)为确定碱式碳酸铝镁的组成,进行如下实验:
①准确称取3.390 g样品与足量稀盐酸充分反应,生成CO2 0.560 L(已换算成标准状况下)。
②另取一定量样品在空气中加热,样品的固体残留率[(固体样品的剩余质量/固体样品的起始质量)×100%]随温度的变化如下图所示(样品在270 ℃时已完全失去结晶水,600 ℃以上残留固体为金属氧化物的混合物)。

根据以上实验数据计算碱式碳酸铝镁样品中的n(OH-)∶n(CO
 )(写出计算过程)
)(写出计算过程)
您最近一年使用:0次
【推荐2】取6.32 g KMnO4固体,加热一段时间后,剩余固体5.84 g。该剩余固体与足量的浓盐酸在加热条件下充分反应,生成单质气体A,产物中Mn元素以Mn2+存在。
请计算:
(1)KMnO4的分解率:_______ 。
(2)气体A的物质的量:_______ 。
请计算:
(1)KMnO4的分解率:
(2)气体A的物质的量:
您最近一年使用:0次




