下表是某食用碘盐包装袋上的部分说明:
请回答下列问题:
(1)下列说法正确的是___________ 。
A.碘酸钾易挥发 B.高温会导致碘的损失
C.用淀粉就能直接检验碘盐中的碘酸钾 D.碘酸钾可氧化氯化钠
(2)碘酸钾与碘化钾在酸性条件下发生如下反应:KIO3+KI+H2SO4→K2SO4+I2+H2O(未配平),该化学方程式配平后系数依次为___________________ 。
w.该反应的还原剂为_____ ;1mol KIO3完全反应转移的电子总数为______ 。
(3)碘不能多也不能少。已知:I2+2S2O32-=2I-+S4O62-,我校化学兴趣小组测定某食用碘盐中碘的含量。其步骤为:
①准确称取w g食盐,加适量蒸馏水使其完全溶解;②用稀硫酸酸化所得溶液,加入足量KI溶液,使KIO3与KI反应完全;③以淀粉为指示剂,逐滴加入物质的量浓度为1.0×10-3mol·L-1的Na2S2O3溶液20.0mL,恰好反应完全。则所测盐中碘的含量是(以含w的代数式表示)_________ mg/kg。
| 配 料 | 食盐、碘酸钾、抗结剂 |
| 碘含量 | 35±15mg/kg |
| 储藏方法 | 密封、避光、防潮 |
| 食用方法 | 烹饪时,待食品熟后加入碘盐 |
(1)下列说法正确的是
A.碘酸钾易挥发 B.高温会导致碘的损失
C.用淀粉就能直接检验碘盐中的碘酸钾 D.碘酸钾可氧化氯化钠
(2)碘酸钾与碘化钾在酸性条件下发生如下反应:KIO3+KI+H2SO4→K2SO4+I2+H2O(未配平),该化学方程式配平后系数依次为
w.该反应的还原剂为
(3)碘不能多也不能少。已知:I2+2S2O32-=2I-+S4O62-,我校化学兴趣小组测定某食用碘盐中碘的含量。其步骤为:
①准确称取w g食盐,加适量蒸馏水使其完全溶解;②用稀硫酸酸化所得溶液,加入足量KI溶液,使KIO3与KI反应完全;③以淀粉为指示剂,逐滴加入物质的量浓度为1.0×10-3mol·L-1的Na2S2O3溶液20.0mL,恰好反应完全。则所测盐中碘的含量是(以含w的代数式表示)
10-11高三·河南信阳·阶段练习 查看更多[1]
(已下线)2012届河南省信阳市高中毕业班第一次调研考试化学试卷
更新时间:2016-12-09 02:11:18
|
相似题推荐
计算题
|
适中
(0.65)
名校
【推荐1】完成下列有关物质的量的相关计算
(1)等质量的NH3和CH4,分子个数比为___________ ,同温同压下,等体积的CO2和O2密度比为___________ 。
(2)S燃烧时有SO2生成,其原理为:S+O2 SO2,若转移2.408×1024个电子,则生成的SO2的物质的量是
SO2,若转移2.408×1024个电子,则生成的SO2的物质的量是___________ 。
(3)在标准状况下,224mL CO2恰好与20mL NaOH溶液反应生成NaHCO3,则此NaOH溶液中n(NaOH)为___________ 。
(4)氢气是一种清洁能源,甲烷制氢的化学方程式为CH4+O2=CO2+2H2.在标准状况下,CH4与一定量的O2中恰好完全反应,反应后测得生成物的体积是672mL,则生成H2___________ mol,消耗的O2的体积是___________ 。
(1)等质量的NH3和CH4,分子个数比为
(2)S燃烧时有SO2生成,其原理为:S+O2
 SO2,若转移2.408×1024个电子,则生成的SO2的物质的量是
SO2,若转移2.408×1024个电子,则生成的SO2的物质的量是(3)在标准状况下,224mL CO2恰好与20mL NaOH溶液反应生成NaHCO3,则此NaOH溶液中n(NaOH)为
(4)氢气是一种清洁能源,甲烷制氢的化学方程式为CH4+O2=CO2+2H2.在标准状况下,CH4与一定量的O2中恰好完全反应,反应后测得生成物的体积是672mL,则生成H2
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】在反应:3BrF3+5H2O= HBrO3+Br2+9HF十O2中(F为-1价)
(1)此反应中被氧化的元素是_________ 、被还原的元素是_____________ 。
(2)当有5mol水参加反应时,被氧化的水的物质的量为________ ,被还原的BrF3的物质的量为_________ 。
(1)此反应中被氧化的元素是
(2)当有5mol水参加反应时,被氧化的水的物质的量为
您最近一年使用:0次
【推荐3】HIO4主要以H5IO6形式存在,H5IO6是白色晶体,易溶于水,具有很强的氧化性,在强酸溶液中能氧化Mn2+。
(1)请完成并配平下列离子反应。
__________ Mn2++________ H5IO6
__________  +
+________ 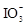 +
+________ H++________
(2)根据以上离子方程式判断H5IO6是________ 电离物质(填“易”或“难”)。
(3)上述反应,被氧化的元素是________ (填元素符号),当1 mol Mn2+参加反应时,转移电子的物质的量为________ 。
(1)请完成并配平下列离子反应。

 +
+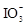 +
+(2)根据以上离子方程式判断H5IO6是
(3)上述反应,被氧化的元素是
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐1】已知HCN有剧毒;HCN、HOCN中N元素的化合价相同。
a.碳与镁形成的1mol化合物Q与水反应,生成2molMg(OH)2和1mol烃,该烃分子中碳氢质量比为9:1, Q与水反应的化学方程式为__________ 。
b.NaCN超标的电镀废水可用两段氧化法处理:
①.NaCN与NaClO反应,生成NaOCN和NaCl
②.NaOCN与NaClO反应,生成Na2CO3、CO2、NaCl和N2
完成下列填空:
①写出第二次氧化时发生反应的离子方程式__________________________
②(CN)2与Cl2的化学性质相似。(CN)2与NaOH溶液反应生成_________ 和H2O。
③处理200 m3含NaCN 10.3 mg/L的废水,实际至少需NaClO___ g(实际用量应为理论值的4倍),才能使NaCN含量低于0.5 mg/L,达到排放标准。
a.碳与镁形成的1mol化合物Q与水反应,生成2molMg(OH)2和1mol烃,该烃分子中碳氢质量比为9:1, Q与水反应的化学方程式为
b.NaCN超标的电镀废水可用两段氧化法处理:
①.NaCN与NaClO反应,生成NaOCN和NaCl
②.NaOCN与NaClO反应,生成Na2CO3、CO2、NaCl和N2
完成下列填空:
①写出第二次氧化时发生反应的离子方程式
②(CN)2与Cl2的化学性质相似。(CN)2与NaOH溶液反应生成
③处理200 m3含NaCN 10.3 mg/L的废水,实际至少需NaClO
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐2】研究物质性质及物质转化具有重要的价值。回答下列问题:
(1)已知常温下,在溶液中可发生如下反应。
① ;②
;② 。
。
反应①中还原剂为_____ ;反应②中每消耗1个 ,转移
,转移_____ 个电子。
(2)某反应的反应物与生成物有 ,已知氧化性:
,已知氧化性: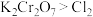 ,写出并配平该化学方程式:
,写出并配平该化学方程式:_____ 。
(3)按如图所示操作,充分反应后。

①试管Ⅰ中发生反应的化学方程式为_____ ;试管Ⅱ中铜丝上观察到的现象是_____ 。
②结合Ⅰ、Ⅱ实验现象可知 的氧化性由强到弱的顺序为
的氧化性由强到弱的顺序为_____ 。
(1)已知常温下,在溶液中可发生如下反应。
①
 ;②
;② 。
。反应①中还原剂为
 ,转移
,转移(2)某反应的反应物与生成物有
 ,已知氧化性:
,已知氧化性: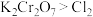 ,写出并配平该化学方程式:
,写出并配平该化学方程式:(3)按如图所示操作,充分反应后。

①试管Ⅰ中发生反应的化学方程式为
②结合Ⅰ、Ⅱ实验现象可知
 的氧化性由强到弱的顺序为
的氧化性由强到弱的顺序为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】电解饱和食盐水可以产生氯气、氢气和氢氧化钠,氯气与石灰乳反应可制漂白粉:2Cl2 +2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O。
(1)请写出电解饱和食盐水的化学方程式,若为氧化还原反应则用单线桥标出电子转移的方向和数目_______________ 。
(2)若电解饱和食盐水时消耗NaCl 58.5g,试计算理论上最多可得到氯气的体积(标准状况)为多少__________ ?
(3)若将1mol氯气通入石灰乳中,理论上可得到Ca(ClO)2的质量是多少_______ ?
(1)请写出电解饱和食盐水的化学方程式,若为氧化还原反应则用单线桥标出电子转移的方向和数目
(2)若电解饱和食盐水时消耗NaCl 58.5g,试计算理论上最多可得到氯气的体积(标准状况)为多少
(3)若将1mol氯气通入石灰乳中,理论上可得到Ca(ClO)2的质量是多少
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】世界卫生组织建议一般健康人群的每天应食用不超过6克盐。下图为某加碘盐的规格标签。
(1)专家建议烹饪食物时,应在最后加碘盐。你认为可能的原因是什么_____ ?
(2)成年人每天需摄入0.15~0.20mg碘元素才能满足人体需要。若每天食用6克这种碘盐,那么你认为标签中的KIO3含量应为以下哪个选项___________ ?
a.10~20mg·kg-1 b.20~30mg·kg-1 c.40~50mg·kg-1
(3)黄花鱼的碘含量为0.058毫克/千克。若一个成年人只食用黄花鱼,需达到多少的量才能满足碘元素的摄入_____ ?这种方法是否合适_____ ? (不考虑从其他途径摄入的碘元素)
| 配料 | 氯化钠(NaCl)、碘酸钾(KIO3) |
| KIO3含量 | |
| 保质期 | 18个月 |
| 食用方法 | 勿长时间炖炒 |
| 贮存方法 | 避光、避热、密封、防潮 |
(1)专家建议烹饪食物时,应在最后加碘盐。你认为可能的原因是什么
(2)成年人每天需摄入0.15~0.20mg碘元素才能满足人体需要。若每天食用6克这种碘盐,那么你认为标签中的KIO3含量应为以下哪个选项
a.10~20mg·kg-1 b.20~30mg·kg-1 c.40~50mg·kg-1
(3)黄花鱼的碘含量为0.058毫克/千克。若一个成年人只食用黄花鱼,需达到多少的量才能满足碘元素的摄入
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】市售铁强化盐中铁含量测定。
已知:①铁强化盐中含有NaCl、KIO3、NaFeY,其中n(KIO3):n(NaFeY)=1:50,
②I2+2S2O =2I-+S4O
=2I-+S4O
称取m g样品,加稀硫酸溶解后配成100 mL溶液。取出10 mL,加入稍过量的KI溶液,充分反应后,滴入淀粉溶液,用c mol/L Na2S2O3标准溶液滴定,重复操作2~3次,消耗Na2S2O3标准溶液平均值为V mL。
(1)I-除了与Fe3+反应外,还可发生的反应的离子方程式为___________ 。
(2)样品中铁元素的质量分数为___________ (列出式子即可)。
已知:①铁强化盐中含有NaCl、KIO3、NaFeY,其中n(KIO3):n(NaFeY)=1:50,
②I2+2S2O
 =2I-+S4O
=2I-+S4O
称取m g样品,加稀硫酸溶解后配成100 mL溶液。取出10 mL,加入稍过量的KI溶液,充分反应后,滴入淀粉溶液,用c mol/L Na2S2O3标准溶液滴定,重复操作2~3次,消耗Na2S2O3标准溶液平均值为V mL。
(1)I-除了与Fe3+反应外,还可发生的反应的离子方程式为
(2)样品中铁元素的质量分数为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】为了防治环境污染并对尾气进行综合利用,某硫酸厂用氨水吸收尾气中的SO2,再向吸收液中加入浓硫酸,以制取高浓度的SO2及(NH4)2SO4和NH4HSO4固体。
为了测定上述(NH4)2SO4和NH4HSO4固体混合物的组成,现称取该样品四份,分别加入相同浓度的NaOH溶液各40.00mL,加热至120℃左右,使氨气全部逸出[(NH4)2SO4和NH4HSO4的分解温度均高于200℃],测得有关实验数据如下(标准状况):
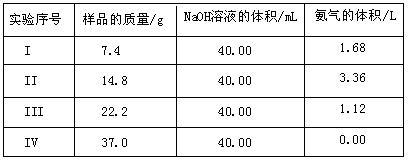
(1)实验过程中有关反应的离子方程式为______________________________ ;
(2)由I组数据直接推测:标准状况下3.7g样品进行同样实验时,生成氨气的体积为______ L;
(3)试计算该混合物中(NH4)2SO4和NH4HSO4的物质的量之比_________ ;
(4)欲计算该NaOH溶液的物质的量浓度应选择第_________ 组数据,由此求得NaOH溶液的物质的量浓度为_____________ 。
为了测定上述(NH4)2SO4和NH4HSO4固体混合物的组成,现称取该样品四份,分别加入相同浓度的NaOH溶液各40.00mL,加热至120℃左右,使氨气全部逸出[(NH4)2SO4和NH4HSO4的分解温度均高于200℃],测得有关实验数据如下(标准状况):

(1)实验过程中有关反应的离子方程式为
(2)由I组数据直接推测:标准状况下3.7g样品进行同样实验时,生成氨气的体积为
(3)试计算该混合物中(NH4)2SO4和NH4HSO4的物质的量之比
(4)欲计算该NaOH溶液的物质的量浓度应选择第
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】在200ml 0.5 mol·L-1的Al2(SO4)3溶液中,Al3+的物质的量浓度是 ,Al3+的质量是 ,SO42-的个数是 。
您最近一年使用:0次



