实验是进行化学研究的重要环节,下列有关化学实验的说法错误的是
| A.用酒精灯外焰加热铝箔,铝箔熔化但不滴落,说明Al2O3的熔点比Al的熔点高 |
B.可用勒夏特列原理解释2NO2(g) N2O4(g)体系加压后颜色变深 N2O4(g)体系加压后颜色变深 |
| C.用酸性KMnO4溶液验证草酸的还原性 |
| D.向滴有KSCN的FeCl3溶液中加入NaOH溶液以研究反应物浓度对化学平衡的影响 |
更新时间:2017-09-02 13:15:48
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】下列叙述Ⅰ和叙述Ⅱ均正确并且有因果关系的是( )
| 选项 | 叙述Ⅰ | 叙述Ⅱ |
| A | S2-具有还原性 | S2-能除去工业废水中的Cu2+等重金属离子 |
| B | NH3具有还原性 | 蘸有浓硝酸的玻璃棒靠近浓氨水时冒白烟 |
| C | 熔融状态的Al2O3中有自由移动的Al3+和O2- | 电解熔融状态的Al2O3制备Al |
| D | SO2具有漂白性 | SO2能使紫色石蕊试液先变红后褪色 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】提纯下列物质(括号内物质为杂质)选用的试剂和方法都正确的是
| 物质 | 除杂试剂 | 方法 | |
| A | FeCl3溶液(FeCl2) | Cl2 | —— |
| B | FeCl2溶液(FeCl3) | 足量铜粉 | 过滤 |
| C | KNO3(KCl) | —— | 蒸发结晶 |
| D | Al2O3(Fe2O3) | NaOH溶液 | 过滤 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列事实不能用勒夏特列原理解释的是
| A.工业合成氨中,将氨气液化分离以提高氨气产率 |
| B.开启啤酒瓶后,瓶中马上泛起大量泡沫 |
| C.实验室中常用排饱和食盐水的方法收集氯气 |
| D.盛有2mL5%H2O2溶液的试管中滴入1mL0.1mol·L-1FeCl3溶液,试管中迅速产生大量气泡 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】高中化学涉及的原理很多,掌握与应用好原理是学习好化学的理论基础。下列应用与对应原理不相符的是
| A.用CCl4 萃取碘水中的碘,应用了“相似相溶原理” |
B.反应2HI(g) H2(g)+ l2(g)达到平衡后,增大压强(减小体积),混合气体颜色加深,符合“平衡移动原理” H2(g)+ l2(g)达到平衡后,增大压强(减小体积),混合气体颜色加深,符合“平衡移动原理” |
| C.Fe的核外电子排布式:1s22s22p63s23p63d64s2,遵从“构造原理” |
D.3H2(g)+ N2(g) 2NH3(g) ΔH=-92.4 kJ·mol-1;既符合“质量守恒原理”也遵从“能量守恒原理” 2NH3(g) ΔH=-92.4 kJ·mol-1;既符合“质量守恒原理”也遵从“能量守恒原理” |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】已知: 在水溶液中以水合铁离子的形式存在,如
在水溶液中以水合铁离子的形式存在,如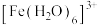 (几乎无色);
(几乎无色);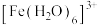 水解生成
水解生成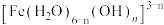 (黄色);
(黄色);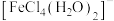 (黄色)。
(黄色)。
下列实验所得结论不正确 的是
注:加热为微热,忽略体积变化。
 在水溶液中以水合铁离子的形式存在,如
在水溶液中以水合铁离子的形式存在,如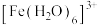 (几乎无色);
(几乎无色);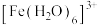 水解生成
水解生成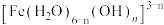 (黄色);
(黄色);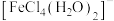 (黄色)。
(黄色)。下列实验所得结论
| ① | ② | ③ | ④ |
 0.1mol/L  溶液 溶液 |  酸化的0.1mol/L  溶液 溶液 | 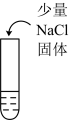 酸化的0.1mol/L  溶液 溶液 |  0.1mol/L  溶液 溶液 |
| 加热前溶液为浅黄色,加热后颜色变深 | 加热前溶液接近无色,加热后溶液颜色无明显变化 | 加入NaCl后,溶液立即变为黄色,加热后溶液颜色变深 | 加热前溶液为黄色,加热后溶液颜色变深 |
A.实验①中, 溶液显浅黄色原因是 溶液显浅黄色原因是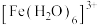 发生了水解反应 发生了水解反应 |
B.实验②中,酸化对 水解的影响程度大于温度的影响 水解的影响程度大于温度的影响 |
C.实验③中,存在可逆反应: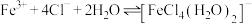 |
D.实验④,可证明升高温度, 水解平衡正向移动 水解平衡正向移动 |
您最近一年使用:0次
【推荐2】室温下,下列实验探究方案不能达到实验目的的是
| 选项 | 探究方案 | 实验目的 |
| A | 向2mL1mol·L-1CH3COOH溶液中滴加1mol·L-1Na2CO3溶液,观察现象 | 比较Ka(CH3COOH)和Ka1(H2CO3)的大小 |
| B | 向4mL0.1mol·L-1CuSO4溶液中滴加1mol·L-1氨水至沉淀溶解,再加入8mL95%乙醇,过滤 | 制备[Cu(NH3)4]SO4•H2O晶体 |
| C | 把两个体积相同、封装有等量NO2和N2O4混合气体的烧瓶分别同时浸泡在热水和冰水中,观察混合气体的颜色变化 | 探究温度对化学平衡的影响 |
| D | 向溶液X中滴加少量稀硝酸,然后滴入几滴Ba(NO3)2溶液,观察现象 | 检验溶液X是否含有SO |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次

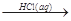

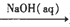

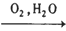
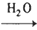 H2SiO3
H2SiO3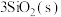
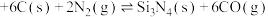
 。根据勒夏特列原理,该反应的合适条件应为
。根据勒夏特列原理,该反应的合适条件应为


