(1)在同温同压下,2gCO2的体积为1120mL,而2gA气体的体积为770mL,则气体A的摩尔质量为__________ mol/L。
(2)现有A、B、C三种化合物,各取40g相混合,完全反应后,得B 18g,C49g,还有D生成。已知D的式量为106。现将22gA和11gB混合反应,能生成D_____ mol。
(3)往硫酸铝铵【NH4Al(SO4)2】溶液中滴加Ba(OH)2溶液并加热,刚好使NH4+全部转化为NH3,写出反应的离子 方程式:________________________________________ 。
(2)现有A、B、C三种化合物,各取40g相混合,完全反应后,得B 18g,C49g,还有D生成。已知D的式量为106。现将22gA和11gB混合反应,能生成D
(3)往硫酸铝铵【NH4Al(SO4)2】溶液中滴加Ba(OH)2溶液并加热,刚好使NH4+全部转化为NH3,写出反应的
更新时间:2017-09-19 22:46:15
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】计算并填空:
(1)若某原子的摩尔质量是Mg/mol,则一个该原子的真实质量是___ g。
(2)CO和CO2的混合气体18g,完全燃烧后测得CO2体积为11.2L(标准状况):
①混合气体中CO的质量是___ g。
②混合气体中CO2在标准状况下的体积是___ L。
③混合气体在标准状况下的密度是___ g·L-1(精确到0.1)。
(1)若某原子的摩尔质量是Mg/mol,则一个该原子的真实质量是
(2)CO和CO2的混合气体18g,完全燃烧后测得CO2体积为11.2L(标准状况):
①混合气体中CO的质量是
②混合气体中CO2在标准状况下的体积是
③混合气体在标准状况下的密度是
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】化学计量在化学中占有重要地位。请回答下列问题:
(1)2019年1月21日13时42分,我国在酒泉卫星发射中心用长征十一号运载火箭成功发射了三颗卫星。长征系列运载火箭的燃料之一是肼( )。回答下列问题:
)。回答下列问题:
①肼的摩尔质量是_______ 。
②16g肼中含有氮原子的数目为_______ 。
③肼在氧气中燃烧生成 和
和 ,一定质量的肼燃烧后生成
,一定质量的肼燃烧后生成 和
和 的物质的量之比是
的物质的量之比是_______ 。每生成标准状况下44.8L的氮气,需要消耗肼的质量为_______ 。
(2)22.2g某二价金属氯化物(ACl2)中含有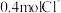 ,则A的相对原子质量是
,则A的相对原子质量是_______ ;ACl2的化学式是_______ 。
(3)在0.2L由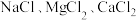 组成的混合液中,部分离子浓度大小如图所示。
组成的混合液中,部分离子浓度大小如图所示。
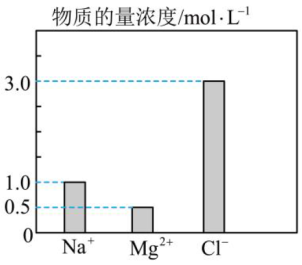
①该混合液中 的物质的量为
的物质的量为_______ mol,将该混合液加水稀释至体积为1L,稀释后溶液中 的物质的量浓度为
的物质的量浓度为_______ mol/L。
②向该稀释后的溶液中加入足量硝酸酸化的硝酸银溶液,可得到沉淀_______ mol。
(4)如图所示,气缸的总体积一定,内部被活塞隔成Ⅰ、Ⅱ两部分,活塞可以自由移动,也可以固定。0℃时向Ⅰ中充入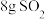 ,Ⅱ中充入
,Ⅱ中充入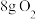 ,则当活塞不再移动时,Ⅰ、Ⅱ两部分体积比为
,则当活塞不再移动时,Ⅰ、Ⅱ两部分体积比为_______ 。

(1)2019年1月21日13时42分,我国在酒泉卫星发射中心用长征十一号运载火箭成功发射了三颗卫星。长征系列运载火箭的燃料之一是肼(
 )。回答下列问题:
)。回答下列问题:①肼的摩尔质量是
②16g肼中含有氮原子的数目为
③肼在氧气中燃烧生成
 和
和 ,一定质量的肼燃烧后生成
,一定质量的肼燃烧后生成 和
和 的物质的量之比是
的物质的量之比是(2)22.2g某二价金属氯化物(ACl2)中含有
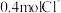 ,则A的相对原子质量是
,则A的相对原子质量是(3)在0.2L由
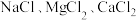 组成的混合液中,部分离子浓度大小如图所示。
组成的混合液中,部分离子浓度大小如图所示。
①该混合液中
 的物质的量为
的物质的量为 的物质的量浓度为
的物质的量浓度为②向该稀释后的溶液中加入足量硝酸酸化的硝酸银溶液,可得到沉淀
(4)如图所示,气缸的总体积一定,内部被活塞隔成Ⅰ、Ⅱ两部分,活塞可以自由移动,也可以固定。0℃时向Ⅰ中充入
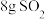 ,Ⅱ中充入
,Ⅱ中充入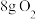 ,则当活塞不再移动时,Ⅰ、Ⅱ两部分体积比为
,则当活塞不再移动时,Ⅰ、Ⅱ两部分体积比为
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐3】完成下列填空。
(1)0.1molH2所含的氢原子数是___________ 个,标况下,2.24L氢气的质量是___________ 克。
(2)28克铁的物质的量是___________ ,含铁原子___________ 个。
(3)3.01×1023个二氧化碳分子的物质的量是___________ ,标况下的体积是___________ 。
(4)在标准状况下有:①6.72LCH4,②3.01×1023个HCl分子,③13.6gH2S,④0.2molNH3,用序号回答下列问题:
a.体积由大到小___________ ;
b.密度由大到小___________ ;
c.质量由大到小___________ ;
d.氢原子个数由大到小___________ 。
(1)0.1molH2所含的氢原子数是
(2)28克铁的物质的量是
(3)3.01×1023个二氧化碳分子的物质的量是
(4)在标准状况下有:①6.72LCH4,②3.01×1023个HCl分子,③13.6gH2S,④0.2molNH3,用序号回答下列问题:
a.体积由大到小
b.密度由大到小
c.质量由大到小
d.氢原子个数由大到小
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】(1)在标准状况下,CO和CO2的混合气体共39.2 L,质量为61 g,其中CO2为________ mol,该混合气体中CO 与CO2的密度之比为________ 。
(2)同温同压下,同体积的甲烷(CH4)和二氧化碳中,质量之比为__________ ,
(3)在同温、同压下,A容器中的H2与B容器中的NH3所含氢原子总数相等,则A与B的体积之比为________
(4)有K2SO4和Al2(SO4)3的混合溶液,已知其中Al3+的物质的量浓度为0.4 mol/L,SO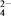 的物质的量浓度为0.7 mol/L,则此溶液中K+ 的物质的量浓度为
的物质的量浓度为0.7 mol/L,则此溶液中K+ 的物质的量浓度为________
(2)同温同压下,同体积的甲烷(CH4)和二氧化碳中,质量之比为
(3)在同温、同压下,A容器中的H2与B容器中的NH3所含氢原子总数相等,则A与B的体积之比为
(4)有K2SO4和Al2(SO4)3的混合溶液,已知其中Al3+的物质的量浓度为0.4 mol/L,SO
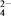 的物质的量浓度为0.7 mol/L,则此溶液中K+ 的物质的量浓度为
的物质的量浓度为0.7 mol/L,则此溶液中K+ 的物质的量浓度为
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】完成下列问题
(1)1 mol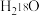 与1 mol
与1 mol 中子数之比为
中子数之比为_______ 。
(2)已知阴离子R2-的原子核内有n个中子,R原子的质量数为m,则w g R原子完全转化为R2-时,含有电子的物质的量是_______ 。
(1)1 mol
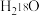 与1 mol
与1 mol 中子数之比为
中子数之比为(2)已知阴离子R2-的原子核内有n个中子,R原子的质量数为m,则w g R原子完全转化为R2-时,含有电子的物质的量是
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】I.根据物质的组成、结构、性质等进行分类,可预测物质的性质及变化。
现有下列九种物质:
①HCl气体 ②固体Cu ③乙醇 ④三氧化硫 ⑤熔融NaCl ⑥AlCl3固体 ⑦NH4Cl溶液 ⑧NaHCO3固体 ⑨硫酸钡固体。按照不同的依据对其进行分类:
(1)所给状态能导电的是_______ (填序号)。
(2)属于酸式盐的物质为________ (填序号),其电离方程式为_______ 。
(3)属于共价化合物的是________ (填序号)。
(4)属于酸的物质是______ (填序号),其电子式的形成过程__________ 。
II.物质的量是联系宏观和微观的桥梁:
(5)40.5g某金属氯化物MCl2中含0.6molCl-,则该氯化物的摩尔质量为________ 。
(6)标准状况下,与34g的H2S气体含相同H原子数的CH4的体积为_________ 。
(7)在同温同压下,等质量的CO和CO2.其体积之比为___________ 。
现有下列九种物质:
①HCl气体 ②固体Cu ③乙醇 ④三氧化硫 ⑤熔融NaCl ⑥AlCl3固体 ⑦NH4Cl溶液 ⑧NaHCO3固体 ⑨硫酸钡固体。按照不同的依据对其进行分类:
(1)所给状态能导电的是
(2)属于酸式盐的物质为
(3)属于共价化合物的是
(4)属于酸的物质是
II.物质的量是联系宏观和微观的桥梁:
(5)40.5g某金属氯化物MCl2中含0.6molCl-,则该氯化物的摩尔质量为
(6)标准状况下,与34g的H2S气体含相同H原子数的CH4的体积为
(7)在同温同压下,等质量的CO和CO2.其体积之比为
您最近半年使用:0次
填空题
|
适中
(0.64)
【推荐1】按要求写出下列反应方程式:
(1)金属铝与氢氧化钠溶液反应的离子方程式_______ ;
(2)铁与水蒸气在一定条件下反应的方程式_______ ;
(3)钠与水反应的离子方程式_______ ;
(1)金属铝与氢氧化钠溶液反应的离子方程式
(2)铁与水蒸气在一定条件下反应的方程式
(3)钠与水反应的离子方程式
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】H7N9型禽流感是一种新型禽流感,研究表明,该病毒对热敏感,煮沸2分钟以上即可失去活性,许多常用消毒药物如:高锰酸钾、漂白粉、氯气等,也都可以将该病毒杀灭。
(1)新制氯水中含有多种微粒,将紫色石蕊试液滴入氯水中,溶液显红色起作用的微粒是____ ;过一会儿,溶液颜色逐渐褪去,起作用的微粒是______ 。
(2)工业上制取漂白粉的反应方程式为:___________ 。
(3)已知高锰酸钾与浓盐酸混合能产生氯气,化学反应方程式为:2KMnO4 +16HCl 2MnCl2+2KCl+8H2O+5Cl2↑
2MnCl2+2KCl+8H2O+5Cl2↑
该反应中氧化剂为________ 。请用双线桥法表示电子转移的情况。_________________
(4)向漂白粉清液中滴加碳酸钠溶液,有白色沉淀生成,写出发生反应的离子方程式___ 。
(5)将过量氯气通入FeBr2溶液中,写出该反应的离子方程式__________ 。
(1)新制氯水中含有多种微粒,将紫色石蕊试液滴入氯水中,溶液显红色起作用的微粒是
(2)工业上制取漂白粉的反应方程式为:
(3)已知高锰酸钾与浓盐酸混合能产生氯气,化学反应方程式为:2KMnO4 +16HCl
 2MnCl2+2KCl+8H2O+5Cl2↑
2MnCl2+2KCl+8H2O+5Cl2↑该反应中氧化剂为
(4)向漂白粉清液中滴加碳酸钠溶液,有白色沉淀生成,写出发生反应的离子方程式
(5)将过量氯气通入FeBr2溶液中,写出该反应的离子方程式
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐3】亚砷酸(H3AsO3)可用于治疗急性早幼粒细胞白血病,可通过注射至血液的方式直接给药。医用的亚砷酸溶液可通过将As2O3溶于过量NaOH溶液后加稀硫酸配置。一般情况下,亚砷酸溶液中各种微粒的物质的量分数与pH的关系如图所示。
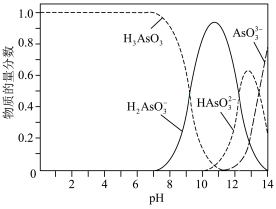
(1)写出As2O3溶于过量NaOH溶液的离子方程式:___________ 。
(2)将亚砷酸溶液注入一般情况下的血液后,砷元素的主要存在形式为___________ (填微粒化学符号)。
(3)该条件下, 的电离平衡常数Ka3与
的电离平衡常数Ka3与 的水解平衡常数Kh1的大小关系为Ka3
的水解平衡常数Kh1的大小关系为Ka3 ____ Kh1(填“>”、“<”或“=”,下同)。对于0.1 mol/L Na2HAsO3溶液而言,c( )
)______ c( )。
)。

(1)写出As2O3溶于过量NaOH溶液的离子方程式:
(2)将亚砷酸溶液注入一般情况下的血液后,砷元素的主要存在形式为
(3)该条件下,
 的电离平衡常数Ka3与
的电离平衡常数Ka3与 的水解平衡常数Kh1的大小关系为Ka3
的水解平衡常数Kh1的大小关系为Ka3  )
) )。
)。
您最近半年使用:0次



