20. 汽车尾气中排放的N
xO
y和CO,科学家寻找高效催化剂实现大气污染物转化:
2CO(g)+2NO(g)
⇌N
2(g)+2CO
2(g)
△H
1(1)已知:CO的燃烧热△H
2 = -283 kJ·moL
-1。几种化学键的键能数据如下:
化学键 | N≡N键 | O=O键 | N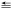 O键 O键 |
键能/kJ·moL-1 | 945 | 498 | 630 |
已知:N
2(g)+O
2(g) =2NO(g)
△H
3,则:△H
1=
__________。
(2)CO与空气在KOH溶液中构成燃料电池(石墨为电极),若放电后电解质溶液中离子浓度大小顺序为c(K
+)> c(HCO
3-)> c(OH
-) > c(H
+)> c(CO
32-),则负极的反应式为
________;
(3)在一定温度下,向2L的密闭容器中充入4.0molNO
2和4.0molCO,在催化剂作用下发生反应4CO(g)+2NO
2(g)
⇌N
2(g)+4CO
2(g)
△H< 0,相关数据如下:
| 0 min | 5min | 10min | 15min | 20min |
| c(NO2) | 2.0 | 1.7 | 1.56 | 1.5 | 1.5 |
| c(N2) | 0 | 0.15 | 0.22 | 0.25 | 0.25 |
①5~10min,用CO的浓度变化表示的反应速率为:
____________。
②能说明上述反应达到平衡状态的是
__________。
A.2n
正(NO
2) =n
逆(N
2)
B.混合气体的平均相对分子质量不变
C.气体密度不变
D.容器内气体压强不变
③20min时,向容器中加入1.0molNO
2和1.0molCO,在t
1时刻再次达到平衡时,NO
2的转化率比原平衡时
_____(填“变大”、“ 变小”或“不变”)。
④计算此温度下的化学平衡常数K=
__________。
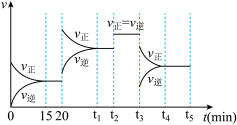
⑤在上述平衡的基础上,在时间t
2、t
3时改变反应的某一条件,反应速率的变化如图所示,则在t
3时刻改变的反应条件是:
_______;在时间15-20,t
1-t
2,t
2-t
3,t
4-t
5时的平衡常数分别为K
1、K
2、K
3、K
4,请比较各平衡常数的大小关系:
_____________________。