Ⅰ、水的电离平衡曲线如图所示。

(1)若以A点表示25℃时水的电离平衡的离子浓度,当温度升高到100℃时,水的电离平衡状态移动到B点,则此时水的离子积从________ 变化到_________ 。
(2)将pH=8的Ba(OH)2溶液与pH=5的稀盐酸混合,并保持100℃的恒温,致使混合溶液的pH=7,则Ba(OH)2和盐酸的体积比为__________________ 。
Ⅱ、有A、B、C、D四种强电解质,它们在水中电离时可产生下列离子(每种物质只含一种阴离子且互不重复 ):阳离子 Na+、Ba2+、NH4+ 阴离子 CH3COO-、Cl-、OH-、SO42-。已知:①A、C溶液的pH均大于7,A、B的溶液中水的电离程度相同;②C溶液和D溶液相遇时只生成白色沉淀,B溶液和C溶液相遇时只生成刺激性气味的气体,A溶液和D溶液混合时无明显现象。
①A是__________________ ,B是 __________________ 。
②用离子方程式表示A溶液呈碱性的原因__________________________ 。

(1)若以A点表示25℃时水的电离平衡的离子浓度,当温度升高到100℃时,水的电离平衡状态移动到B点,则此时水的离子积从
(2)将pH=8的Ba(OH)2溶液与pH=5的稀盐酸混合,并保持100℃的恒温,致使混合溶液的pH=7,则Ba(OH)2和盐酸的体积比为
Ⅱ、有A、B、C、D四种强电解质,它们在水中电离时可产生下列离子(每种物质
①A是
②用离子方程式表示A溶液呈碱性的原因
更新时间:2017-11-15 08:25:05
|
相似题推荐
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐1】Ⅰ.水在25℃和95℃时电离平衡曲线如图。

(1)在曲线B所对应的温度下,将 的
的 溶液与
溶液与 的
的 溶液混合,若所得混合溶液的
溶液混合,若所得混合溶液的 ,则
,则 溶液与
溶液与 溶液的体积比为
溶液的体积比为_______ 。
(2)在曲线A所对应的温度下,将a 的氨水与0.01
的氨水与0.01 的盐酸等体积混合充分反应后溶液呈中性,用含a的代数式表示
的盐酸等体积混合充分反应后溶液呈中性,用含a的代数式表示 的电离常数
的电离常数
_______ 。
(3)在曲线A所对应的温度下, 的溶度积
的溶度积 ,则
,则 在该温度下的溶解度是
在该温度下的溶解度是_______ ( 饱和溶液的密度可近似为1
饱和溶液的密度可近似为1 )。
)。
Ⅱ.已知A、B、C、D均为石墨电极;烧杯甲中是 溶液,烧杯乙中是
溶液,烧杯乙中是 溶液,向C电极中通入氧气,D电极通入甲烷气体。
溶液,向C电极中通入氧气,D电极通入甲烷气体。

(4)若将烧杯乙的电解质改为熔融碳酸钾,写出D的电极反应方程式。_______ 。
(5)反应一段时间后,若改为A与C连,B和D连,B的电极反应为_______ 。
(6)当D通入2.8
 (标况),A电极析出
(标况),A电极析出_______  的
的 ,B极的产物
,B极的产物_______
(7)一段时间后,向甲中投入0.1
 可令甲中电解质溶液复原,则转移电子数目为
可令甲中电解质溶液复原,则转移电子数目为_______
(8)当B级上产生22.4 气体时,将A、B两电极反接,A板上又产生22.4
气体时,将A、B两电极反接,A板上又产生22.4 气体,B极增加
气体,B极增加_______  (假设
(假设 足量,气体体积均在标况下测量)
足量,气体体积均在标况下测量)

(1)在曲线B所对应的温度下,将
 的
的 溶液与
溶液与 的
的 溶液混合,若所得混合溶液的
溶液混合,若所得混合溶液的 ,则
,则 溶液与
溶液与 溶液的体积比为
溶液的体积比为(2)在曲线A所对应的温度下,将a
 的氨水与0.01
的氨水与0.01 的盐酸等体积混合充分反应后溶液呈中性,用含a的代数式表示
的盐酸等体积混合充分反应后溶液呈中性,用含a的代数式表示 的电离常数
的电离常数
(3)在曲线A所对应的温度下,
 的溶度积
的溶度积 ,则
,则 在该温度下的溶解度是
在该温度下的溶解度是 饱和溶液的密度可近似为1
饱和溶液的密度可近似为1 )。
)。Ⅱ.已知A、B、C、D均为石墨电极;烧杯甲中是
 溶液,烧杯乙中是
溶液,烧杯乙中是 溶液,向C电极中通入氧气,D电极通入甲烷气体。
溶液,向C电极中通入氧气,D电极通入甲烷气体。
(4)若将烧杯乙的电解质改为熔融碳酸钾,写出D的电极反应方程式。
(5)反应一段时间后,若改为A与C连,B和D连,B的电极反应为
(6)当D通入2.8

 (标况),A电极析出
(标况),A电极析出 的
的 ,B极的产物
,B极的产物(7)一段时间后,向甲中投入0.1

 可令甲中电解质溶液复原,则转移电子数目为
可令甲中电解质溶液复原,则转移电子数目为(8)当B级上产生22.4
 气体时,将A、B两电极反接,A板上又产生22.4
气体时,将A、B两电极反接,A板上又产生22.4 气体,B极增加
气体,B极增加 (假设
(假设 足量,气体体积均在标况下测量)
足量,气体体积均在标况下测量)
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐2】回答下列问题:
(1)某温度(t℃)时,水的电离图象如图所示,a点水的离子积kw=________ ,该温度下,pH= 11的NaOH溶液与pH = 2的H2SO4溶液等体积混合,溶液显_____ (填“酸”或“碱”)性。

(2)25℃时,向0.1mol/L的氨水中加入少量NH4Cl固体,当固体溶解后,测得溶液pH____ (填“增大”、“减小”或“不变”,下同),NH 的物质的量浓度
的物质的量浓度_______
(3)将体积相等的NaOH稀溶液和CH3COOH溶液混合,若溶液中c(Na+)=c(CH3COO-),则该溶液显_______ (填“酸”、“碱”或“中”)性,则混合前c(NaOH)____ (填“>”“<”或“=”)c(CH3COOH)
(4)已知Kb(NH3·H2O)= 1×10-5,Ka(HF)=3.5x10-4,则1 mol/L NH4F溶液呈_____ (填“酸”或“碱”)性。
(5) NH4Cl的水解平衡常数Kh=_____
(1)某温度(t℃)时,水的电离图象如图所示,a点水的离子积kw=

(2)25℃时,向0.1mol/L的氨水中加入少量NH4Cl固体,当固体溶解后,测得溶液pH
 的物质的量浓度
的物质的量浓度(3)将体积相等的NaOH稀溶液和CH3COOH溶液混合,若溶液中c(Na+)=c(CH3COO-),则该溶液显
(4)已知Kb(NH3·H2O)= 1×10-5,Ka(HF)=3.5x10-4,则1 mol/L NH4F溶液呈
(5) NH4Cl的水解平衡常数Kh=
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐3】水的电离平衡曲线如图所示:
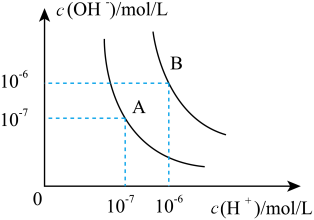
(1)若以A点表示25℃时水的电离平衡时的离子的浓度,当温度升高到100℃时,水的电离平衡状态到B点,则此时水的离子积从_______ 增加到_______ ,造成水的离子积增大的原因是_______ 。
(2)恒温下,向pH=6的蒸馏水中加入2.3g的金属钠,充分反应后,再加蒸馏水稀释到1L,所得溶液的pH=_______ 。
(3)向pH=6的蒸馏水和c(H+)=10-6 mol·L-1的稀盐酸中分别加入大小、质量相同的金属钠,反应刚开始时,产生H2的速率前者与后者相比是_______(填序号)
(4)25℃时,pH=10的X、Y两种碱溶液各1mL,分别稀释至100mL,其pH与溶液体积(V)的关系如图所示,下列说法正确的是_______。

(5)100℃时,将pH=9的NaOH溶液与pH=4的硫酸溶液混合, 若所得混合溶液pH=7,则NaOH溶液与硫酸溶液的体积比为_______ 。

(1)若以A点表示25℃时水的电离平衡时的离子的浓度,当温度升高到100℃时,水的电离平衡状态到B点,则此时水的离子积从
(2)恒温下,向pH=6的蒸馏水中加入2.3g的金属钠,充分反应后,再加蒸馏水稀释到1L,所得溶液的pH=
(3)向pH=6的蒸馏水和c(H+)=10-6 mol·L-1的稀盐酸中分别加入大小、质量相同的金属钠,反应刚开始时,产生H2的速率前者与后者相比是_______(填序号)
| A.一样快 | B.前者快 | C.后者快 | D.无法比较 |

| A.X、Y两种碱溶液中溶质的物质的量浓度一定相等 |
| B.稀释后,X溶液的碱性比Y溶液的碱性强 |
| C.分别完全中和X、Y这两种碱溶液时,消耗同浓度盐酸的体积VX>VY |
| D.若8<a<10,则X、Y都是弱碱 |
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
【推荐1】含硫化合物在生产、科研中应用广泛。请回答下列问题:
(1)多种多样的盐:
① 在染料工业中用于生产硫化染料,其水溶液显碱性的原因:
在染料工业中用于生产硫化染料,其水溶液显碱性的原因:_____________ (用离子反应方程式表示),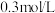 的
的 溶液与
溶液与 的
的 溶液中
溶液中
_____________  (填“>”、“<”或“=”);
(填“>”、“<”或“=”);
② 可应用做医药、照相还原剂、染料中间体等,写出
可应用做医药、照相还原剂、染料中间体等,写出 溶液的质子守恒表达式:
溶液的质子守恒表达式:_____________ [用含离子浓度的关系式表示,用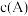 表示粒子A的浓度];③
表示粒子A的浓度];③ 可用作矿物分解助熔剂。已知:
可用作矿物分解助熔剂。已知: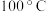 时,
时,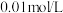 的
的 溶液中水电离的
溶液中水电离的 ,该温度下将
,该温度下将 的
的 溶液
溶液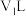 与
与 的
的 溶液
溶液 混合,所得溶液
混合,所得溶液 ,则
,则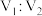 为
为_____________ (忽略溶液混合时的体积变化)。
(2) 可用于金属精制、农药、医药、催化剂再生。常温下,向
可用于金属精制、农药、医药、催化剂再生。常温下,向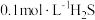 溶液中通入
溶液中通入 气体或加入
气体或加入 固体,测得
固体,测得 与溶液
与溶液 的关系如图所示(忽略体积的变化及)
的关系如图所示(忽略体积的变化及) 挥发)。
挥发)。

①当 时,溶液中
时,溶液中
_____________  ;
;
②当溶液 时,溶液中的
时,溶液中的
_____________  ;
;
③某溶液含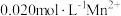 、
、 ,当溶液
,当溶液
_____________ 时, 开始沉淀[已知:
开始沉淀[已知: ]。
]。
(1)多种多样的盐:
①
 在染料工业中用于生产硫化染料,其水溶液显碱性的原因:
在染料工业中用于生产硫化染料,其水溶液显碱性的原因: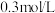 的
的 溶液与
溶液与 的
的 溶液中
溶液中
 (填“>”、“<”或“=”);
(填“>”、“<”或“=”);②
 可应用做医药、照相还原剂、染料中间体等,写出
可应用做医药、照相还原剂、染料中间体等,写出 溶液的质子守恒表达式:
溶液的质子守恒表达式: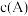 表示粒子A的浓度];③
表示粒子A的浓度];③ 可用作矿物分解助熔剂。已知:
可用作矿物分解助熔剂。已知: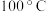 时,
时,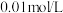 的
的 溶液中水电离的
溶液中水电离的 ,该温度下将
,该温度下将 的
的 溶液
溶液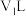 与
与 的
的 溶液
溶液 混合,所得溶液
混合,所得溶液 ,则
,则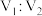 为
为(2)
 可用于金属精制、农药、医药、催化剂再生。常温下,向
可用于金属精制、农药、医药、催化剂再生。常温下,向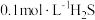 溶液中通入
溶液中通入 气体或加入
气体或加入 固体,测得
固体,测得 与溶液
与溶液 的关系如图所示(忽略体积的变化及)
的关系如图所示(忽略体积的变化及) 挥发)。
挥发)。
①当
 时,溶液中
时,溶液中
 ;
;②当溶液
 时,溶液中的
时,溶液中的
 ;
;③某溶液含
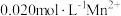 、
、 ,当溶液
,当溶液
 开始沉淀[已知:
开始沉淀[已知: ]。
]。
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
【推荐2】弱电解质的电离平衡、盐类的水解平衡和难溶物的溶解平衡均属化学平衡。根据要求回答问题:
(1)常温下浓度均为 的8种溶液:①
的8种溶液:① 溶液;②
溶液;② 溶液;③
溶液;③ 溶液;④
溶液;④ 溶液;⑤
溶液;⑤ 溶液;⑥
溶液;⑥ 溶液;⑦
溶液;⑦ 溶液;⑧
溶液;⑧ 溶液,这些溶液的pH由小到大的顺序是
溶液,这些溶液的pH由小到大的顺序是______________ (填序号)。
(2)常温下, 的盐酸和
的盐酸和 的
的 溶液中,水电离出的
溶液中,水电离出的 分别为
分别为 和
和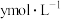 ,二者的关系正确的是
,二者的关系正确的是____________ (填字母)。
a.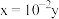 b.
b.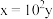 c.
c. d.
d.
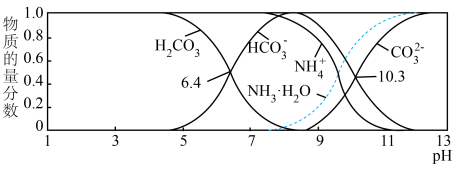
(3)室温下,测得用氨水吸收 时,溶液中含碳(氮)各粒子的物质的量分数和pH的关系如图,若所得溶液
时,溶液中含碳(氮)各粒子的物质的量分数和pH的关系如图,若所得溶液 ,则溶液中
,则溶液中 =
=_________ (已知 )。
)。
(4)工业上常用氨水吸收含碳燃料燃烧中产生的温室气体 ,其产物之一是
,其产物之一是 。已知常温下碳酸的电离常数
。已知常温下碳酸的电离常数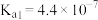 ,
,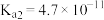 ,
, 的电离常数
的电离常数 ,则所得
,则所得 溶液中
溶液中
___________  (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
(5)常温下,将 的氨水溶液加水稀释,下列数值一定减小的是____________(填字母)。
的氨水溶液加水稀释,下列数值一定减小的是____________(填字母)。
(6)某温度下,测得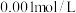 的
的 溶液中水电离出的
溶液中水电离出的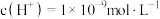 ,将
,将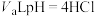 溶液和
溶液和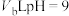 的
的 溶液混合均匀,测得溶液的
溶液混合均匀,测得溶液的 ,则
,则
___________ 。
(7)常温下,若在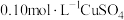 溶液中加入
溶液中加入 稀溶液充分搅拌,有浅蓝色氢氧化铜沉淀生成,当溶液的
稀溶液充分搅拌,有浅蓝色氢氧化铜沉淀生成,当溶液的 时,
时,
_________  。
。
(1)常温下浓度均为
 的8种溶液:①
的8种溶液:① 溶液;②
溶液;② 溶液;③
溶液;③ 溶液;④
溶液;④ 溶液;⑤
溶液;⑤ 溶液;⑥
溶液;⑥ 溶液;⑦
溶液;⑦ 溶液;⑧
溶液;⑧ 溶液,这些溶液的pH由小到大的顺序是
溶液,这些溶液的pH由小到大的顺序是(2)常温下,
 的盐酸和
的盐酸和 的
的 溶液中,水电离出的
溶液中,水电离出的 分别为
分别为 和
和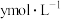 ,二者的关系正确的是
,二者的关系正确的是a.
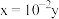 b.
b.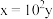 c.
c. d.
d.
(3)室温下,测得用氨水吸收
 时,溶液中含碳(氮)各粒子的物质的量分数和pH的关系如图,若所得溶液
时,溶液中含碳(氮)各粒子的物质的量分数和pH的关系如图,若所得溶液 ,则溶液中
,则溶液中 =
= )。
)。
(4)工业上常用氨水吸收含碳燃料燃烧中产生的温室气体
 ,其产物之一是
,其产物之一是 。已知常温下碳酸的电离常数
。已知常温下碳酸的电离常数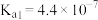 ,
,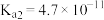 ,
, 的电离常数
的电离常数 ,则所得
,则所得 溶液中
溶液中
 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。(5)常温下,将
 的氨水溶液加水稀释,下列数值一定减小的是____________(填字母)。
的氨水溶液加水稀释,下列数值一定减小的是____________(填字母)。A. | B. | C. | D. |
(6)某温度下,测得
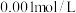 的
的 溶液中水电离出的
溶液中水电离出的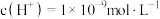 ,将
,将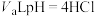 溶液和
溶液和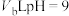 的
的 溶液混合均匀,测得溶液的
溶液混合均匀,测得溶液的 ,则
,则
(7)常温下,若在
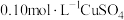 溶液中加入
溶液中加入 稀溶液充分搅拌,有浅蓝色氢氧化铜沉淀生成,当溶液的
稀溶液充分搅拌,有浅蓝色氢氧化铜沉淀生成,当溶液的 时,
时,
 。
。
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐3】Ⅰ.雾霾天气严重影响人们的生活,汽车尾气所排放的氮氧化物及燃煤所排放的硫氧化物是造成雾霾的重要原因。
(1)NH3催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术。反应原理如图所示:

图中是不同催化剂Mn和Cr在不同温度下对应的脱氮率,由图可知工业使用的最佳的催化剂和相应的温度分别为________ 。
(2)改善能源结构是治理雾霾问题的最直接有效途径。二甲醚是一种清洁能源,可用合成气在催化剂存在下制备二甲醚,其反应原理为:2CO(g)+4H2(g) CH3OCH3 (g)+H2O(g) ΔH, 在恒容密闭容器里按体积比为1∶2充入一氧化碳和氢气,一定条件下反应达到平衡状态。当改变反应的某一个条件后,下列变化能说明平衡一定向逆反应方向移动的是
CH3OCH3 (g)+H2O(g) ΔH, 在恒容密闭容器里按体积比为1∶2充入一氧化碳和氢气,一定条件下反应达到平衡状态。当改变反应的某一个条件后,下列变化能说明平衡一定向逆反应方向移动的是________ 。
A.一氧化碳的转化率减小 B.容器的压强增大 C.化学平衡常数K值减小
D.逆反应速率先增大后减小 E.混合气体的密度增大
(3)25℃时, mL 0.2
mL 0.2 稀盐酸与
稀盐酸与 mL 0.1
mL 0.1 NaOH溶液混合,忽略溶液混合时的体积变化。若
NaOH溶液混合,忽略溶液混合时的体积变化。若 ,则混合溶液的pH=
,则混合溶液的pH=___________ ;若混合溶液的pH=12,则
___________ 。(已知溶液pH均为25℃时的pH, )
)
Ⅱ.25℃时,pH=2的盐酸和醋酸各1mL分别加水稀释,pH随溶液体积变化的曲线如下图所示。请回答如下问题

(4)曲线___________ (填“Ⅰ”或“Ⅱ”)代表盐酸的稀释过程
(5)a溶液中水的电离程度比b溶液___________ (填“大”或“小”)
(6)将a、b两溶液加热至30℃,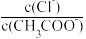
___________ (填“变大”、“变小”或“不变”)
(7)设稀释前的醋酸电离度为0.1%,醋酸的电离常数Ka=___________ 。
(1)NH3催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术。反应原理如图所示:

图中是不同催化剂Mn和Cr在不同温度下对应的脱氮率,由图可知工业使用的最佳的催化剂和相应的温度分别为
(2)改善能源结构是治理雾霾问题的最直接有效途径。二甲醚是一种清洁能源,可用合成气在催化剂存在下制备二甲醚,其反应原理为:2CO(g)+4H2(g)
 CH3OCH3 (g)+H2O(g) ΔH, 在恒容密闭容器里按体积比为1∶2充入一氧化碳和氢气,一定条件下反应达到平衡状态。当改变反应的某一个条件后,下列变化能说明平衡一定向逆反应方向移动的是
CH3OCH3 (g)+H2O(g) ΔH, 在恒容密闭容器里按体积比为1∶2充入一氧化碳和氢气,一定条件下反应达到平衡状态。当改变反应的某一个条件后,下列变化能说明平衡一定向逆反应方向移动的是A.一氧化碳的转化率减小 B.容器的压强增大 C.化学平衡常数K值减小
D.逆反应速率先增大后减小 E.混合气体的密度增大
(3)25℃时,
 mL 0.2
mL 0.2 稀盐酸与
稀盐酸与 mL 0.1
mL 0.1 NaOH溶液混合,忽略溶液混合时的体积变化。若
NaOH溶液混合,忽略溶液混合时的体积变化。若 ,则混合溶液的pH=
,则混合溶液的pH=
 )
)Ⅱ.25℃时,pH=2的盐酸和醋酸各1mL分别加水稀释,pH随溶液体积变化的曲线如下图所示。请回答如下问题

(4)曲线
(5)a溶液中水的电离程度比b溶液
(6)将a、b两溶液加热至30℃,
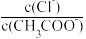
(7)设稀释前的醋酸电离度为0.1%,醋酸的电离常数Ka=
您最近一年使用:0次



