钨酸钙是非常重要的化学原料,主要用于生产钨铁、钨丝及钨合金等钨制品。在钨冶炼工艺中,将氢氧化钙加入钨酸钠碱性溶液中得到钨酸钙。发生反应:
Ⅰ.WO42ˉ(aq)+Ca(OH)2(s) CaWO4(s)+2OHˉ(aq) K1
CaWO4(s)+2OHˉ(aq) K1
已知:反应Ⅰ的平衡常数K1理论值如下表,请回答下列问题:
(1)判断反应Ⅰ的△S______ 0、△H______ 0(填“>”、“=”或“<”),在______ (填“较高”或“较低”)温度下有利于该反应自发进行。
(2)氢氧化钙和钨酸钙(CaWO4)都是微溶电解质,溶解度均随温度升高而减小。它们在水中存在如下沉淀溶解平衡:
Ⅱ.CaWO4(s) Ca2+(aq) + WO42ˉ(aq) K2
Ca2+(aq) + WO42ˉ(aq) K2
Ⅲ.Ca(OH)2(s) Ca2+(aq) + 2OHˉ(aq) K3
Ca2+(aq) + 2OHˉ(aq) K3
①根据反应Ⅰ~Ⅲ,可推导出K1、K2与K3之间的关系,则K1=______ (用K2、K3表示)。
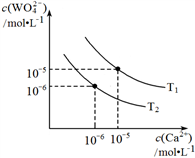
②根据反应Ⅱ,右图为不同温度下CaWO4的沉淀溶解平衡曲线。则T1____ T2(填“>”“=”或“<”)。T1时,向0.5 mol•Lˉ1钨酸钠的碱性溶液中,加入适量Ca(OH)2,反应达到平衡后WO42ˉ的转化率为60%,此时溶液中c(Ca2+)=_______ mol•Lˉ1。(假设反应前后体积不变)
(3)制取钨酸钙时,适时向反应混合液中添加适量的某种酸性物质,有利于提高WO42ˉ的转化率。反应后过滤,再向滤液中通CO2,进一步处理得到Na2CO3。
①在反应混合液中不直接通入CO2,其理由是_____________ ;
②用平衡移动原理解释添加酸性物质的理由______________ 。
Ⅰ.WO42ˉ(aq)+Ca(OH)2(s)
 CaWO4(s)+2OHˉ(aq) K1
CaWO4(s)+2OHˉ(aq) K1已知:反应Ⅰ的平衡常数K1理论值如下表,请回答下列问题:
温度/℃ | 25 | 50 | 90 | 100 |
K1 | 79.96 | 208.06 | 222.88 | 258.05 |
(1)判断反应Ⅰ的△S
(2)氢氧化钙和钨酸钙(CaWO4)都是微溶电解质,溶解度均随温度升高而减小。它们在水中存在如下沉淀溶解平衡:
Ⅱ.CaWO4(s)
 Ca2+(aq) + WO42ˉ(aq) K2
Ca2+(aq) + WO42ˉ(aq) K2Ⅲ.Ca(OH)2(s)
 Ca2+(aq) + 2OHˉ(aq) K3
Ca2+(aq) + 2OHˉ(aq) K3①根据反应Ⅰ~Ⅲ,可推导出K1、K2与K3之间的关系,则K1=
②根据反应Ⅱ,右图为不同温度下CaWO4的沉淀溶解平衡曲线。则T1

(3)制取钨酸钙时,适时向反应混合液中添加适量的某种酸性物质,有利于提高WO42ˉ的转化率。反应后过滤,再向滤液中通CO2,进一步处理得到Na2CO3。
①在反应混合液中不直接通入CO2,其理由是
②用平衡移动原理解释添加酸性物质的理由
更新时间:2017-11-25 09:26:57
|
相似题推荐
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐1】CO2可作为合成低碳烯烃的原料加以利用。如:
2CO2(g)+6H2(g) CH2=CH2(g)+4H2O(g) ΔH= a kJ·mol-1
CH2=CH2(g)+4H2O(g) ΔH= a kJ·mol-1
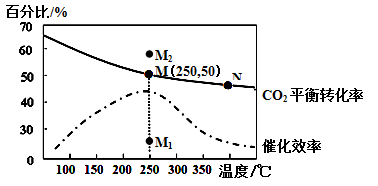
如图所示为在体积为1 L的恒容容器中,投料为3 mol H2和1 mol CO2时,测得的温度对CO2的平衡转化率和催化剂催化效率的影响。
已知:H2和CH2=CH2的标准燃烧热分别是-285.8 kJ·mol-1和-1411.0 kJ·mol-1。
H2O(g) H2O(l) ΔH=-44 kJ·mol-1
H2O(l) ΔH=-44 kJ·mol-1
请回答:
(1)a=____________ kJ·mol-1。
(2)上述由CO2合成CH2=CH2的反应在_______ 下自发(填“高温”或“低温”),理由是_____________ 。
(3)计算250 ℃时该反应平衡常数的数值K=____________ 。
(4)下列说法正确的是____________ 。
a.平衡常数大小:M>N
b.反应物活化分子百分数大小:M>N
c.其他条件不变,若不使用催化剂,则250℃时CO2的平衡转化率可能位于点M1
d.其他条件不变,若投料改为4 mol H2和1 mol CO2时,则250℃时CO2的平衡转化率可能位于点M2
e.当压强、混合气体的密度或n(H2)/n(CO2)不变时均可视为化学反应已达到平衡状态
(5)保持某温度(大于100℃)不变,在体积为V L的恒容容器中以n(H2)∶n(CO2)=3∶1的投料比加入反应物,至t0时达到化学平衡。t1时将容器体积瞬间扩大至2V L并保持不变,t2时重新达平衡。作出容器内混合气体的平均相对分子质量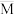 随时间变化的图象。
随时间变化的图象。
____________

2CO2(g)+6H2(g)
 CH2=CH2(g)+4H2O(g) ΔH= a kJ·mol-1
CH2=CH2(g)+4H2O(g) ΔH= a kJ·mol-1如图所示为在体积为1 L的恒容容器中,投料为3 mol H2和1 mol CO2时,测得的温度对CO2的平衡转化率和催化剂催化效率的影响。

已知:H2和CH2=CH2的标准燃烧热分别是-285.8 kJ·mol-1和-1411.0 kJ·mol-1。
H2O(g)
 H2O(l) ΔH=-44 kJ·mol-1
H2O(l) ΔH=-44 kJ·mol-1请回答:
(1)a=
(2)上述由CO2合成CH2=CH2的反应在
(3)计算250 ℃时该反应平衡常数的数值K=
(4)下列说法正确的是
a.平衡常数大小:M>N
b.反应物活化分子百分数大小:M>N
c.其他条件不变,若不使用催化剂,则250℃时CO2的平衡转化率可能位于点M1
d.其他条件不变,若投料改为4 mol H2和1 mol CO2时,则250℃时CO2的平衡转化率可能位于点M2
e.当压强、混合气体的密度或n(H2)/n(CO2)不变时均可视为化学反应已达到平衡状态
(5)保持某温度(大于100℃)不变,在体积为V L的恒容容器中以n(H2)∶n(CO2)=3∶1的投料比加入反应物,至t0时达到化学平衡。t1时将容器体积瞬间扩大至2V L并保持不变,t2时重新达平衡。作出容器内混合气体的平均相对分子质量
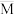 随时间变化的图象。
随时间变化的图象。
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐2】费托合成是以合成气为原料,在催化作用下合成液态烃的工艺流程,是我国煤化工的重点发展方向。催化剂的选择性、高稳定性是研究重点,目前主要以纳米铁系催化剂以及钴系催化剂为主,实验室常以固定床或者搅拌釜作为该反应的研究装置,已知该反应的机理如图所示:

已知2CO(g)+4H2(g) C2H4(g)+2H2O(g)△H=-237kJ/mol反应Ⅰ
C2H4(g)+2H2O(g)△H=-237kJ/mol反应Ⅰ
CO(g)+3H2(g) CH4(g)+H2O(g)△H=-178kJ/mol反应Ⅱ
CH4(g)+H2O(g)△H=-178kJ/mol反应Ⅱ
(1)C是一种良好的还原剂,可用来还原各种金属氧化物,如图为C和Al分别和氧气反应的吉布斯自由能变与温度的关系,已知ΔG<0,反应自发,写出C在2000K以上还原Al2O3的化学方程式:__ ,由如图推测2000K以上该反应是反应___ (填“自发”或者“不自发”)。
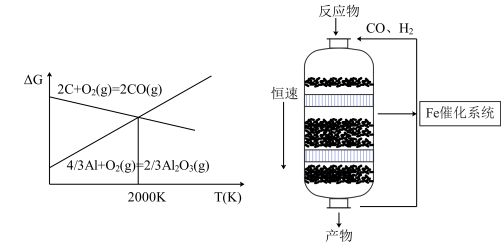
(2)在固定床反应器中,生产条件为5MPa,200℃~250℃,流速100mL/min,若不考虑其它产物的情况,下列说法错误 的是___ 。
A.采用纳米铁催化剂可以提高催化剂表面积,加快化学反应速率
B.合成气在催化剂表面没有化学键的形成,催化剂改变了化学反应历程
C.固定床反应器中合成气的流速影响产物的转化率和选择性
D.适当升高温度(不考虑催化剂失活)可以提高CO的平衡转化率
E.反应开始前往往先通入H2处理一段时间是为了激活催化剂,去除表面氧化膜
(3)已知固定床反应器中增加装置压强会导致产物中C2H4选择性上升,可能的原因是___ 。
(4)实验中通常也以搅拌釜作为恒容反应容器,在搅拌釜中加入铁系催化剂,再通入10MPa合成气后关闭进气,升温到200℃维持稳定,开启搅拌桨,一直反应到约10~20h后装置内气压不再发生改变(不考虑装置漏气)。在保持其他条件不变的情况下,为了提高C2H4的选择性可以采取的措施是___ 。
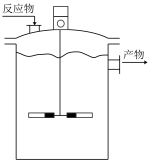
A.适当升高温度 B.改变催化剂 C.适当降低温度 D.加快搅拌速度
(5)搅拌釜反应器中按照投料比 =3:1通入气体,起始压强为8MPa,关闭进气阀,控制反应温度为200℃,反应结束后测得CO的转化率为20%,C2H4的选择性为50%,求该条件下反应Ⅱ的Kp=
=3:1通入气体,起始压强为8MPa,关闭进气阀,控制反应温度为200℃,反应结束后测得CO的转化率为20%,C2H4的选择性为50%,求该条件下反应Ⅱ的Kp=___ (MPa)-2(对于气相反应,用某组分B的平衡压强p(B)代替物质的量浓度c(B)表示的平衡常数记作Kp)。
(6)某课题小组采用气相色谱研究该反应中C1到C4的各种烃类分布,以N2作为载气(流动相),已知不同气体在同一色谱柱中出峰时间不相同,如图为该产物色谱图中的部分内容,请利用气相色谱设计一种方法判断哪一个峰是乙烯___ 。



已知2CO(g)+4H2(g)
 C2H4(g)+2H2O(g)△H=-237kJ/mol反应Ⅰ
C2H4(g)+2H2O(g)△H=-237kJ/mol反应ⅠCO(g)+3H2(g)
 CH4(g)+H2O(g)△H=-178kJ/mol反应Ⅱ
CH4(g)+H2O(g)△H=-178kJ/mol反应Ⅱ(1)C是一种良好的还原剂,可用来还原各种金属氧化物,如图为C和Al分别和氧气反应的吉布斯自由能变与温度的关系,已知ΔG<0,反应自发,写出C在2000K以上还原Al2O3的化学方程式:

(2)在固定床反应器中,生产条件为5MPa,200℃~250℃,流速100mL/min,若不考虑其它产物的情况,下列说法
A.采用纳米铁催化剂可以提高催化剂表面积,加快化学反应速率
B.合成气在催化剂表面没有化学键的形成,催化剂改变了化学反应历程
C.固定床反应器中合成气的流速影响产物的转化率和选择性
D.适当升高温度(不考虑催化剂失活)可以提高CO的平衡转化率
E.反应开始前往往先通入H2处理一段时间是为了激活催化剂,去除表面氧化膜
(3)已知固定床反应器中增加装置压强会导致产物中C2H4选择性上升,可能的原因是
(4)实验中通常也以搅拌釜作为恒容反应容器,在搅拌釜中加入铁系催化剂,再通入10MPa合成气后关闭进气,升温到200℃维持稳定,开启搅拌桨,一直反应到约10~20h后装置内气压不再发生改变(不考虑装置漏气)。在保持其他条件不变的情况下,为了提高C2H4的选择性可以采取的措施是

A.适当升高温度 B.改变催化剂 C.适当降低温度 D.加快搅拌速度
(5)搅拌釜反应器中按照投料比
 =3:1通入气体,起始压强为8MPa,关闭进气阀,控制反应温度为200℃,反应结束后测得CO的转化率为20%,C2H4的选择性为50%,求该条件下反应Ⅱ的Kp=
=3:1通入气体,起始压强为8MPa,关闭进气阀,控制反应温度为200℃,反应结束后测得CO的转化率为20%,C2H4的选择性为50%,求该条件下反应Ⅱ的Kp=(6)某课题小组采用气相色谱研究该反应中C1到C4的各种烃类分布,以N2作为载气(流动相),已知不同气体在同一色谱柱中出峰时间不相同,如图为该产物色谱图中的部分内容,请利用气相色谱设计一种方法判断哪一个峰是乙烯


您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
【推荐3】钛(Ti)及其合金是理想的高强度、低密度结构材料。以钛渣(主要成分为 ,含少量V、Si和Al的氧化物杂质)为原料,制备金属钛的工艺流程如下:
,含少量V、Si和Al的氧化物杂质)为原料,制备金属钛的工艺流程如下:
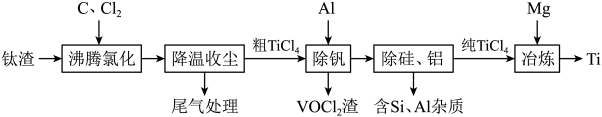
已知“降温收尘”后,粗 中含有的几种物质的沸点:
中含有的几种物质的沸点:
回答下列问题:
(1)已知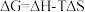 ,
, 的值只决定于反应体系的始态和终态,忽略
的值只决定于反应体系的始态和终态,忽略 、
、 随温度的变化。若
随温度的变化。若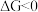 ,则该反应可以自发进行。根据下图判断:
,则该反应可以自发进行。根据下图判断: 时,下列反应不能自发进行的是_______。
时,下列反应不能自发进行的是_______。
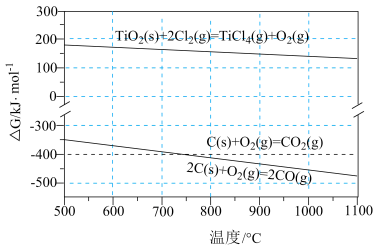
(2) 与C、
与C、 ,在
,在 的沸腾炉中充分反应后,混合气体中各组分的分压如下表:
的沸腾炉中充分反应后,混合气体中各组分的分压如下表:
①该温度下, 与C、
与C、 反应的总化学方程式为
反应的总化学方程式为_______ ;
②随着温度升高,尾气中 的含量升高,原因是
的含量升高,原因是_______ 。
(3)“除钒”过程中的化学方程式为_______ ;“除硅、铝”过程中,分离 中含
中含 、
、 杂质的方法是
杂质的方法是_______ 。
(4)“除钒”和“除硅、铝”的顺序_______ (填“能”或“不能”)交换,理由是_______ 。
(5)下列金属冶炼方法与本工艺流程中加入 冶炼
冶炼 的方法相似的是_______。
的方法相似的是_______。
 ,含少量V、Si和Al的氧化物杂质)为原料,制备金属钛的工艺流程如下:
,含少量V、Si和Al的氧化物杂质)为原料,制备金属钛的工艺流程如下:
已知“降温收尘”后,粗
 中含有的几种物质的沸点:
中含有的几种物质的沸点:| 物质 |  |  |  |  |
沸点/ | 136 | 127 | 57 | 180 |
(1)已知
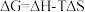 ,
, 的值只决定于反应体系的始态和终态,忽略
的值只决定于反应体系的始态和终态,忽略 、
、 随温度的变化。若
随温度的变化。若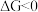 ,则该反应可以自发进行。根据下图判断:
,则该反应可以自发进行。根据下图判断: 时,下列反应不能自发进行的是_______。
时,下列反应不能自发进行的是_______。
A. | B. |
C. | D. |
 与C、
与C、 ,在
,在 的沸腾炉中充分反应后,混合气体中各组分的分压如下表:
的沸腾炉中充分反应后,混合气体中各组分的分压如下表:| 物质 |  |  |  |  |
分压 | 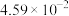 | 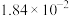 |  |  |
 与C、
与C、 反应的总化学方程式为
反应的总化学方程式为②随着温度升高,尾气中
 的含量升高,原因是
的含量升高,原因是(3)“除钒”过程中的化学方程式为
 中含
中含 、
、 杂质的方法是
杂质的方法是(4)“除钒”和“除硅、铝”的顺序
(5)下列金属冶炼方法与本工艺流程中加入
 冶炼
冶炼 的方法相似的是_______。
的方法相似的是_______。| A.高炉炼铁 | B.电解熔融氯化钠制钠 | C.铝热反应制锰 | D.氧化汞分解制汞 |
您最近一年使用:0次
【推荐1】CuCl为白色固体,微溶于水,不溶于乙醇和稀硫酸,在空气中迅速被氧化成绿色;见光则分解,变成褐色;已知CuCl+ 3Cl-=[CuCl4]3-。从酸性电镀废液(主要含Cu2+、Fe3+)中制备氯化亚铜的工艺流程图如下:

(1)图中的铁粉可以用二氧化硫气体代替,可以减少污染气体的排放,请写出用SO2代替铁粉进行反应的离子方程式:_____________ 。
(2)常温下形成电镀污泥时,溶液pH=9,已知Ksp[Fe(OH)3]=4×10-38,Ksp[Cu(OH)2]=2×10-20,此时溶液中c(Fe3+):c(Cu2+)=_______ 。
(3)析出CuCl晶体后,采用过滤的方法进行分离,再对晶体进行洗涤。下列关于洗涤的说法正确的是______ (填序号)。
A.因为存在CuCl的沉淀溶解平衡,所以用饱和NaCl溶液洗涤可以降低CuCl的溶解度
B.尽量少用水洗涤,防止其溶解或水解生成CuOH
C.可以用乙醇洗涤使产品快速干燥
D.洗涤时在漏斗中充分搅拌,使杂质尽可能地溶解达到除去的目的
E.如果采用减压过滤,在洗涤时应该先打开阀门与空气相通,再关闭抽气泵,然后再向漏斗中加入洗涤液
(4)第三次过滤的滤液主要成分是_________ 。
(5)对污泥进行酸浸时的化学反应方程式为___________________ 。
(6)检验氧化亚铜晶体洗涤干净的操作是_______________ 。
(7)以粗铜为电极电解一定浓度的氯化钠溶液,控制一定的电压和电流,也可以制得氯化亚铜,写出电解时的阳极反应式:_____________ 。

(1)图中的铁粉可以用二氧化硫气体代替,可以减少污染气体的排放,请写出用SO2代替铁粉进行反应的离子方程式:
(2)常温下形成电镀污泥时,溶液pH=9,已知Ksp[Fe(OH)3]=4×10-38,Ksp[Cu(OH)2]=2×10-20,此时溶液中c(Fe3+):c(Cu2+)=
(3)析出CuCl晶体后,采用过滤的方法进行分离,再对晶体进行洗涤。下列关于洗涤的说法正确的是
A.因为存在CuCl的沉淀溶解平衡,所以用饱和NaCl溶液洗涤可以降低CuCl的溶解度
B.尽量少用水洗涤,防止其溶解或水解生成CuOH
C.可以用乙醇洗涤使产品快速干燥
D.洗涤时在漏斗中充分搅拌,使杂质尽可能地溶解达到除去的目的
E.如果采用减压过滤,在洗涤时应该先打开阀门与空气相通,再关闭抽气泵,然后再向漏斗中加入洗涤液
(4)第三次过滤的滤液主要成分是
(5)对污泥进行酸浸时的化学反应方程式为
(6)检验氧化亚铜晶体洗涤干净的操作是
(7)以粗铜为电极电解一定浓度的氯化钠溶液,控制一定的电压和电流,也可以制得氯化亚铜,写出电解时的阳极反应式:
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
【推荐2】H2C2O4(草酸)是一种无色晶体,易溶于水,熔点为182 ℃,150~160℃升华,189.5 ℃分解。25℃时,Ka1=6×10-2,Ka2=6.4×10-5,Ksp(CaC2O4) =4.0×10-9。某校甲、乙、丙3 个学习小组设计实验探究草酸的化学性质。
(1)草酸中所含官能团的名称为__________ ;
反应Ca2+(aq)+H2C2O4(aq) CaC2O4(s)+2H+(aq),25℃时的平衡常数K=
CaC2O4(s)+2H+(aq),25℃时的平衡常数K=__________ 。
(2)甲组同学在Na2CO3溶液中加入少量草酸溶液产生大量气体,他们查得H2CO3的Ka1=4.47×10-7,Ka2=4.68×10-11,则发生反应的离子方程式为______________ 。
(3)乙组同学在酸性KMnO4溶液中逐滴加入草酸溶液,溶液紫色逐渐褪去,说明草酸具有_____ 性,反应中氧化产物与还原产物的物质的量之比为_________ 。
(4)丙组同学设计下列装置分解H2C2O4 并设计实验装置检验产物中的CO2 和CO。
 ①分解H2C2O4 装置中最好的是
①分解H2C2O4 装置中最好的是__________ (填字母)。
②d中澄清石灰水变浑浊,能否说明有CO2 生成?___ (填“能“或“不能”,下同),理由是________ ;仅依据装置g中澄清石灰水变浑浊,能否说明有CO生成?_________ ,理由是_____________ 。
(1)草酸中所含官能团的名称为
反应Ca2+(aq)+H2C2O4(aq)
 CaC2O4(s)+2H+(aq),25℃时的平衡常数K=
CaC2O4(s)+2H+(aq),25℃时的平衡常数K=(2)甲组同学在Na2CO3溶液中加入少量草酸溶液产生大量气体,他们查得H2CO3的Ka1=4.47×10-7,Ka2=4.68×10-11,则发生反应的离子方程式为
(3)乙组同学在酸性KMnO4溶液中逐滴加入草酸溶液,溶液紫色逐渐褪去,说明草酸具有
(4)丙组同学设计下列装置分解H2C2O4 并设计实验装置检验产物中的CO2 和CO。
 ①分解H2C2O4 装置中最好的是
①分解H2C2O4 装置中最好的是②d中澄清石灰水变浑浊,能否说明有CO2 生成?
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐3】以钛铁矿(主要成分为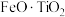 ,还含有
,还含有 、
、 、
、 等杂质)为原料合成锂离子电池的电极材料钛酸锂(
等杂质)为原料合成锂离子电池的电极材料钛酸锂( )和磷酸亚铁锂(
)和磷酸亚铁锂( )的工艺流程如下:
)的工艺流程如下:

回答下列问题:
(1)“溶浸”后溶液中的金属阳离子主要包括 、
、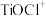
_______ 。“滤液”经加热水解后转化为富钛渣(钛元素主要以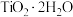 形式存在),写出上述制备
形式存在),写出上述制备 的离子方程式:
的离子方程式:_______ 。在制备时加入大量的水,同时加热的目的是_______
(2)“溶钛”过程反应温度不能太高,其原因是_______ 。
(3)“沉铁”步骤反应的化学方程式为_______ ,“沉铁”后的滤液经处理后可返回_______ 工序循环利用。
(4)“煅烧”制备 过程中,
过程中, 和
和 的理论投入量的物质的量之比为
的理论投入量的物质的量之比为_______ 。
(5)以 和
和 作电极组成电池,充电时发生反应:
作电极组成电池,充电时发生反应: (
(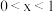 ),阳极的电极反应式为
),阳极的电极反应式为_______ 。
(6)从废旧 电极中可回收锂元素。用硝酸充分溶浸废旧
电极中可回收锂元素。用硝酸充分溶浸废旧 电极,测得浸取液中
电极,测得浸取液中 ,加入等体积的碳酸钠溶液将
,加入等体积的碳酸钠溶液将 转化为
转化为 沉淀,若沉淀中的锂元素占浸取液中锂元素总量的90%,则反应后的溶液中
沉淀,若沉淀中的锂元素占浸取液中锂元素总量的90%,则反应后的溶液中 的浓度为
的浓度为_______  [已知
[已知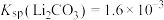 ,假设反应后溶液体积为反应前两溶液之和]。
,假设反应后溶液体积为反应前两溶液之和]。
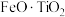 ,还含有
,还含有 、
、 、
、 等杂质)为原料合成锂离子电池的电极材料钛酸锂(
等杂质)为原料合成锂离子电池的电极材料钛酸锂( )和磷酸亚铁锂(
)和磷酸亚铁锂( )的工艺流程如下:
)的工艺流程如下:
回答下列问题:
(1)“溶浸”后溶液中的金属阳离子主要包括
 、
、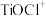
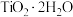 形式存在),写出上述制备
形式存在),写出上述制备 的离子方程式:
的离子方程式:(2)“溶钛”过程反应温度不能太高,其原因是
(3)“沉铁”步骤反应的化学方程式为
(4)“煅烧”制备
 过程中,
过程中, 和
和 的理论投入量的物质的量之比为
的理论投入量的物质的量之比为(5)以
 和
和 作电极组成电池,充电时发生反应:
作电极组成电池,充电时发生反应: (
(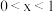 ),阳极的电极反应式为
),阳极的电极反应式为(6)从废旧
 电极中可回收锂元素。用硝酸充分溶浸废旧
电极中可回收锂元素。用硝酸充分溶浸废旧 电极,测得浸取液中
电极,测得浸取液中 ,加入等体积的碳酸钠溶液将
,加入等体积的碳酸钠溶液将 转化为
转化为 沉淀,若沉淀中的锂元素占浸取液中锂元素总量的90%,则反应后的溶液中
沉淀,若沉淀中的锂元素占浸取液中锂元素总量的90%,则反应后的溶液中 的浓度为
的浓度为 [已知
[已知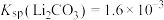 ,假设反应后溶液体积为反应前两溶液之和]。
,假设反应后溶液体积为反应前两溶液之和]。
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐1】室温下,将一定浓度的Na2CO3溶液滴入CuSO4溶液中得到了蓝色沉淀。为了确定沉淀的组成,某研究性学习小组进行了以下实验和研究。
(一)【提出假说】
假设一:两者反应只生成CuCO3沉淀;
假设二:两者反应只生成Cu(OH)2沉淀;
假设三:________________________________________ ;
(二)【理论探究】
查阅资料:CuCO3和Cu(OH)2均不带结晶水;
KSP〔CuCO3〕=1.4×10-10KSP〔Cu(OH)2〕=5.6×10-20
若只由此数据结合适当计算来判断,假设______________ 是正确的。
(三)【实验探究】
步骤一:将CuSO4溶液倒入等浓度等体积的Na2CO3溶液中并搅拌,有蓝色沉淀生成。
步骤二:将沉淀从溶液中分离出来,其操作方法为:①过滤 ,②______ ,③干燥。
步骤三:利用下图所示装置,进行定量分析:

① A装置中玻璃仪器的名称是______________ 。
② 仪器组装好后首先要进行的实验操作是_________________ 。
③ 实验结束时通入过量的空气的作用是_________________ 。
④ 数据记录:
(四)【实验结论】
利用上述数据初步判断该沉淀的成分是CuCO3和Cu(OH)2,在沉淀中二者的物质的量之比为____________________ 。若所得沉淀是纯净物而不是混合物,请写出该物质的化学式_________________________________ 。
(一)【提出假说】
假设一:两者反应只生成CuCO3沉淀;
假设二:两者反应只生成Cu(OH)2沉淀;
假设三:
(二)【理论探究】
查阅资料:CuCO3和Cu(OH)2均不带结晶水;
KSP〔CuCO3〕=1.4×10-10KSP〔Cu(OH)2〕=5.6×10-20
若只由此数据结合适当计算来判断,假设
(三)【实验探究】
步骤一:将CuSO4溶液倒入等浓度等体积的Na2CO3溶液中并搅拌,有蓝色沉淀生成。
步骤二:将沉淀从溶液中分离出来,其操作方法为:①过滤 ,②
步骤三:利用下图所示装置,进行定量分析:

① A装置中玻璃仪器的名称是
② 仪器组装好后首先要进行的实验操作是
③ 实验结束时通入过量的空气的作用是
④ 数据记录:
| B装置的质量(g) | C装置的质量(g) | D装置的质量(g) | |
| 实验前 | 15.4 | 262.1 | 223.8 |
| 实验后 | 6.1 | 264.8 | 230.4 |
(四)【实验结论】
利用上述数据初步判断该沉淀的成分是CuCO3和Cu(OH)2,在沉淀中二者的物质的量之比为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐2】镍电池广泛应用于混合动力汽车系统,电极材料由Ni(OH)2、碳粉和氧化铁等涂在铝箔上制成。由于电池使用后电极材料对环境有危害,某兴趣小组对该电池电极材料进行回收研究,设计实验流程如下:

已知:a.NiCl2易溶于水,Fe3+不能氧化Ni2+。
b.某温度下一些金属氢氧化物的Ksp及开始沉淀和完全沉淀时的理论pH如表所示:
回答下列问题:
(1)根据表中数据判断步骤②依次析出的沉淀Ⅱ________ 和沉淀Ⅲ________ (填化学式),则pH1________ pH2(填“>”、“=”或“<”),控制两种沉淀析出可利用________ (填序号)。
A.pH试纸 B.石蕊指示剂 C.pH计
(2)已知溶解度:NiC2O4>NiC2O4·H2O>NiC2O4·2H2O,则步骤③的化学方程式是________________________________________________ 。
步骤③后,过滤沉淀所需的玻璃仪器有____________ 。若过滤时发现滤液中有少量浑浊,从实验操作的角度给出两种可能的原因:______ 、 ____________________________ 。
(3)④中阳极反应产生的气体E为________ ,验证该气体的试剂为__________________________________________________________ 。
(4)试写出步骤⑥的离子方程式:______________________________ 。

已知:a.NiCl2易溶于水,Fe3+不能氧化Ni2+。
b.某温度下一些金属氢氧化物的Ksp及开始沉淀和完全沉淀时的理论pH如表所示:
| M(OH)n | Ksp | pH | |
| 开始沉淀 | 沉淀完全 | ||
| Al(OH)3 | 1.9×10-33 | 3.43 | 4.19 |
| Fe(OH)3 | 3.9×10-38 | 2.53 | 2.94 |
| Ni(OH)2 | 1.6×10-14 | 7.60 | 9.75 |
回答下列问题:
(1)根据表中数据判断步骤②依次析出的沉淀Ⅱ
A.pH试纸 B.石蕊指示剂 C.pH计
(2)已知溶解度:NiC2O4>NiC2O4·H2O>NiC2O4·2H2O,则步骤③的化学方程式是
步骤③后,过滤沉淀所需的玻璃仪器有
(3)④中阳极反应产生的气体E为
(4)试写出步骤⑥的离子方程式:
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐3】硝酸铜晶体[Cu(NO3)2•6H2O],是一种重要的化工原料,常用于农药、镀铜、搪瓷等工业。以辉铜矿(主要成分为Cu2S,含少量Fe2O3,、SiO2等杂质)为原料制备硝酸铜晶体的某工艺如图所示:

回答下列问题:
(1)“浸取”时,为了提高浸取率可采取的措施有____ (任写一点),浸取时在生成S的反应中还原剂与氧化剂的物质的量之比为____ 。
(2)滤渣2的主要成分是____ ,滤渣2与稀硝酸反应时,需向装置内通入适量空气,这样做的目的是____ 。
(3)调节溶液pH时选用的物质a可以是_____ ,几种金属离子沉淀的pH范围如图所示,“调pH”时应将溶液pH调至____ 。
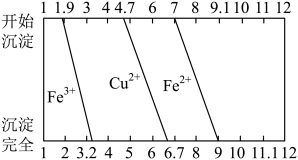
(4)操作X主要包括____ 、____ 、过滤、洗涤、干燥。
(5)用碱性锌锰干电池为电源电解硝酸铜溶液可制得铜单质。请写出电解过程中阳极的电极反应式____ 。

回答下列问题:
(1)“浸取”时,为了提高浸取率可采取的措施有
(2)滤渣2的主要成分是
(3)调节溶液pH时选用的物质a可以是

(4)操作X主要包括
(5)用碱性锌锰干电池为电源电解硝酸铜溶液可制得铜单质。请写出电解过程中阳极的电极反应式
您最近一年使用:0次



