海水是巨大的资源宝库。
Ⅰ.从海水中提取食盐和溴(海水中溴以溴化钠为主)的过程如下:

(1)步骤①工业上得到氯气的化学方程式为:_______________________________________________ 。
(2)步骤②的化学方程式为:________________________________________________ 。
(3)步骤③用SO2水溶液吸收Br2,可制得HBr和硫酸,离子方程式为:________________________ 。
Ⅱ.海洋植物如海带、海藻中含有丰富的碘元素,燃烧的灰烬中碘元素以I-的形式存在。实验室里从海藻中提取碘的流程如下:

(4)指出提取碘的过程中有关的实验操作名称:
①______________ ③______________ ④______________
(5)步骤③操作所需的玻璃仪器主要是______________________ 。
(6)提取碘的过程中,可供选择的有机试剂是______ (填字母)。
A.苯、酒精 B.汽油、醋酸 C.四氯化碳、苯
Ⅰ.从海水中提取食盐和溴(海水中溴以溴化钠为主)的过程如下:

(1)步骤①工业上得到氯气的化学方程式为:
(2)步骤②的化学方程式为:
(3)步骤③用SO2水溶液吸收Br2,可制得HBr和硫酸,离子方程式为:
Ⅱ.海洋植物如海带、海藻中含有丰富的碘元素,燃烧的灰烬中碘元素以I-的形式存在。实验室里从海藻中提取碘的流程如下:

(4)指出提取碘的过程中有关的实验操作名称:
①
(5)步骤③操作所需的玻璃仪器主要是
(6)提取碘的过程中,可供选择的有机试剂是
A.苯、酒精 B.汽油、醋酸 C.四氯化碳、苯
更新时间:2017-12-18 17:31:43
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】利用硫铁矿(主要成分FeS2)生产硫酸和绿矾(FeSO4·7H2O)的工业流程示意图如下:

(1)沸腾炉中,硫铁矿进行粉碎处理的目的是_______ 。
(2)吸收塔中,发生的主要反应的化学方程式是_______ 。
(3)反应釜中,烧渣经过反应转化为溶液I和固体。
①烧渣中的FeS在反应中做_______ 剂(填“氧化”或“还原”)。
②溶液I中所含溶质的化学式是_______ 。
(4)操作a的主要步骤是:加热浓缩、_______ 、过滤洗涤。
(5)流程中,固体X可以选择硫铁矿(FeS2)或_______ ;当固体X为硫铁矿(FeS2)时,将溶液I与固体X发生反应的离子方程式补充完整:______________ 。
FeS2+_______+_______=Fe2++ +_______
+_______

(1)沸腾炉中,硫铁矿进行粉碎处理的目的是
(2)吸收塔中,发生的主要反应的化学方程式是
(3)反应釜中,烧渣经过反应转化为溶液I和固体。
①烧渣中的FeS在反应中做
②溶液I中所含溶质的化学式是
(4)操作a的主要步骤是:加热浓缩、
(5)流程中,固体X可以选择硫铁矿(FeS2)或
FeS2+_______+_______=Fe2++
 +_______
+_______
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】氯化亚铜常用作有机合成工业中的催化剂。氯化亚铜是白色粉末,难溶于水、乙醇。潮湿的氯化亚铜在空气中迅速被氧化呈绿色。现以粗盐水(含 、
、 、
、 等杂质)、Cu、稀硫酸、
等杂质)、Cu、稀硫酸、 、
、 等为原粒合成氯化亚铜的工艺如下:
等为原粒合成氯化亚铜的工艺如下:

(1)反应Ⅰ用于提纯粗盐,加 溶液的作用是
溶液的作用是_______ 。
(2)反应Ⅱ是电解食盐水的过程,写出反应的化学方程式_______ 。
(3)写出反应Ⅳ的离子方程式(已知: 在反应中做还原剂)
在反应中做还原剂)_______ 。
(4)反应Ⅴ中 的实际耗用量比理论耗用量大的原因是
的实际耗用量比理论耗用量大的原因是_______ 。
(5)反应Ⅲ或反应Ⅴ后,过滤得到CuCl沉淀,_______ ,将纯净的 在真空干燥机内干燥2小时,冷却,密封包装即得产品。
在真空干燥机内干燥2小时,冷却,密封包装即得产品。 沉淀在真空干燥机内干燥的目的是
沉淀在真空干燥机内干燥的目的是_______ 。
 、
、 、
、 等杂质)、Cu、稀硫酸、
等杂质)、Cu、稀硫酸、 、
、 等为原粒合成氯化亚铜的工艺如下:
等为原粒合成氯化亚铜的工艺如下:
(1)反应Ⅰ用于提纯粗盐,加
 溶液的作用是
溶液的作用是(2)反应Ⅱ是电解食盐水的过程,写出反应的化学方程式
(3)写出反应Ⅳ的离子方程式(已知:
 在反应中做还原剂)
在反应中做还原剂)(4)反应Ⅴ中
 的实际耗用量比理论耗用量大的原因是
的实际耗用量比理论耗用量大的原因是(5)反应Ⅲ或反应Ⅴ后,过滤得到CuCl沉淀,
 在真空干燥机内干燥2小时,冷却,密封包装即得产品。
在真空干燥机内干燥2小时,冷却,密封包装即得产品。 沉淀在真空干燥机内干燥的目的是
沉淀在真空干燥机内干燥的目的是
您最近一年使用:0次
【推荐3】纯碱是人们生活的必需品和重要的化工原料。我国化学家侯德榜开创了侯德榜制碱法,解决了20世纪初我国的用碱问题。
I.工业碳酸钠(纯度约为98%)中常含有Ca2+、Mg2+、Fe3+、Cl-和 等杂质,为提纯工业碳酸钠,并获得试剂级碳酸钠的简要工艺流程如图:
等杂质,为提纯工业碳酸钠,并获得试剂级碳酸钠的简要工艺流程如图:

已知:碳酸钠的饱和溶液在不同温度下析出的溶质如图所示:

(1)热的Na2CO3溶液有较强的去油污能力,其原因是(用离子方程式及必要的文字加以解释____________ 。
(2)“趁热过滤”时的温度应控制在____________ 。
II.电解Na2CO3溶液制取NaHCO3溶液和NaOH溶液的装置如图所示

在阳极区发生的反应包括____________ 。阳离子交换膜允许____________ 通过。物质B是____________ (填化学式),作用为____________ 。
I.工业碳酸钠(纯度约为98%)中常含有Ca2+、Mg2+、Fe3+、Cl-和
 等杂质,为提纯工业碳酸钠,并获得试剂级碳酸钠的简要工艺流程如图:
等杂质,为提纯工业碳酸钠,并获得试剂级碳酸钠的简要工艺流程如图:
已知:碳酸钠的饱和溶液在不同温度下析出的溶质如图所示:

(1)热的Na2CO3溶液有较强的去油污能力,其原因是(用离子方程式及必要的文字加以解释
(2)“趁热过滤”时的温度应控制在
II.电解Na2CO3溶液制取NaHCO3溶液和NaOH溶液的装置如图所示

在阳极区发生的反应包括
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】海洋资源丰富,海水水资源的利用和海水化学资源(主要为NaCl和MgSO4及K、Br等元素)的利用具有非常广阔的前景。

回答下列问题:
(1)NaCl 溶液由粗盐水精制而成,为除去Mg2+和Ca2+,要加入的试剂分别为__________________ 、__________________ 。
(2)写出步骤Ⅰ中反应的总化学方程式为___________________________________ 。
(3)简述步骤Ⅱ中能析出KClO3晶体而无其他晶体析出的原因是_____________________________ 。
(4)已知MgCl2溶液受热时易水解生成Mg(OH)Cl,写出该过程的化学方程式__________________ 。
(5)为得到无水MgCl2,步骤Ⅲ的操作应为_____________________________ 。
(6)步骤Ⅳ中,电解熔融MgCl2得到的镁需要在保护气中冷却,下列气体可以作为保护气的是_____ 。
A.N2 B.H2 C. CO2 D.空气
(7)海水中溴含量为65mg·L-1。若1L海水中95%溴元素被氧化为Br2经热空气吹出,溴单质残留量3%。最后用SO2将90%Br2还原成Br-,所得溶液体积为50mL。此过程的目的为________________ 。所得溶液中溴离子浓度为海水中溴离子浓度的_____________ 倍(精确到0.1)。

回答下列问题:
(1)NaCl 溶液由粗盐水精制而成,为除去Mg2+和Ca2+,要加入的试剂分别为
(2)写出步骤Ⅰ中反应的总化学方程式为
(3)简述步骤Ⅱ中能析出KClO3晶体而无其他晶体析出的原因是
(4)已知MgCl2溶液受热时易水解生成Mg(OH)Cl,写出该过程的化学方程式
(5)为得到无水MgCl2,步骤Ⅲ的操作应为
(6)步骤Ⅳ中,电解熔融MgCl2得到的镁需要在保护气中冷却,下列气体可以作为保护气的是
A.N2 B.H2 C. CO2 D.空气
(7)海水中溴含量为65mg·L-1。若1L海水中95%溴元素被氧化为Br2经热空气吹出,溴单质残留量3%。最后用SO2将90%Br2还原成Br-,所得溶液体积为50mL。此过程的目的为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】中国有广阔的海岸线,建设发展海洋经济、海水的综合利用大有可为。
I.空气吹出法工艺,是目前“海水提溴”的最主要方法之一。其工艺流程如下图所示,试回答下列问题:

(1)以上步骤Ⅰ中已获得游离态的溴,步骤Ⅱ又将之转变成化合态的溴,其目的是________ 。
(2)步骤②通入热空气或水蒸气吹出Br2,利用了溴的________ 。
A 氧化性 B 还原性 C 挥发性 D腐蚀性
(3)流程Ⅱ中涉及的离子反应方程式如下,请在下面横线内填入适当的化学计量数:
___Br2+___=___+___Br-+___CO2↑________ 。
(4)上述流程中吹出的溴蒸气,也可先用二氧化硫水溶液吸收,再用氯气氧化后蒸馏。写出溴与二氧化硫水溶液反应的离子方程式:________ 。
(5)流程Ⅲ蒸馏过程中,温度应控制在80~90℃。温度过高或过低都不利于生产,请解释原因:_________ 。
Ⅱ.目前世界上60%的镁是从海水中提取的。海水提镁的主要流程如下:

(6)操作A是_________ ,试剂a是__________ 。
(7)由无水MgCl2制取Mg的化学方程式是_________ 。从考虑成本和废物循环利用的角度,副产物可以用于________ 。
I.空气吹出法工艺,是目前“海水提溴”的最主要方法之一。其工艺流程如下图所示,试回答下列问题:

(1)以上步骤Ⅰ中已获得游离态的溴,步骤Ⅱ又将之转变成化合态的溴,其目的是
(2)步骤②通入热空气或水蒸气吹出Br2,利用了溴的
A 氧化性 B 还原性 C 挥发性 D腐蚀性
(3)流程Ⅱ中涉及的离子反应方程式如下,请在下面横线内填入适当的化学计量数:
___Br2+___=___+___Br-+___CO2↑
(4)上述流程中吹出的溴蒸气,也可先用二氧化硫水溶液吸收,再用氯气氧化后蒸馏。写出溴与二氧化硫水溶液反应的离子方程式:
(5)流程Ⅲ蒸馏过程中,温度应控制在80~90℃。温度过高或过低都不利于生产,请解释原因:
Ⅱ.目前世界上60%的镁是从海水中提取的。海水提镁的主要流程如下:

(6)操作A是
(7)由无水MgCl2制取Mg的化学方程式是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】
(1)海水是巨大的资源宝库,工业上从海水中提取食盐和溴的过程如下:

操作Ⅱ发生反应的离子方程式为____________________ ;
可以用碳酸钠溶液代替操作Ⅱ中的二氧化硫水溶液,生成物中溴的化合价分别为+5和-1价,操作Ⅲ中如果用稀硫酸代替氯气,则操作Ⅲ中发生反应的离子方程式为_________________ 。
(2)溴苯是一种化工原料,可以用溴和苯反应合成。实验室合成溴苯的装置示意图如下:

下表为苯、溴和溴苯的相关数据:
回答下列问题:
在A中加入30.0 mL无水苯和少量铁屑。在B中小心加入8.0 mL液态溴。向A中滴加液溴,反应一段时间后,点燃酒精灯加热蒸馏。
①A的容积最适合的是________ (填编号)。
a.25 mL b.50 mL c.100 mL d.250 mL
②收集溴苯时,应根据________ (填“C1”或“C2”)所显示的温度,其温度应为__________________ 。
③在反应开始后到收集溴苯之前,应先将F装置连接在D装置后,用它可承接的物质有___________ (填化学式)。
④某化学小组设计如下实验方案,证明苯和溴发生的是取代反应而不是加成反应。
第一步:取少量反应后F装置中的溶液于试管中;第二步:向其中加入过量的稀硝酸;第三步:继续滴加少量的硝酸银溶液。如果有浅黄色沉淀生成则证明苯和溴发生的是取代反应。
该实验方案________ (填“合理”或“不合理”),理由是___________________________ 。
(1)海水是巨大的资源宝库,工业上从海水中提取食盐和溴的过程如下:

操作Ⅱ发生反应的离子方程式为
可以用碳酸钠溶液代替操作Ⅱ中的二氧化硫水溶液,生成物中溴的化合价分别为+5和-1价,操作Ⅲ中如果用稀硫酸代替氯气,则操作Ⅲ中发生反应的离子方程式为
(2)溴苯是一种化工原料,可以用溴和苯反应合成。实验室合成溴苯的装置示意图如下:

下表为苯、溴和溴苯的相关数据:
| 苯 | 溴 | 溴苯 | |
| 密度/g·cm-3 | 0.88 | 3.10 | 1.50 |
| 沸点/℃ | 80 | 59 | 156 |
| 水中溶解度 | 微溶 | 微溶 | 微溶 |
在A中加入30.0 mL无水苯和少量铁屑。在B中小心加入8.0 mL液态溴。向A中滴加液溴,反应一段时间后,点燃酒精灯加热蒸馏。
①A的容积最适合的是
a.25 mL b.50 mL c.100 mL d.250 mL
②收集溴苯时,应根据
③在反应开始后到收集溴苯之前,应先将F装置连接在D装置后,用它可承接的物质有
④某化学小组设计如下实验方案,证明苯和溴发生的是取代反应而不是加成反应。
第一步:取少量反应后F装置中的溶液于试管中;第二步:向其中加入过量的稀硝酸;第三步:继续滴加少量的硝酸银溶液。如果有浅黄色沉淀生成则证明苯和溴发生的是取代反应。
该实验方案
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】海水中含有丰富的人体不可缺少的碘元素,它以碘离子的形式存在。某学生为探究海带中碘元素的存在,按如图流程进行了实验:

回答下列问题:
(1)A步骤的操作名称是____ ;A步骤用到的主要玻璃仪器是____ (选填下列字母代号)
a.漏斗 b.分液漏斗 c.量筒 d.蒸发皿
(2)B步骤中加入的试剂是____ 。
(3)通入Cl2时反应的离子方程式为____ ,其中氧化剂是____ 。
(4)下列试剂,可用来萃取碘水中的碘的有:____ (填字母代号)
A.酒精 B.苯 C.水 D.四氯化碳

回答下列问题:
(1)A步骤的操作名称是
a.漏斗 b.分液漏斗 c.量筒 d.蒸发皿
(2)B步骤中加入的试剂是
(3)通入Cl2时反应的离子方程式为
(4)下列试剂,可用来萃取碘水中的碘的有:
A.酒精 B.苯 C.水 D.四氯化碳
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】以干海带为原料提取碘单质和氯化钾的过程主要分三步:完成下列填空:
(1)步骤一:灼烧干海带,使其灰化后用热水浸泡、过滤,制得原料液,含有氯化钾等物质。实验室灼烧海带应放在____ (填写仪器名称)中加热,选用热水而不是冷水浸泡海带灰的目的是____ 。
(2)步骤二:原料液经结晶过滤分离出氯化钾后,向滤液中通适量氯气氧化I-,制得富碘溶液。实验室模拟氧化过程的实验装置如图所示。
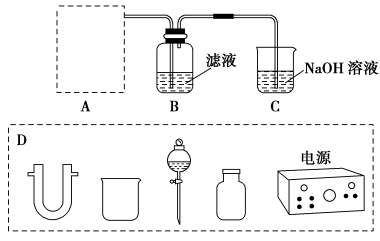
装置中A部分用于制取氯气,实验室制取氯气通常有两种方案:一是在强酸性条件下用氧化剂氧化Cl-;二是电解法。限用图D中的仪器(支撑仪器、导管、导线、石墨棒和橡皮塞除外),能实现的反应是___ (选填编号)。
a.2NaCl(s)+MnO2+2H2SO4(浓) MnSO4+Cl2↑+Na2SO4+2H2O
MnSO4+Cl2↑+Na2SO4+2H2O
b.2KMnO4+16HCl(浓)→2MnCl2+2KCl+5Cl2↑+8H2O
c.2NaCl+2H2O 2NaOH+Cl2↑+H2↑
2NaOH+Cl2↑+H2↑
d.4HCl(浓)+MnO2 MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
广口瓶B中发生反应的离子方程式是____ 。装置C中NaOH的作用是___ 。
(3)步骤三:取100 mL B中富碘溶液,按如下流程分离碘单质。
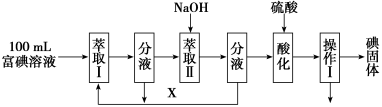
萃取Ⅱ和酸化过程发生的离子反应方程式分别是:
3I2+6OH-=5I-+IO3-+3H2O;____ ;
萃取剂X应选择____ (选填编号)。
a.100mL苯 b.10mL乙醇 c.10 mLCCl4 d.10mL己烯
实验室进行萃取操作的仪器是_____ 。操作Ⅰ的名称是___ 。
(4)分离出的KCl样品中常含有少量NaCl和K2CO3等物质,设计实验用沉淀法测定氯化钾样品中K2CO3的质量分数:①要用到的化学试剂是___ (填写化学式);②要测定的物理量是_____ 。
(1)步骤一:灼烧干海带,使其灰化后用热水浸泡、过滤,制得原料液,含有氯化钾等物质。实验室灼烧海带应放在
(2)步骤二:原料液经结晶过滤分离出氯化钾后,向滤液中通适量氯气氧化I-,制得富碘溶液。实验室模拟氧化过程的实验装置如图所示。

装置中A部分用于制取氯气,实验室制取氯气通常有两种方案:一是在强酸性条件下用氧化剂氧化Cl-;二是电解法。限用图D中的仪器(支撑仪器、导管、导线、石墨棒和橡皮塞除外),能实现的反应是
a.2NaCl(s)+MnO2+2H2SO4(浓)
 MnSO4+Cl2↑+Na2SO4+2H2O
MnSO4+Cl2↑+Na2SO4+2H2Ob.2KMnO4+16HCl(浓)→2MnCl2+2KCl+5Cl2↑+8H2O
c.2NaCl+2H2O
 2NaOH+Cl2↑+H2↑
2NaOH+Cl2↑+H2↑d.4HCl(浓)+MnO2
 MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O广口瓶B中发生反应的离子方程式是
(3)步骤三:取100 mL B中富碘溶液,按如下流程分离碘单质。

萃取Ⅱ和酸化过程发生的离子反应方程式分别是:
3I2+6OH-=5I-+IO3-+3H2O;
萃取剂X应选择
a.100mL苯 b.10mL乙醇 c.10 mLCCl4 d.10mL己烯
实验室进行萃取操作的仪器是
(4)分离出的KCl样品中常含有少量NaCl和K2CO3等物质,设计实验用沉淀法测定氯化钾样品中K2CO3的质量分数:①要用到的化学试剂是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】海洋是一座巨大的化学资源宝库,如图是从海水中或海产品中提取若干种化学物质的流程图。
Ⅰ.海水提溴的流程如图所示:
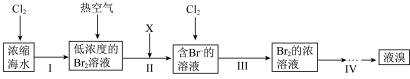
(1)X可用 气体,该反应的离子方程式为
气体,该反应的离子方程式为___________ 。
(2)步骤Ⅳ包含蒸馏,该操作不需要下列仪器中的___________ (填字母)。
a. b.
b. c.
c.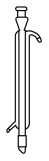 d.
d.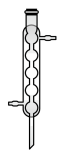 e.
e. f.
f.
Ⅱ.兴趣小组同学按如图实验过程,证明海带中存在碘元素。
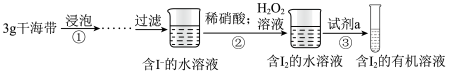
(3)实验时需要将干海带放入___________ 中灼烧(填仪器名称)
(4) 的作用是
的作用是___________ (用离子方程式解释)
(5)试剂a不能选择的是(填序号)___________。
(6)操作③的名称是___________ 。
(7)操作③中需要振荡排放气体,放气时分液漏斗的状态是___________。
Ⅰ.海水提溴的流程如图所示:

(1)X可用
 气体,该反应的离子方程式为
气体,该反应的离子方程式为(2)步骤Ⅳ包含蒸馏,该操作不需要下列仪器中的
a.
 b.
b. c.
c. d.
d. e.
e. f.
f.
Ⅱ.兴趣小组同学按如图实验过程,证明海带中存在碘元素。

(3)实验时需要将干海带放入
(4)
 的作用是
的作用是(5)试剂a不能选择的是(填序号)___________。
A. | B.苯 | C.酒精 | D.裂化汽油 |
(7)操作③中需要振荡排放气体,放气时分液漏斗的状态是___________。
A.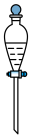 | B. | C.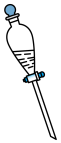 | D.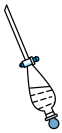 |
您最近一年使用:0次



